Autor : LÃģpez Ana M.1, Abrate Vanesa del V.1, Echazarreta AndrÃĐs2, Arias Sergio3, Del Olmo Ricardo4, Colodenco Federico4, Arce Santiago C.5, Giugno Eduardo6
1 Hospital Privado Universitario de CÃģrdoba, 2Hospital Interzonal Especializado en agudos y crÃģnicos San Juan de Dios, La Plata, 3Instituto Nacional de Enfermedades Respiratorias Emilio Coni, Ministerio de Salud de la NaciÃģn, Santa Fe, 4Hospital MarÃa Ferrer, Ciudad AutÃģnoma de Buenos Aires, 5Instituto de Investigaciones MÃĐdicas A. Lanari, Universidad de Buenos Aires, Ciudad AutÃģnoma de Buenos Aires, 6 Hospital CetrÃĄngolo, provincia de Buenos Aires
https://orcid.org/0000-0001-7719-8682
https://orcid.org/0000-0003-4997-5768
https://orcid.org/0000-0002-1178-4299
https://orcid.org/0000-0002-8375-1939
https://orcid.org/0000-0003-2629-3262
Correspondencia : Vanesa Abrate E-mail: abrate.vanesa@gmail.com
RESUMEN
Introducción: Asma y EPOC son enfermedades
heterogéneas, algunos pacientes comparten características
clínicas de ambas. Existen incertidumbres en los criterios para definir
superposición asma-EPOC (ACO) y la prevalencia es entre el 15% y el 25%
de la población adulta con obstrucción crónica del flujo
aéreo. Motiva este estudio determinar la prevalencia de ACO en
Argentina, que es desconocida.
Objetivos: Primario: Determinar prevalencia de ACO en el
estudio EPOC-AR. SeÂcundarios: Evaluar y analizar las características
clínicas de los pacientes con ACO, la gravedad de los síntomas,
la frecuencia y gravedad de exacerbaciones. Describir y comparar el tratamiento
entre ACO vs. EPOC puros.
Base de datos del estudio EPOC.AR: Espirometrías,
asma, atopía o rinitis, síntomas respiratorios: CAT (prueba de
evaluación de EPOC) y mMRC (Medical Research Council modificado), frecuencia de
exacerbaciones/año previo, comorbilidades y tratamientos. Guías GOLD
2017 para determinar grados de obstrucción espirométrica
y Grupos A, B, C y D.
Criterios diagnósticos de ACO (comité
expertos USA, Europa del Este y Asia-Denver 2015):
CRITERIOS MAYORES: 1. Obstrucción persistente (FEV1/FVC pos-BD
<70% o LIN) en ≥ 40 años. 2. TBQ ≥ 10
paquetes/año, contaminación ambiental o biomasa. 3. Historia
documentada de asma antes de los 40 años o respuesta pos-BD ≥ 400 mL en FEV1.
CRITERIOS MENORES: 1. Historia documentada de
atopía o rinitis alérgica. 2. ResÂpuesta pos-BD en FEV1 > 200 mL. 3. Recuento de eosinófilos
en sangre periférica ≥ 300 células-Ul-1 (no realizado en EPOC.AR).
Prueba de Chi-cuadrado, Chi-cuadrado de Pearson,
razón de verosimilitud, asociación lineal por lineal.
Resultados: EPOC (n498), n95 con criterios de ACO,
masculino (53,4%) y edad proÂmedio 63,6 años.
El 1%, sin asma y respuesta BD ≥ 400 mL; el 32,7%, asmáticos (3,6% respuesta BD ≥
400 mL y el 14,5%, entre 200-400 mL);
n23 respuesta BD ≥ 400 mL (4,6%). PrevalenÂcia
ACO: 19,08% (IC 15,6-22,5) y del 2,6% del total de la población de
EPOC.AR. En población ACO vs. EPOC, se detectó: menor promedio de
edad y de FEV1 pre
BD (p < 0,01), mayor respuesta BD (p < 0,05), mayor frecuencia de
sibilancias (p < 0,01; IC 2,75-7,64), mayor frecuencia de diagnóstico
previo de asma (p < 0,01; IC 3,79-10,05) y el 26,08% tenían
antecedentes familiares de asma. Mayor uso de ATB (p < 0,05) e ICS/LABA (p
< 0,05; IC 1,1-5,3). Mayor frecuencia de exacerbaciones (12,47%; IC
9,56-15,39) que motivaron indicación de medicación en un 90,48% y
2,49 veces más de alteraciones en actividades diarias y ausentismo
laboral. No se registraron diferencias significativas entre pacientes con ACO
frente a EPOC puros en frecuencia de grupos A, B, C y D.
Conclusiones: La prevalencia de ACO fue del 19,08% en
pacientes EPOC del esÂtudio EPOC.AR; tenían significativamente menor
edad, mayor grado de obstrucción, frecuencia de sibilancias, uso de
antibióticos/año previo y CI (LABA/CI). Destacamos la importancia
de identificar este fenotipo para un tratamiento adecuado por sus impliÂcancias
clínicas, y deterioro en calidad de vida.
Palabras clave: Asma, Enfermedad Pulmonar Obstructiva Crónica, Tabaquismo
ABSTRACT
Background: Asthma and COPD are
heterogeneous diseases, and some patients share clinical features of both
conditions. There are uncertainties about the criteria to define asthma-COPD
overlap (ACO), and its prevalence is 15-25% in the adult population with
chronic airflow obstruction. The purpose of this study was to determine the
prevalence of ACO in Argentina, which is unknown.
Objectives: Primary: to determine
the prevalence of ACO in the EPOC.AR study. Secondary: to evaluate and analyze
the clinical features of patients with ACO, the severity of the symptoms, and
the frequency and severity of exacerbations. to
describe and compare the treatment of ACO with that of pure COPD.
Database of the EPOC.AR study: spirometries, asthma, atopy or
rhinitis, respiratory symptoms: CAT (COPD Assesment
Test) and mMRC (Modified Medical Research Council) scale,
frequency of exacerbations/previous year, comorbidities and treatments. 2017
GOLD Guides (Global Initiative for Chronic Obstructive Lung Disease) to
determine airflow obstruction degrees and Groups A, B, C, and D.
ACO diagnostic criteria (expert
committee from USA, East Europe and Asia that took place in Denver, 2015):
MAJOR CRITERIA: 1. Persistent
obstruction (post-BD [bronchodilator] FEV1/FVC
(forced expiratory volume in the first second/forced vital capacity) < 70%
or LLN [lower limit of normal] ) in ≥ 40 years.
2. SM (smoking) ≥ 10 packs/year, air pollution
or biomass. 3. Documented history of asthma before 40 years or post-BD response
≥ 400 ml in FEV1.
MINOR CRITERIA: 1. Documented
history of atopy or allergic rhinitis. 2. Post-BD
response in FEV1 >
200 ml. 3. Peripheral blood eosinophil count ≥ 300 cells-Ul-1 (not
performed in EPOC.AR).
Chi-Square Test,
Pearsonâs Chi Square Test, likelihood ratio, linear-by-linear association.
Results: COPD (n 498), n 95 with
ACO criteria, males (53.4%), mean age 63.6 years.
1% without asthma and BD response
≥ 400 ml; 32.7% asthmatics (3.6% with BD response ≥ 400 ml and
14.5% between 200-400 ml); n 23 with BD response ≥ 400 ml (4.6%). ACO
prevalence: 19.08% (CI [Confidence Interval] 15.6-22.5) and 2.6% of the total
population of EPOC.AR. In the comparison between the ACO and COPD populations,
we detected the following: lower mean age and pre-BD FEV1 (p < 0.01), higher frequency of BD
response (p < 0.05), higher frequency of sibilance (p < 0.01; CI
2.75-7.64), higher frequency of previous asthma
diagnosis (p < 0.01; CI 3.79-10.05); and 26.08% had family history of
asthma. Greater use of ATBs (antibiotics) (p < 0.05) and
ICS (inhaled corticosteroids)/ LABA (long-acting beta- adrenergic agonists) (p
< 0.05; CI 1.1-5.3). Higher frequency of
exacerbations (12.47%; CI 9.56-15.39) that motivated the indication of
medication in 90.48% and 2.49 times more alterations in daily activities and
absence from work.
There werenât any significant
differences between patients with ACO and pure COPD regarding frequency of
groups A, B, C and D.
Conclusions: the prevalence of
ACO was 19.08% in the COPD patients of the EPOC. AR study; they were
significantly younger, with higher degree of obstruction, frequency of
sibilance, use of antibiotics/previous year and inhaled corticosteroids
(LABA/IC). We emphasize the importance of identifying this phenotype in order
to use a suitable treatÂment, given its clinical implications and deterioration
in quality of life.
Key word: Asthma,
Pulmonary Disease, Chronic Obstructive, Smoking
Recibido: 14/07/2021
Aceptado: 13/03/2022
INTRODUCCIÓN
Con el creciente reconocimiento de que el asma y la EPOC
son enfermedades heterogéneas y que comparten similitudes
clínicas, funcionales e inÂflamatorias, la atención se ha
dirigido a quienes tienen características clínicas de ambas
enfermeÂdades, a los que se ha calificado como pacientes con
superposición asma-EPOC (ACO)1, 2 . En pacientes fumadores, el asma se
considera un factor de riesgo para desarrollar EPOC, como se ha demostrado en
el estudio epidemiológico de Tucson, con un increÂmento del riesgo doce
veces superior en asmáticos fumadores frente a fumadores no
asmáticos3 .
Otro dato que sustenta la coexistencia de la suÂperposición
asma-EPOC, es que se ha demostrado que la hiperactividad bronquial es un
predictor independiente de EPOC y de mortalidad de causa respiratoria en
estudios poblacionales4,
así como también un indicador de riesgo de la declinación
acelerada de la función pulmonar en pacientes con EPOC leve5.
No se dispone actualmente de evidencias que soporten las
decisiones terapéuticas en los pacienÂtes con ACO, ya que
tradicionalmente han sido sistemáticamente excluidos en los protocolos
de investigación para mantener la homogeneidad de la población en
quienes cumplían con las definiÂciones estándar de EPOC o asma1.
Aproximadamente uno de cada cuatro pacientes con EPOC
tiene características asmáticas; y fueÂron calificados
recientemente como ACO por la IniÂciativa Global para el Asma (GINA) y la
Iniciativa Global EPOC (GOLD). Por lo tanto, identificarlos representa, en la
vida real, un desafío diagnóstico y terapéutico1,
sumado a que la definición precisa de ACO es todavía
controvertida6 .
No obstante, hay acuerdo emergente de que alÂgunas de las
características claves de ACO incluyen la limitación persistente
del flujo aéreo, definida como una relación VEF1/CVF < 70% posbroncoÂdilatador,
en individuos sintomáticos de 40 o más años con una
historia bien documentada de asma en la niñez o edad adulta temprana y
exposición al humo de cigarrillos (más de 10 p/y) o a biomasa1.
En los pacientes con EPOC, el diagnóstico de ACO
desempeña un papel fundamental para sumar la prescripción de un
esteroide inhalado (ICS). Por el contrario, en los pacientes asmáticos,
cuando se diagnostica ACO, no existen significativas imÂplicancias
terapéuticas, porque la terapia inicial con la combinación de
beta agonistas de acción prolongada más ICS, no difiere entre los
asmáticos puros y los que tienen superposición con EPOC2.
El impacto del correcto diagnóstico para un
tratamiento adecuado es crucial porque los paÂcientes con ACO tienen una mayor
carga de síntomas, como disnea y tos, mayor riesgo de una
disminución rápida del FEV1,
de exacerbaciones, hospitalizaciones y mortalidad por EPOC1
cuando se comparan, con pacientes con EPOC o asmáticos
puros.
La motivación para realizar este estudio de la
prevalencia de la superposición asma-EPOC, a través de la base de
datos del estudio epidemiolóÂgico EPOC AR7 , es conocer la realidad en nuestro
país, ya que no existe hasta la fecha información sobre esta.
Objetivos
Primario: Determinar la prevalencia de ACO en el estudio de epidemiológico
de prevalencia de EPOC en la Argentina7 .
Secundarios
1. Evaluar y analizar las características
clínicas de los pacientes con ACO en comparación con los
pacientes EPOC.
2. Describir y comparar el tratamiento recibido por los
pacientes con ACO y EPOC.
MATERIAL Y MÉTODOS
Este estudio es un subanálisis
del estudio EPOC AR, que incluye todos los pacientes diagnosticados como EPOC,
dentro de este grupo se diferenciaron aquellos que tenían los criterios
diagnósticos de ACO. El estudio EPOC. AR.7
es multicéntrico, de corte
transversal, de base poblacional seleccionada aleatoriamente mediante muestreo
por conglomerados en seis aglomerados urbanos de Argentina, con el objetivo de
establecer la prevalencia de EPOC y evaluar las características
clínicas y sociodemográficas de los sujetos, tratamiento y
diversos factores de riesgo. El estudio se llevó adelante entre agosto
de 2014 y mayo de 2016.
Los aglomerados urbanos seleccionados fueron: La Plata,
Rosario, Ciudad Autónoma de Buenos Aires, Zona Norte del Gran Buenos
Aires, Córdoba y Mendoza. Los datos se seleccionaron mediante muestreo
probabilístico polietápico por
conglomerados basados en unidades de área cartográfica y descrito
con mayor detalle en el material suplementario. Se invitó a participar
del estudio a cada persona seleccioÂnada y, en caso de que aceptaran, se
solicitó la firma del consentimiento informado7 .
Definición de términos
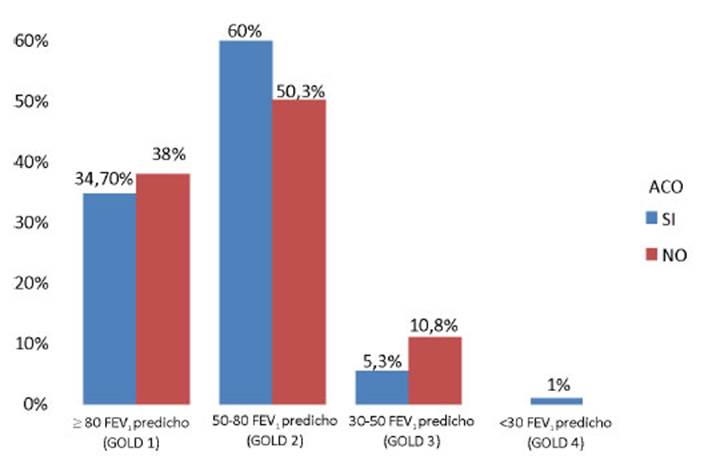
Se definió EPOC como un cociente FEV1/FVC posbronÂcodilatador <0,7 y se utilizó la
clasificación GOLD 2017 para definir el grado de obstrucción y
valoración multidiÂmensional ABCD10 .
Clasificación de GOLD 201710
Global Strategy for the Diagnosis, Management and Prevention of
COPD, Global Initiative for Chronic Obstructive Lung Disease (GOLD) 2017.
http://goldcopd.org
Definición de ACO
Se utilizarán como criterios diagnósticos
de ACO los recoÂmendados por un panel de discusión de expertos de NorteÂamérica,
Europa del Este y Asia, realizado en Denver (CO, EE. UU.) el 16 de mayo de
2015.
Se trata de tres criterios mayores y tres menores. El
Comité recomienda la presencia de los tres criterios mayores y, por lo
menos, 1 de los menores.
Si bien el Comité reconoce que es una
definición arbitraria y que requiere validación, estos son
criterios dinámicos y con la adición de nuevos datos se
requerirán modificaciones11.
CRITERIOS MAYORES
1. Obstrucción persistente al flujo de la
vía aérea (VEF1/CVF pos-BD < 70% o LIN) en individuos de 40
años o más.
2. Tabaquismo de, al menos, 10 paquetes/años o
exposición a la contaminación ambiental en el interior o exterior
(por ejemplo, biomasa).
3. Historia documentada de asma antes de los 40
años o resÂpuesta broncodilatadora >400 mL
en el VEF1.
CRITERIOS MENORES
1. Historia documentada de atopía o rinitis
alérgica.
2. Respuesta broncodilatadora en el VEF1 < 200 mL.
3. Recuento de eosinófilos
en sangre periférica ≥ 300 células- Ulâ1.
NOTA: Se excluirá dentro de los criterios menores
la presencia de eosinofilia en sangre
periférica, ya que a los pacientes del estudio EPOC.AR no se les
realizaron extracÂciones de sangre para ningún tipo de estudio.
EXACERBACIONES
Se definieron las exacerbaciones según las
Guías GOLD 201710 como un
empeoramiento agudo de los síntomas que requieren una terapia adicional.
Se clasifican de la siguiente manera:
1. LEVES: Tratadas con broncodilatadores (BD) de
acción corta (SABD).
2. MODERADAS: Tratadas con SABD más
antibióticos o corticoides orales.
3. Graves: El paciente requiere hospitalización o
visitas al servicio de emergencia. También pueden asociarse a insuÂficiencia
respiratoria aguda.
Se analizaron, en los pacientes diagnosticados como EPOC,
las variables siguientes:
1. Datos de la Historia Clínica:
âĒ Antecedentes de tabaquismo (paquetes/año).
âĒ Antecedentes de asma, atopía o rinitis
alérgica.
âĒ Síntomas respiratorios: Cuestionarios CAT
(prueba de evaluación de EPOC)8 y Cuestionario mMRC (Medical Research Council
modificado)9.
âĒ Frecuencia de exacerbaciones en el año previo
con interÂnaciones y sin estas.
âĒ Comorbilidades sistémicas.
âĒ Tratamiento recibido.
2. Espirometrías prebroncodilatador y posbroncodilatador.
Análisis estadístico
Prueba de Chi-cuadrado, Chi-cuadrado de Pearson,
razón de verosimilitud, asociación lineal por lineal. El
análisis estadístico se realizará usando el programa InfoStad 2014e. Se considerará como valor de
significancia de âpâ < 0,05.
RESULTADOS
La población que presentaba criterios
diagnósticos de EPOC fue de 504 pacientes y no había datos
disponibles en 6, por lo que la población analizada correspondió
a 498 pacientes (n = 498). La prevaÂlencia de EPOC fue de 14,5% (IC:
13,4-15,7%). En esta población, se detectaron 95 pacientes con criÂterios
de ACO, con predominio del sexo masculino (53,4%) y con una edad promedio de
63,6 años (DS Âą 10,83), distribuidas en un 28% entre edades de 40-59
años, un 52% entre 60 años y 75 años y el 20% de la
población era mayor de 75 años.
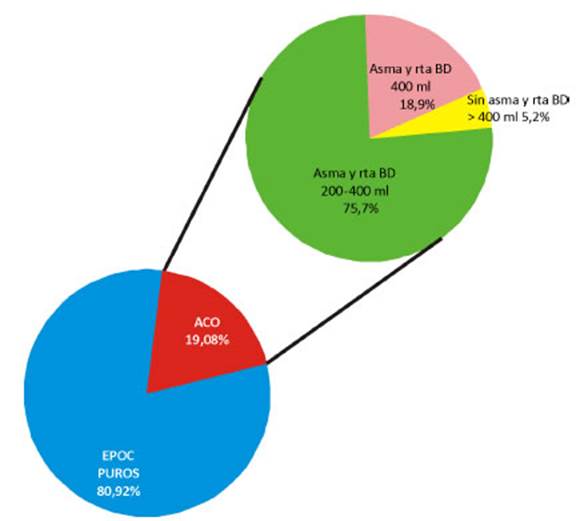
La prevalencia de ACO en la población con criterios
diagnósticos de EPOC fue del 19,08% (IC95%:15,6-22,5), lo que
corresponde al 2,6% del total de la población del estudio EPOC.AR. La
prevalencia de los casos compatibles con ACO, según los criterios
diagnósticos utilizados, se preÂsentan en la Figura 1, donde un 1%
corresponde a pacientes sin antecedentes de asma y con una respuesta BD ≥
400 mL; un 32,7% de los pacientes eran
asmáticos, pero con diferentes respuestas broncodilatadoras: un 3,6%
tuvieron una respuesta BD ≥ 400 mL y en un
14,5% la respuesta BD fue entre 200 mL y 400 mL (Figura 2).
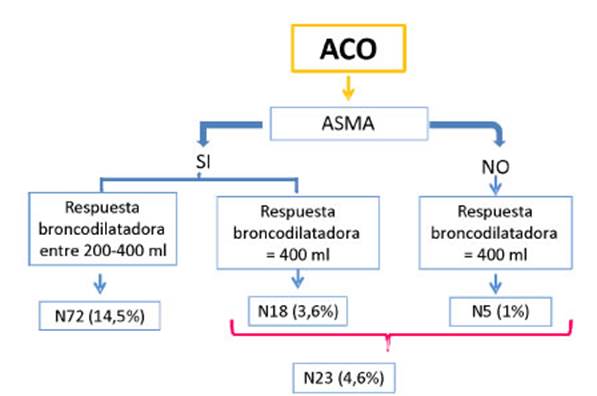
Un 4,6% del total de la población con criterios
diagnósticos de ACO, que incluyó pacientes asmáÂticos y no
asmáticos (n = 23) tenían una respuesta BD ≥ 400 mL.
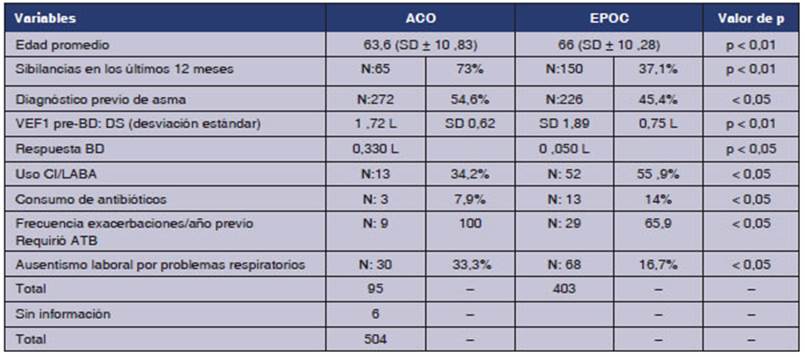
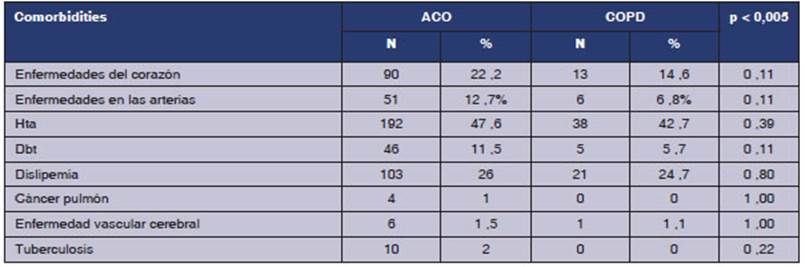
En la Tabla 1, se compararon las poblaciones de pacientes
con EPOC frente a aquellos con criterios diagnósticos de ACO. se
detectó en estos últimos un menor promedio de edad y del FEV1 pre-BD,
ambos con significancia estadística (p < 0,01). También
hubo diferencias significativas en las espirometrías
pos-BD, ya que se encontró una mayor respuesta BD (p < 0,05)
en los pacientes con ACO. Además, se encontró una mayor
frecuencia de sibilancias (p < 0,01; IC 2,75%-7,64%), un mayor
incremenÂto de diagnósticos previos de asma y bronquitis (p <
0,01; IC 3,79%-10,05%) y en un 26,08% (IC 22,16%-29,99%) el paciente
tenía conocimientos de que algún familiar tuvo diagnóstico
de asma. Si consideramos la medicación de los pacientes con ACO, estos
tenían un mayor uso de corticoides inhalados combinados con
broncodilatadores B2 agonistas
de acción prolongada (ICS/LABA) p < 0,05; IC 1,1%-5,3%. En el
grupo de pacientes con ACO, la frecuencia de exacerbaciones fue mayor (12,47%; IC 9,56%-15,39%), con un incremento en el consumo
de ATB (p < 0,05) indicados por profesionales de la salud en un
90,48%. Los paÂcientes con ACO presentaron 2,49 veces (IC95%: 1,50%-4,15%)
más probabilidad de tener problemas respiratorios impidieron sus
actividades diarias o provocaron ausentismo laboral vs. pacientes con EPOC
puros (p < 0,05).
DISCUSION
Existen amplias variaciones en la prevalencia de ACO que
están relacionadas con el tipo de poblaÂción analizada
(análisis de bases de datos o estudios clínicos), los diferentes
criterios empleados para la identificación de ACO y la definición
de asma y de EPOC6;
también influye el grupo etario (todos los adultos o los mayores de 40
años)
La prevalencia de ACO en la población
general oscila entre el 1,6% y el 4,5%, en los pacientes con EPOC entre el
12,1% y el 55,2%, y en pacientes con asma entre el 13,3% y el 61%13.
En pacientes EPOC, en el estudio UPLIFT,
cuando se consideró el criterio de una respuesta significativa al BD, la
prevalencia fue del 52%16.
En un metaanálisis
publicado recientemente, que incluyó diecinueve estudios, la prevalencia
de ACO entre los pacientes diagnosticados de EPOC fue del 27% en estudios
poblacionales y del 28% en estudios de pacientes hospitalarios6.
En España, los resultados del reciente
estudio CHAIN, que incluyó 831 pacientes con EPOC pro cedentes de 36
hospitales universitarios, mostraÂron una prevalencia de ACO (se utilizaron
criterios específicos mayores y menores modificados de GesEPOC) del 15%, estos resultados son similares a los del
estudio COPDGene, que fue del 13%6.
En nuestro trabajo, la prevalencia de ACO fue
del 19,08% (IC 15,6%-22,5%) en la población con EPOC del estudio EPOC.AR
y representó un 2,6% del total de la población de este estudio de
base poÂblacional (N 3.469), porcentajes que coinciden con los datos
reportados en la bibliografía. No obstante, en definitiva, si bien la
prevalencia de ACO varía ampliamente según la fuente considerada
y el criÂterio utilizado para definirlo, se podría establecer que su
prevalencia varía entre el 1,6% y el 4,5% de la población general
adulta y entre el 15% y el 25% de la población adulta con
obstrucción crónica del flujo aéreo6.
Si bien Llanos y cols. reportan que los
pacientes con EPOC tenían menor FEV1
prebroncodilatador que los pacientes
con ACO14, en nuestro
estudio obÂservamos que los pacientes con ACO tenían signiÂficativamente
un menor FEV1 prebroncodilatador.
Varios estudios demostraron que individuos
con ACO tienen una mayor frecuencia de síntomas respiratorios comparado
con aquellos con EPOC puÂros. Maselli y cols.15
encontraron que este grupo de pacientes refieren una mayor
frecuencia de disnea y un gran impacto en la calidad de vida. El autor menciona
que no existe en la actualidad evidencia de este empeoramiento en los
síntomas, pero puede ser debido a un double
hit, con afección tanto de la vía aérea como del
alvéolo e incremento de la susceptibilidad de
padecer exacerbaciones. En líneas generales, el grupo de pacientes con
ACO presentan más síntomas, peor calidad de vida y mayor riesgo
de exacerbaciones que los pacientes con EPOC, aunque mejor supervivencia13.
Estos hallazgos los observamos en nuestro estudio, ya que los pacientes con ACO
tenían mayor frecuencia de sibilancias y de diagnóstico previo de
asma y bronquitis.
Tanto los pacientes con asma como aquellos con EPOC se
caracterizan por deterioro agudo de los síntomas respiratorios, y estos
eventos tienen un significativo impacto en la calidad de vida y en los costos
en salud7.
En varias cohortes, comparaban solo pacientes con asma o EPOC, y observaron que
las exacerbaciones se presentaban más frecuentemente en el grupo de ACO,
pero estas observaciones no son consistentes en grados leves de la enfermedad y
el mecanismo que explique esta aseveración es desconocido. En nuestro
estudio también observamos una frecuencia significatiÂvamente mayor de
exacerbaciones al comparar los pacientes con ACO vs. el grupo de EPOC.
Existe un interés cada vez mayor en los factores
que afectan la enfermedad, incluidas las condicioÂnes comórbidas.
Existen estudios recientes que han demostrado una mayor frecuencia de
condiciones comórbidas en los pacientes con
ACO, pero los mecanismos no son claros15 . En nuestro grupo de pacientes, no se
observó aumento de comorbilidaÂdes en el grupo de ACO cuando se lo
comparó con el grupo de EPOC puros.
Existen limitaciones en nuestro estudio, alguna de ellas,
corresponden a las del EPOC.AR. En la población evaluada en el grupo de
pacientes ACO, si bien hubo un predominio masculino, la diferenÂcia no fue
significativa. Esto pudo deberse a una mayor permanencia de las mujeres en los
hogares encuestados, especialmente en horarios matutinos, y a una mejor
predisposición de estas a realizar los procedimientos del estudio. Una
limitación específica en este trabajo de prevalencia de la suÂperposición
asma-EPOC en el estudio EPOC.AR7 es que no se
dispuso del recuento de eosinófilos en sangre
periférica, ya que a los pacientes de EPOC.AR no se les realizaron
extracciones de sangre para ningún tipo de estudio.
CONCLUSIONES
La prevalencia de ACO fue del 19,08% en los pacienÂtes
con diagnóstico de EPOC del estudio EPOC.AR. Los pacientes que
cumplían los criterios diagnóstiÂcos de ACO tenían
significativamente menor edad, mayor grado de obstrucción, de uso de
corticoides inhalados, frecuencia de sibilancias y de exacerbaÂciones que requirieron
el uso de antibióticos. DestaÂcamos la importancia de identificar este
fenotipo que tiene diferentes y más serias implicancias clínicas
y pronósticas, con el objetivo de optimizar su
manejo.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de
interés en relación con el contenido de este artículo
BIBLIOGRAFÍA
1. Sin DD. Asthma-COPD overlap
syndrome: what we know and what we donât Tuberc Respir Dis 2017; 80: 11-20.
https://doi.org/10.4046/trd.2017.80.1.11
2. Miravitlles
M. Diagnosis of asthma-COPD overlap: the five commandments. Eur
Respir J 2017; 49: 1700506.
https://doi.org/10.1183/13993003.00506-2017
3. Silva GE, Guerra S, Barbee RA.
Asthma as a risk factor for COPD in a longuitudinal
Study. Chest 2004; 126: 59-65. https://doi.org/10.1378/chest.126.1.59
4. Hosper
JJ, Postma DS, Weiss ST, et al. Histamine airÂway hyperresponsiveness and mortality from Chronic Obstructive
Pulmonary Disease: a cohort study. Lancet 2000;356(9238):
1313-7. https://doi.org/10.1016/S0140-6736(00)02815-4
5. Taskin
DP, Altose MD, Connett JE, et al. Methacholine reactivity
predicts change in lung function over time in smokers with early Chronic
Obstructive Pulmonary Disease: The Lung Health Study Research Group. Am J Respir Crit Care Med 1996;153(6 Pt 1): 1802-11.
https://doi.org/10.1164/ajrccm.153.6.8665038
6. Maselli
DJ, Hardin M, Christenson SA, et al. CliniÂcal Approach to the Therapy of
Asthma-COPD OverÂlap. Chest. 2019; 155: 168-77. https://doi.org/10.1016/j.chest.2018.07.028
7. Echazarreta AL, Arias SJ,
del Olmo R, et al; Grupo de estudio EPOC.AR. Prevalencia de enfermedad pulmonar
obstructiva crónica en 6 aglomerados urbanos de Argentina: el estudio
EPOC.AR. Arch Bronconeumol
2018; 54: 260-9. https://doi.org/10.1016/j.arbres.2017.09.018
8. Jones PW, Harding G, Berry P, Wiklund I, Chen WH, Kline Leidy N. Developmentand
first validation of the COPD assessment test. Eur Respir J. 2009;34:648-54.
https://doi.org/10.1183/09031936.00102509
9. Bestall
JC, Paul EA, Garrod R, Garnham
R, Jones PW, Wedzicha JA. Usefulness
of the Medical Research Council (MRC) dyspnoea scale
as a measure of disability in patients with chronic obstructive pulmonary
disease. Thorax. 1999; 54:
581-6. https://doi.org/10.1136/thx.54.7.581
10. Vogelmeier CF, Criner GJ, Martínez FJ. Global strategy for the diagnosis, management, and prevention of chronic obstructive lung disease 2017 report: GOLD executive summary.
Arch Bronconeumol.
2017; 53: 128-49. https://doi.org/10.1016/j.arbres.2017.02.001
11. Bonten TN, Kasteleyn MJ, de Mutsert R. Chavannes,Annelies M. Slats and Christian Taube Defining asthma-COPD overÂlap syndrome: a population-based study. Eur
Respir J 2017; 49: 1602008.
https://doi.org/10.1183/13993003.02008-2016
12. Sin DD, Miravitlles M, Mannino DM, et al. What is asthma -COPD overlap syndrome? Towards a
consensus definition from a round table discussion. Eur
Respir J 2016; 48: 664-3.
https://doi.org/10.1183/13993003.00436-2016
13. Plaza V, Álvarez F, Calle M, et al. Consenso
sobre el solaÂpamiento de asma y EPOC (ACO) entre la Guía
española de la EPOC (GesEPOC) y la Guía
Española para el Manejo del Asma (GEMA). Arch Bronconeumol. 2017; 53(8): 443-9.
https://doi.org/10.1016/j.arbres.2017.04.002
14. Pérez de Llano L, Cosío BG, Miravitlles M, Plaza V; CHAÂCOS study
group. Accuracy of a New Algorithm to Identify Asthma-COPD Overlap (ACO)
Patients in a Cohort of Patients with Chronic Obstructive Airway Disease. Arch Bronconeumol (Engl Ed). 2018; 54: 198-204.
https://doi.org/10.1016/j.arbr.2017.10.016
15. Maselli
DJ, Hanania N. A Asthma COPD
overlap: Impact of associated comorbidities. PulmonaryPharmacology
& Therapeutics. 2018; 52: 27-31.
https://doi.org/10.1016/j.pupt.2018.08.006
16. Bateman ED, Reddel HK, van Zyl-Smit RN, et
al. The asthma-COPD overlap syndrome: towards a revised taxonomy of chronic
airways diseases? Lancet Respir Med 2015; 3:
719-28. https://doi.org/10.1016/S2213-2600(15)00254-4