Autor Da Lozzo Alejandro Gabriel1 Svetliza Graciela NoemĂ2 Dietrich AgustĂn1 Wainstein Esteban Javier2 Montagne Juan Alejandro1 RaĂces Micaela1 Orazi MarĂa Laura2 Villarroel Mendoza Sonia3 Beveraggi Enrique Jorge1
1 CirugĂa Torácica y Trasplante Pulmonar, Servicio de CirugĂa General, Hospital Italiano de Buenos Aires, Argentina 2 NeumonologĂa, Servicio de ClĂnica MĂ©dica, Hospital Italiano de Buenos Aires, Argentina 3Servicio de Terapia Intensiva, Hospital Italiano de Buenos Aires, Argentina
Correspondencia : Da Lozzo AG. E-mail: alejandro.dalozzo@hospitalitaliano.org.ar
Resumen
Ante
la escasez de donantes pulmonares, el aumento de los pacientes en lista de
espera y el aumento de las muertes en lista de espera existen varias
estrategias que buscan resolver estos problemas. Las estrategias de
promoción son necesarias, continuas y transverÂsales a todo el proceso.
Las de procuración implican mejora continua en la calidad de
atención médica, siendo muy costo-efectivas en nuestro contexto.
Las de distribución ya se emplean y han generado mejoras en el acceso al
trasplante; deben ser constantemente evaluadas. Las de selección
involucran mejoras a expensas de mayores costos a veces con consecuencias
negativas, por lo que deben ser evaluadas caso a caso. El uso de EVLP es
efectivo, aunque pareciera no ser una intervención costo-efectiva en
nuestro medio debiendo emplearse otras estrategias previamente. La
utilización de donantes a corazón parado es efectiva
aunque requiere de una inversión en el sistema logístico que no
parece ser viable por el momento en Argentina.
Palabras
clave: Trasplante
de pulmón; Trasplante de órganos; Selección de donante;
Obtención de tejidos y órganos
Abstract
Giventhe shortage of lung donors and the increase in patients and deaths on the
waiting lists, there are several strategies that could be carried out. Promotion strategies are necessary, continuous and transversal to the
entire process. Strategies that attempt to enhance organ procurement involve continuous improvement in the quality of healthcare, which is highly
profitable in our context. Interventions on grafts distribution
are already in use and have
generated improvements in access to lung transplantation. Laxity in the selection criteria
generates higher costs, sometimes with negative consequences,
so a case-by-case selection
must be applied. Ex vivo lung perfusion is effective, although
it does not
appear to be a cost-effective
intervention in our country,
other strategies must be implemented previously. The use of non-heart-beating lung
donors requires an investment in a logistics system that nowadays does
not seem viable in Argentina.
Key
words: Lung transplantation;
Organ transplantation; Donor selection; Tissue and organ procurement
Introducción
La
cantidad de trasplantes pulmonares ha ido en aumento en el mundo,
observándose en los últimos años una
estabilización. Dicho aumento se ha producido a expensas de los
trasplantes bilaterales que son mayoritarios, siendo los unilaterales
proporcionalmente menores año tras año. Europa ha reducido la
cantidad de trasplantes en forma relativa con aumentos proporcionales de los
trasplantes realizados en América del Norte
pero sobre todo en otras localizaciones1.
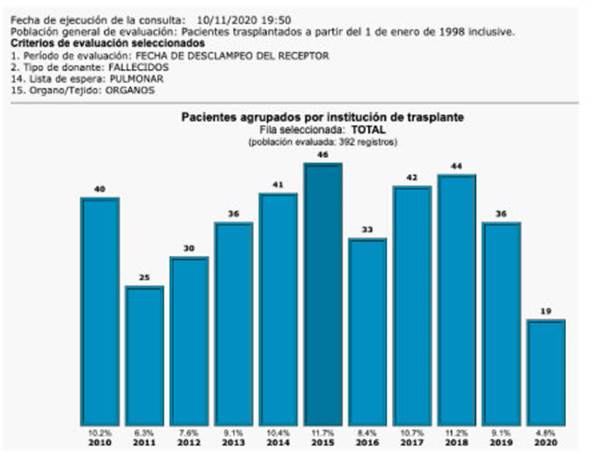
En
Argentina, la cantidad de trasplantes ha variado anualmente en los
últimos 10 años (2010-2019), con un promedio de 37 trasplantes
anuales (Figura 1). El 87% de los mismos son realizados en 2 centros.
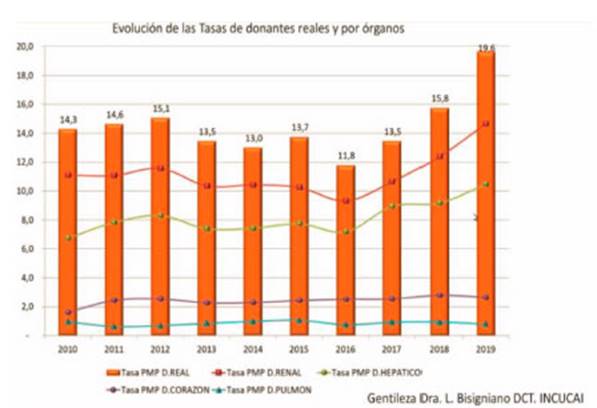
Existe
una menor tasa de utilización de órganos para pulmón y
corazón respecto a hígado y riñón que se ha elevado
en los últimos años. Ésta está cerca del 1 por
millón (específica por órgano pulmón), para una
tasa de 19,6 por millón en 2019 para el resto de los órganos (Figura
2).
En
el resto del mundo la tasa de conversión de donantes en general a
donantes de pulmón es vaÂriable: con máximos cercanos al 60% en
países como Austria y Canadá, y mínimos del 17% en
países como España y Reino Unido2.
En EE.UU la tasa es del 18,5% para pulmón,
mientras que es del 67% para riñón3.
En Argentina, ha aumentado del 6,2% en el período 2011-2015, al 10,6%
entre 2016-20184 coincidiendo este aumento con la
visibilización mediática y judicial que
hubo en el país con la modifiÂcación de la ley de trasplante5.
La
disparidad descrita hace años entre los ingresos en lista de espera y la
cantidad de trasplantes efectuados genera un aumento de muertes en lista de
espera6. En los registros
del Sintra, desde 2010 hasta 11/2020, 407 pacientes de la lista pulmonar y 44 de
la cardio-pulmonar fueron excluidos por faÂllecimiento.
En el mismo período, 281 pacientes fueron incluidos en la lista pulmonar
mientras que 4 en la cardiopulmonar. Solamente 402 pacientes fueron
trasplantados en el mismo período*.
Los
problemas planteados son: la escasez de donantes pulmonares, el aumento de los
pacientes en lista de espera y el aumento de las muertes en lista de espera.
Existen varias estrategias para resolver estos problemas. Trataremos de
dividirlas en grupos temáticos para hacer más fácil su
comprensión.
Estrategias
Existen
estrategias enfocadas en la promoción del trasplante pulmonar.
Básicamente apuntan a conÂcientizar a la población del problema y
tienen como objetivo aumentar la donación global de órganos. Se
requiere de la propaganda estatal a través de programas
específicos. Países como España han logrado tasas de 34
donantes por millón de habitantes (DPMH)7.
En el ámbito local, provincias como Corrientes han logrado tasas
elevadas de 25 DPMH en 20158.
En
2005 en Argentina, a través de la ley 26.066, se estableció la
figura del Donante Presunto9.
Años después, en el 2018 a través de la Ley 27.4475, se consolidó la
confirmación de dicha figura, con un aumento generalizado de las tasas
de donación, probablemente causadas por la visibilidad que tuvo la
problemática de la donación de órganos durante el
tratamiento de dicha ley. En forma indirecta, esto genera un aumento de la
donación global, afectando positivamente a los donantes pulmonares. Este
tipo de estrategias deben ser transversales y continuas en el tiempo para
lograr efectos positivos.
Las
estrategias basadas en la procuración tienen como fundamento la
optimización de los potenÂciales donantes de modo que puedan ser
elegibles por los grupos de trasplante. Todas apelan a una estrategia
ventilatoria protectora y requieren de un adecuado manejo del donante como un
paciente crítico10.
Los aspectos de mejora están dados en el cuidado desde el aspecto
kinésico respiratorio. Su objetivo es la mejoría de las presiones
parciales de oxígeno (PaFiO2)
ofrecidas. El promedio de aceptación para el período 2009-2013
fue de 430 mmHg8.
Es de destacar que a pesar de las múltiples publicaciones
internacionales que ponen el límite de aceptabilidad más bajo11-19, en Argentina los
niveles de exigencia de los grupos son más altos.
La
mejora se ve favorecida por el uso de guías de manejo clínico. El
INCUCAI ha logrado el consenso y difusión de las mismas. No obstante, en
una encuesta anónima de 39-items publicada recientemente20,
dirigida a los profesionales registrados en la Sociedad Argentina de Terapia
Intensiva, se observaron algunos inconvenientes. El porcentaje de respuesta fue
bajo: 736 respuestas (cercano al 10%); 61% médicos; 21% enfermeros y 18%
kinesiólogos. Llama la atención que sólo un 71% de los
respondedores reconocieron a un potencial donante. Pero alarma aún
más que sólo el 18% tenía un protocolo de manÂtenimiento
de los donantes en su centro de atención.
La
experiencia en este aspecto es prometedora. En un trabajo recientemente
publicado de un protocolo realizado en el ámbito de la Ciudad de Buenos
Aires, entre 4/2017 y 3/2018, kinesiólogos respiratorios estuvieron a
cargo de la optimización de los donantes21.
Los potenciales donantes incluidos tenían entre 18 y 65 años, eran donantes ideales de pulmón
o con no más de un criterio marginal; se excluía a pacientes con
alteraciones radiográficas, secreciones purulentas o evidencias de broncoaspiración y antecedentes de paro cardio respiratorio. Se instauró un protocolo de
ventilación mecánica y cuidados respiratorios, con la presencia
de un kinesiólogo respiratorio en el lugar, sistema cerrado de
aspiración, aplicación de fisioterapia respiratoria. El test de
apnea se efectuó con válvula de presión positiva al final
de la espiración (PEEP) para evitar la pérdida de reclutamiento
alveolar y se efectuaron maniobras de reclutamiento. Se logró un aumento
de los pulmones procurados con la totalidad de aceptación de los mismos
con valores estadísticamente significativos.
Las
estrategias basadas en la distribución de los donantes tienen su
origen en el Lung Allocation
Score (LAS) de EE.UU del año 2005 corregida en
2010. Son estrategias enfocadas en la optimización del uso de los
órganos ya procurados. Así se busca lograr cambios en la
distribución de dichos órganos a favor de los pacientes con
más riesgo a morir en lista de espera. Las consecuencias del uso de esta
estrategia fueron la reducción de las muertes en lista de espera y la
realización de más trasplantes22.
En Argentina desde el año 2010, se comenzó a priorizar la
distribución de los donantes en base a la morÂtalidad del receptor,
tanto por la situación clínica (requerimiento de ARM, ECMO o VNI,
o utilización de drogas vasoactivas, entre
otras) como la mortalidad aumentada inherente a su diagnóstico (fibrosis
pulmonar idiopática o quística)23.
La realización de trasplantes uni-pulmonares
también genera un impacto al duplicar el donante a favor de dos
receptores. La detección de anomalías unilaterales puede evitar
perder todo el bloque pulmonar, utilizando pulmones, por ejemplo, con
neumonías contralateraÂles o traumas; aunque esta estrategia implica
mayor riesgo para el receptor y no siempre es posible de utilizar en todas las
patologías (como ser bronquiectasias, fibrosis quística pulmonar,
etc.)24.
El
siguiente escalón de mejora abarca a la selección de los
donantes. Los equipos de trasplante son los que finalmente toman las decisiones
en este punto. Los criterios ideales de selección de los donantes
pulmonares fueron descritos hace más de 20 años25.
Sin embargo, incluso antes de su establecimiento, se comenzaron a describir
experiencias de grupos que comenzaron a utilizar donantes subóptimos
con el objetivo de aumentar la cantidad de donantes26.
En forma paralela, los grupos comenzaron a describir aumentos en las tasa de disfunción primaria de injerto (DPI). En
el caso particular de los trasplantes bilaterales, la consecuencia directa es
el aumento en mortalidad temprana aunque por otro
lado, obÂservaron que la funcionalidad a mediano plazo no se veía
afectada27.
Los
criterios a flexibilizar en la selección pueden ser discordantes en
relación a las consecuencias. En el caso de la edad, algunos trabajos no
muestran diferencias28.
Otros mostraron aumento de las tasas de síndrome de bronquiolitis
obliterante, disminución de la supervivencia global, aumento de la
frecuencia de DPI y hasta consecuencias no tan directas ni correctamente
evaluadas como mayor susceptibilidad a desarrollar cáncer de
pulmón en los receptores, presencia de enfisema subclínico con
reducción en la función pulmonar y menor reserva funcional.
Contrariamente algunos grupos describieron disminución de la frecuencia
de DPI justificándose por una menor inmunogenicidad
de los órganos más añosos29-31.
Cuando
observamos los registros de trasplante pulmonar de la ISHLT, vemos que en los
últimos años los grupos redujeron la edad promedio de sus
donantes con una media de 36 años al 2019.(1)
El análisis multivariable arroja
que por encima de los 55 años existe correlación
estadísticamente significativa de aumento de la mortalidad a 10
años de los receptores. Al discriminar las regiones del trasplante,
observamos que en América del Sur, las edades
de los donantes son más bajas. Mientras que el 58,3% de los donantes en
el mundo pertenecen al grupo etario 18-49 años, ese porcentaje aumenta
al 84,4% para los donantes en la región de Sudamérica es decir
los donantes son más jóvenes en la región32.
La
evaluación de la radiografía de tórax del potencial
donante implica variabilidad interobservador.
Afortunadamente en Argentina cada vez más centros disponen de
radiografía digital, permitiendo el envío de imágenes,
evitando interpretaciones inadecuadas. Puede evaluarse la presencia de edema
bilateral, contusiones, atelectasias y demás alteraciones. Muchos grupos
informaron la presencia de radiografías patológicas en la
selección de sus donantes (23-61%)33.
Finalmente, la radiografía de tórax parece ser más que un
factor de descarte, una variable a corregir.
La
gasometría es quizás la variable más importante en la toma
de decisiones. Asimismo, es la que tiene mayor posibilidad de cambio. Muchos
trabajos referían hace tiempo, que el límite de 300 mmHg parecía ser muy estricto11-19.
A pesar de esto advirtieron precozmente el aumento en la mortalidad temÂprana y
los casos de DPI. Hay que considerar que la gasometría no distingue
lateralidad de la patología. Es por eso que algunos grupos utilizan la
medición intraoperatoria de la misma. Ante una
gasometría no adecuada el equipo de trasplante debe enfocarse en la
optimización del donante, a través de una comunicación
fluida con procurador. Un adecuado control hemodinámico, a través
del uso correcto de drogas y un eficiente manejo hídrico con
medición de diuresis y presión venosa central, sumado a trabajos
kinésicos respiratorios que incluyen la adecuada ventilación y
reclutamiento alveolar, pueden lograr mejoras en los valores de
gasometría. En la práctica, esta variable es la más
exigente dentro de los grupos de trasplante local. En Argentina, los donantes
utilizados en el periodo 2009-13 registraron una PaFiO2
promedio de 430 mmHg3 según datos de INCUCAI. En el mismo
periodo en nuestro cenÂtro, registramos una PaFiO2
de 505 mmHg (valor corregido y
optimizado) para los órganos aceptados e implantados8.
El
tabaquismo es una variable, muchas veces, difícil de obtener en nuestro
medio. El límite establecido es de 20 pack/year.
No pareciera haber diferencias clínicas en cuanto a la evolución
de los pacientes34.
Una
variable a considerar desde el punto de vista local es el tiempo de isquemia,
siendo aceptable con tiempos menores a las 6 horas34.
La falta de logística nacional con ciudades con inadecuada comuÂnicación
terrestre, aeropuertos cerrados en horarios nocturnos y la falta de transporte
aéreo a través de helicóptero (ideal para distancias
menores a los 400 km.), hacen que sea una variable de peso para todos los
grupos de trasplante.
Se
ha tratado de objetivar a través de puntaje la presencia de criterios de
elegibilidad35.
Sin embargo, esto es difícil convirtiéndose estas experiencias en
no reproducibles por distintos grupos. Se requiere de una selección
artesanal en donde el objetivo sea no sumar factores de riesgo, evaluando al
donante en relación al receptor.
Finalizando,
existen estrategias que llamaremos de nuevas tecnologías. Incluyen
múltiples interÂvenciones descritas en la literatura mundial que pueden
tener inconvenientes operativos al momento de extrapolarlas a la
práctica local. Hace más de 15 años se reportó el
primer trasplante pulmonar con un donante inicialmente descartado pero
reacondicionado a través de la perfusión normotérmica
ex-vivo de la solución de Steen (EVLP, ex-vivo
lung perfusion)36. En dicho reporte, se
informa el aumento de una PaFiO2 inicial
de 97 mmHG a una final de 390, haciéndolo apto
para el implante. Años después comienzan a publicarse los
resultados con grupo control de los trasplantes de órganos
acondicionados37.
Este trabajo compara 20 pacientes trasplantados con órganos sometidos a
EVLP contra 116 trasplantes en el grupo control. Los aumentos de las PaFiO2 reportados fueron de 335 mm Hg
a 414 y 443 mm Hg en 1 h y 4 h, respectivamente (P < 0.001). Llamativamente
los investigadores observaron una reducción en la frecuencia de DPI sin
significancia estadística (DPI 72 h. 15% EVLP vs. 30% control (P = 0.11)).
Tampoco encontraron significancias estadísticas en mortalidad a 30
días, complicaciones bronquiales, duración de la
ventilación mecánica y estancia en terapia intensiva (UTI) y
hospitalaria.
Luego
de años de su uso en el mundo, vemos que es una estrategia que logra un
aumento del 20% aproximadamente en la cantidad de trasplantes realizados en el
grupo donde se implementa, requiÂriendo mucha logística y habitualmente
una participación público-privada por los elevados costos que
acarrea (costo incremental de USD 45.000 en EEUU)38.
La costo efectividad de la práctica fue
evaluada en países con sistema público de salud como el Reino
Unido, observando un aumento en años de vida estimado en 0,040, a su vez
que un aumento en los años de vida ajustados por calidad (QALY) de
0,045. No obstante el costo incremental por QALY
ganado fue estimado en ÂŁ90.00039.
Teniendo en cuenta esos costos y el bajo PBI per cápita de nuestro
país, esta tecnología parece superar la capacidad de pago para
nuestro país. En resumen, es una herramienta útil como estrategia
final habiendo realizado previamente intervenciones con mayor
costo-efectividad.
Otra
nueva estrategia es la del uso de donantes en asistolia. Presenta sus inicios
en España en el año 200240,
terminando a finales de 2009 con 29 trasplantes. Los resultados publicados
fueron aceptables en cuanto a supervivencia a mediano y a largo plazo e
incidencia de síndrome de bronquiolitis obliterante (SBO), aunque
reportaron altos índices de falla primaria de órgano y mortalidad
temprana (30d:17%)41.
Un
metaanálisis evalúa 6 trabajos
importantes publicados del tema42.
Allí no se observa aumento significativo de la mortalidad al año,
ni diferencias en cuanto a DPI y rechazo agudo celular. En otros 2 estudios que
utilizaron donantes en asistolia no controlados se observó tasas
relativamente elevadas de DPI, SBO y mortalidad alejada. La conclusión
del metaanálisis es que el uso de donante en
asistolia tendría un potencial de impacto favorable en la reducción
de las listas de espera. El uso de estos donanÂtes es discordante con
frecuencias que varían entre 25-40% para grupos de Londres, Australia y
Países Bajos, respectivamente. No obstante, las cifras para EE.UU no superan el 2%42.
Existe, sin embargo, consenso en que los donantes deben ser controlados. Un
ensayo utilizó pulmones recuperados de donanÂtes no controlados: a todos
se le efectuaba tomografía computada (TC), realizando luego
recuperación a través de EVLP. Luego de 29 meses y 502
potenciales donantes menores a 66 años, ningún pulmón pudo
ser trasplantado debiendo finalizarse el protocolo43.
De modo que si bien la estrategia de donantes en asistolia en interesante hay
que tener cuidado con las extrapolaciones a nuestro medio. Se requiere de un
sólido sistema prehospitalario, con tiempos de
atención menores a 8 minutos, muy difícil de apliÂcar en la
mayoría de nuestras jurisdicciones. Los tiempos de isquemia total deben
ser menores a 300 minutos y los tiempos de isquemia caliente (tiempo entre la
interrupción de la circulación del órgano donado hasta la
perfusión con la solución hipotérmica de
preservación) entre 30 y 120 minutos. Estos valores presentados en la
mayoría de las experiencias son igualmente difíciles de conseguir
en nuestro medio. Secundariamente, el uso de sistemas de circulación
extracorpórea en los centros donde ocurre la procuración es de
difícil implementación en el país. Asimismo, actualmente
EVLP no está disponible para su uso clínico en Argentina.
No
hay dudas de que los resultados muestran que no hay diferencias entre los
grupos; parece facÂtible y seguro; aunque debe realizarse siempre con donantes
en paro cardíaco controlados. En nuestra opinión creemos que
otras intervenciones son más necesarias en nuestro contexto.
Conclusión
Todas
las estrategias son útiles en diferentes niveles. A saber:
Las
estrategias de promoción son necesarias, continuas y transversales a
todo el proceso, no exclusivo al pulmón. Las de procuración son
necesarias, implican una mejora continua en la calidad de atención
médica en general, con una valoración adecuada del RRHH
participante. Impresiona ser muy costo-efectiva en nuestro contexto. Las de distribución
ya se emplean, deben ser constantemente evaluadas para ajustar cambios y han
generado mejoras en el acceso al trasplante. Finalmente, las de
selección involucran mejoras a expensas de mayores costos a veces con
consecuencias negativas, por lo que deben ser evaluadas caso a caso.
Existen
finalmente las estrategias consideradas en esta publicación como de alto
costo, que son la EVLP y el uso de los donantes en asistolia. El uso de EVLP es
efectivo, aunque no impresiona ser una intervención costo-efectiva en
nuestro medio debiendo emplearse otras estrategias previamente. La
utilización de donantes a corazón parado (NHBD) es efectiva aunque requiere de una inversión en un
sistema logístico que no parece ser viable por el momento en Argentina
Conflictos
de interés: Los
autores declaran no tener ningún conflicto de interés en
relación al trabajo publicado.
Bibliografía
1.
Chambers DC, Cherikh WS, Harhay MO, et al. The
International Thoracic Organ
Transplant Registry of the International Society for Heart and Lung
Transplantation: Thirty-sixth
adult lung and heart–lung transplantation
Report—2019; Focus theme: Donor and recipient size match. J Heart Lung Transplant
[Internet]. 2019; 38(10): 1042–55. Disponible en: https://
www.jhltonline.org/article/S1053-2498(19)31619-5/abstract
2.
International donor conversion
rates for lung transplantation need to be standardised. - PubMed - NCBI [Internet]. [citado 21 de noviembre de 2019].
Disponible en:
https://www.ncbi.nlm.nih.gov/pubmed/?term=International+donor+conversion +rates+for+lung+transplantation+need+to+be+standardised
3.
Israni AK, Zaun D, Rosendale JD, et al. OPTN/SRTR 2012 Annual
Data Report: deceased organ donation. Am J Transplant Off J Am Soc Transplant Am Soc Transpl Surg. 2014; 14 Suppl 1: 167-83.
4.
INCUCAI. Sintra INCUCAI. Consulta efectuada 12/11/2019. Período
2016/2018. 121 pacientes trasplantados en lista de pulmón y
cardiopulmonar / 1139 donantes reales = 10,62%. [Internet]. 2019. Disponible
en: https://sintra.incucai.gov.ar/
5.
LEY DE TRASPLANTE DE ÓRGANOS, TEJIDOS Y CÉLULAS. Ley 27447.
[Internet]. InfoLEG - Ministerio de Justicia y Derechos
Humanos - Argentina. [citado 23 de febrero de 2021]. Disponible en:
http://servicios.infoleg.gob.ar/infolegInternet/
anexos/310000-314999/312715/norma.htm
6.
Trulock EP. Lung and Heart-Lung Transplantation: Overview of Results. Semin Respir Crit
Care Med [Internet]. 2001;
22(05): 479–88. Disponible en:
http://www.thieme-connect.de/DOI/DOI?10.1055/s-2001-18420
7.
Miranda B, Vilardell J, Grinyó
JM. Optimizing cadaveric organ procurement: the catalan and Spanish experience. Am J Transplant Off J Am Soc Transplant Am Soc Transpl Surg. 2003; 3(10):
1189-96.
8.
Da Lozzo A, Nicolás M, Dietrich
A, et al. Donante pulmonar con criterio expandido. Rev
Argent Traspl. 2015;VII(2):
64-73.
9.
TRASPLANTE DE ÓRGANOS Y TEJIDOS. Decreto 1949/2006. Modificación
de la reglamentación de la Ley No 24.193 según texto de la Ley No
26.066 aprobada por Decreto No 512 del 10 de abril de 1995. [Internet]. [citado
23 de febrero de 2021]. Disponible en:
http://servicios.infoleg.gob.ar/infolegInternet/anexos/120000-124999/123665/norma.htm
10.
Ruiz VR, Da Lozzo AG, Midley
AD. Optimización del Soporte Ventilatorio del Donante Pulmonar. Revisión
Bibliográfica. Revista Americana de Medicina Respiratoria [Internet].
2017; 17(2): 174–9. Disponible en: http://www.ramr.org/articulos/
volumen_17_numero_2/revision_bibliografica/revision_bibliografica_optimizacion_del_soporte_ventilatorio_del_donante_pulÂmonar.pdf
11.
Botha P, Trivedi D, Weir CJ, et al. Extended donor criteria in lung transplantation: impact on organ allocation.
J Thorac Cardiovasc Surg [Internet]. 2006: 31(5): 1154-60. Disponible en:
http://www.ncbi.nlm.nih.gov/pubmed/16678604
12.
Luckraz H, White P, Sharples
LD, et al. Short- and long-term outcomes
of using pulmonary allograft donors with low Po2. J Heart Lung Transplant
Off Publ Int Soc Heart Transplant.
2005; 24(4): 470-3.
13.
Lardinois D, Banysch M, Korom S, et al. Extended donor lungs: eleven years experience in a consecutive
series. Eur J Cardio- Thorac Surg Off J Eur Assoc Cardio-Thorac
Surg. mayo de 2005; 27(5): 762-7.
14.
Thabut G, Mal H, Cerrina J,
et al. Influence of Donor Characteristics on Outcome After Lung
Transplantation: A Multicenter
Study. J Heart Lung Transplant [Internet]. 2005;
24(9): 1347-53. Disponible en: http://linkinghub.elsevier.com/retrieve/pii/
S1053249804005613
15.
Pilcher DV, Snell GI, Scheinkestel
CD, et al. High donor age, low donor oxygenation,
and high recipient inotrope requirements predict early graft
dysfunction in lung transplant recipients. J Heart Lung Transplant
Off Publ Int Soc Heart Transplant.
2005;24(11): 1814-20.
16.
Gabbay E, Williams TJ, Griffiths
AP, et al. Maximizing the Utilization of Donor Organs Offered for Lung Transplantation.
Am J Respir Crit Care Med [Internet]. 7 de enero
de 1999;160(1): 265-71. Disponible en: http://ajrccm.atsjournals.org/conÂtent/160/1/265
17.
Sundaresan S, Semenkovich
J, Ochoa L, et al. Successful outcome
of lung transplantation is not compromised
by the use of marginal donor lungs. J Thorac Cardiovasc Surg. 1995; 109(6): 1075-9; discussion
1079-80.
18.
Shumway SJ, Hertz MI, Petty
MG, Bolman RM. Liberalization
of donor criteria in lung and heart-lung transplantation. Ann Thorac Surg. 1994; 57(1): 92-5.
19.
Harjula A, Baldwin JC, Starnes
VA, et al. Proper donor selection for heart-lung
transplantation. The
Stanford experience. J Thorac
Cardiovasc Surg. 1987;
94(6): 874-80.
20.
Ruiz VR, Midley AD, Rodríguez PE, et al. Lung Donor Knowledge
and Management Survey among
Health Care Professionals in Argentina. Eur Respir J [Internet]. 2019;
54(suppl 63). Disponible en:
https://erj.ersjournals.com/content/54/suppl_63/ PA1100
21.
Bezzi MG, Brovia CC,
Carballo JM, et al. Impact of implementing
a protocol of respiratory care measures and optimization of mechanical ventilation in potential lung donors. Rev
Bras Ter Intensiva. 2020; 32(4): 571-7.
22.
Egan TM, Edwards LB. Effect
of the lung allocation score on lung transplantation in the United States.
J Heart Lung Transplant [Internet]. 2016; 35(4): 433–9. Disponible en:
https://www.jhltonline.org/article/S1053-2498(16)00057-7/abstract
23.
INCUCAI. Distribución Intratorácica
(Corazón, pulmón, cardiopulmonar) [Internet]. 2017 [citado 9 de
agosto de 2021]. Disponible en:
https://www.argentina.gob.ar/sites/default/files/norm-intrato-reso-incucai_064_17.pdf
24.
Puskas JD, Winton TL,
Miller JD, et al. Unilateral donor lung dysfunction does not preclude
successful contralateral single lung
transplantation. J Thorac Cardiovasc Surg. 1992; 103(5):
1015-7; discussion 1017-8.
25.
Frost AE. Donor criteria and evaluation. Clin Chest Med.
1997; 18(2): 231-7.
26.
Schiavon M, Falcoz P-E, Santelmo N, Massard G. Does the use of extended criteria donors influence early and long-term results of lung transplantation? Interact Cardiovasc Thorac Surg [Internet]. 2012;
14(2): 183–7. Disponible en: http://www. ncbi.nlm.nih.gov/pubmed/22159257
27.
Botha P. Extended donor criteria in lung transplantation. Curr Opin Organ Transplant
[Internet]. 2009; 14(2): 206–10. Disponible en:
http://www.ncbi.nlm.nih.gov/pubmed/19469042
28.
Fischer S, Gohrbandt B, Struckmeier
P, et al. Lung transplantation
with lungs from donors fifty
years of age and older. J Thorac Cardiovasc Surg [Internet]. abril
de 2005; 129(4): 919-25. Disponible en:
http://linkinghub.elsevier.com/retrieve/pii/ S0022522304011766
29.
De Perrot M, Waddell TK, Shargall Y, et al. Impact of donors aged 60 years or more on
outcome after lung transplantation: Results of an 11-year
single-center experience. J Thorac
Cardiovasc Surg [Internet].
2007; 133(2): 525–31. Disponible en:
http://jtcs.ctsnetjournals.org/cgi/content/abstract/133/2/525
30.
Christie JD, Kotloff RM, Pochettino
A, et al. Clinical Risk Factors for Primary
Graft Failure Following Lung TransplantaÂtion*. Chest
[Internet]. 2003; 124(4): 1232-41. Disponible en:
http://chestjournal.chestpubs.org/content/124/4/1232
31.
De Perrot M, Sekine Y,
Fischer S, et al. Interleukin-8 release during ischemia-reperfusion correlates with early graft function
in human lung transplantation.
J Heart Lung Transplant Off Publ Int Soc Heart
Transplant. 2001;20(2): 175-6.
32.
ISHLT. International Thoracic Organ
Transplant (TTX) Registry
[Internet]. 2019 [citado 9 de agosto de 2021]. Disponible en:
https://ishlt.org/research-data/registries/ttx-registry
33.
de Perrot M, Snell GI, Babcock
WD, et al. Strategies to optimize
the use of currently available lung donors. J Heart Lung Transplant Off Publ Int Soc
Heart Transplant
[Internet]. 2004; 23(10): 1127–34. Disponible en: http://www.ncbi.nlm.nih. gov/pubmed/15477105
34.
Orens JB, Boehler A, Perrot M de, et al. A review of lung transplant donor acceptability criteria. J Heart Lung Transplant [Internet]. 2003;
22(11): 1183–200. Disponible en:
http://linkinghub.elsevier.com/retrieve/pii/S1053249803000962
35.
Oto T, Levvey BJ, Whitford H, et al. Feasibility
and Utility of a Lung Donor Score: Correlation With Early Post-Transplant OutÂcomes. Ann Thorac Surg [Internet]. 2007;
83(1): 257. Disponible en:
http://ats.ctsnetjournals.org/cgi/content/abstract/83/1/257
36.
Steen S, Ingemansson R, Eriksson L, et al. First human transplantation of a nonacceptable
donor lung after reconditioning ex vivo. Ann
Thorac Surg [Internet].
2007; 83(6): 2191–4. Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/17532422
37.
Cypel M, Yeung JC, Liu M, et al. Normothermic ex
vivo lung perfusion in clinical lung transplantation.
N Engl J Med. 2011;
364(15): 1431–40.
38.
Divithotawela C, Cypel M, Martinu T, et al. Long-term Outcomes of Lung Transplant With Ex Vivo Lung Perfusion. JAMA Surg. 2019; 154(12): 1143–50.
39.
McMeekin N, Chrysos AE,
Vale L, et al. Incorporating ex-vivo lung perfusion into the UK adult
lung transplant service: an economic
evaluation and decision analytic model. BMC Health Serv Res. 2019; 19(1):
326.
40.
Gámez P, Córdoba M, Ussetti P, et al. Lung transplantation from out-of-hospital non-heart-beating lung
donors. one-year experience and results. J Heart Lung Transplant
Off Publ Int Soc Heart Transplant
[Internet]. 2005; 24(8): 1098–102. Disponible en:
http://www.ncbi.nlm.nih.gov/pubmed/16102446
41.
Gomez-de-Antonio D, Campo-Cañaveral JL, Crowley S, et al. Clinical lung transplantation from uncontrolled non-heart-beating donors
revisited. J Heart Lung Transplant Off Publ Int Soc
Heart Transplant
[Internet]. 2012; 31(4): 349–53. Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/22306439
42.
Krutsinger D, Reed RM, Blevins
A, et al. Lung transplantation
from donation after cardiocirculatory death: a systematic review and meta-analysis. J Heart Lung Transplant
Off Publ Int Soc Heart Transplant.
2015; 34(5): 675–84.
43.
Egan T, Blackwell J, Birchard K, et al. Assessment of Lungs for Transplant
Recovered from Uncontrolled Donation after Circulatory Determination of Death Donors. Ann Am Thorac Soc. 2017;
14(Supplement_3): S251.