Autor Ernst Glendaa,bSabán Melinac, Blanco MagalĂd, Schonfeld Silvanad, Schiavone Miguele, Salvado Alejandrob, Borsini Eduardob,d
aComitĂ© Asesor CientĂfico. Hospital Británico b Servicio de Medicina Respiratoria. Hospital Británico c Servicio de EndocrinologĂa. Hospital Británico d Unidad de sueño y ventilaciĂłn. Hospital Británico e Centro de HipertensiĂłn Arterial. Hospital Británico
Correspondencia : Dra. Glenda Ernst - ComitĂ© asesor cientĂfico - TE. +54 11 4309 6400, Interno 4470 - Perdriel 74 - OF. DOCENCIA - C1280AEB. Buenos Aires
Resumen
Introducción: La presencia de apneas obstructivas del sueño (AOS) constituye una patología prevalente, cuya severidad se estima a partir del índice de apneas e hipopneas (IAH). Se define AOS muy severo (AOSms) por un AHI ≥ 60 eventos/hora cuyas características clínicas podrían ser diferentes. El objetivo de este estudio es describir las características clínicas de pacientes con AOSs y compararlas con formas menos severas de la enfermedad.
Materiales y métodos: Estudio retrospectivo de pacientes derivados a un centro especializado en hipertensión arterial que reunían criterios clínicos para el estudio de AOS. Los pacientes se estudiaron mediante una poligrafía respiratoria, MAPA, cuestionarios y laboratorio. Se utilizaron tests no paramétricos para el análisis de los resultados.
Resultados: Se incluyeron 115 pacientes con AOS, de los cuales 57 presentaron AOS moderado (AOSm), 48 AOSs y 10 AOSms. No se observaron diferencias estadísticamente significativas en la edad, índice de masa corporal (IMC), glucemia, porcentaje de pacientes diabéticos, diámetro de cintura ni de cuello. Se observó un incremento en la proporción de pacientes con hipertensión arterial al aumentar la severidad del AOS que sólo resultó significativo para el valor de la presión arterial diastólica en los pacientes muy severos (AOSms: 94.0 ± 7.7 mmHg vs AOSs: 87.9 ± 8.7 mmHg y AOSm: 84.4 ± 8.2 mmHg; p < 0.05 y p < 0.01 respectivamente).
Conclusiones: En concordancia con trabajos previos, nuestros pacientes con AOSms presentaron mayor grado de hipertensión diastólica con características clínicas similares a las formas menos severas de AOS.
Palabras clave: Apneas Hipopneas Obstructivas de sueño; Índice de Apnea Hipopnea; Hipertensión arterial.
Introducción
El Síndrome de Apneas e Hipopneas Obstructivas del Sueño (SAHOS) constituye una patología cuyo criterio diagnóstico lo constituye la presencia de un índice de apneas-hipopneas (IAH) superior a 5 eventos/hora asociado a excesiva somnolencia diurna o a enfermedad cardíaca o metabólica, su prevalencia en Latinoamérica se estima en alrededor de un 28% en individuos de mediana edad1. En Latinoamérica, en un estudio realizado en el área metropolitana de Sao Paulo (Brasil), Tufik y sus colaboradores, describe una prevalencia en población general cercana al 32.8%2.
La presencia de Apenas obstructivas del sueño (AOS), constituyen un factor de riesgo relacionado con la hipertensión arterial, enfermedad coronaria y accidentes cerebrovasculares3-5. Diferentes mecanismos parecerían estar relacionados con el desarrollo de las complicaciones de esta enfermedad,
incluyendo estrés oxidativo e inflamación6. Estudios de cohortes han demostrado que un incremento de peso aumenta el riesgo de desarrollar AOS7, 8.
La severidad del AOS se determina por la frecuencia en que se producen apneas o hipopneas expresada como eventos por hora (IAH) o como Respiratory Event Related Arousal (RERAS). Estos valores permiten agrupar la severidad como AOS-leve (5 > IAH < 15 eventos/hora), AOS moderado (15 > IAH < 30) o AOS severo (IAH > 30)9, 10. Sin embargo; la categorización de AOS Muy Severo (AOSms) es relativamente inusual y aún no se conocen con detalle todas sus características. Publicaciones recientes han comenzado a describir las particularidades clínicas de esta población. Jurcevic y sus colaboradores, han sugerido que los pacientes con un IAH ≥ 60 eventos/hora presentarían un significativo incremento de la mortalidad11. Por otra parte, un estudio de casos y controles en pacientes con IAH ≥ de 100 eventos/hora; indicaría que este incremento en la severidad a valores superiores a 100 eventos/hora, estaría relacionado con el aumento en la circunferencia del cuello y la presencia de hipertensión arterial12.
El objetivo de este trabajo es describir las características clínicas y bioquímicas de los pacientes con AOS muy severo, en pacientes referidos al Centro de Hipertensión Arterial del Hospital Británico de Buenos Aires que hayan sido seleccionados para un estudio ambulatorio de sueño por presentar sospecha clínica AOS.
Materiales y métodos
Diseño
Estudio retrospectivo para describir pacientes ≥ 18 años derivados para evaluación de factores de riesgo cardiovasculares en un centro especializado en Hipertensión Arterial, entre septiembre de 2015 a marzo 2017. Se incluyeron aquellos pacientes con riesgo incrementado para el desarrollo de AOS. Este estudio fue aprobado por el Comité de Revisión Institucional del Hospital Británico en acuerdo con las normas de Helsinki. Todos los pacientes firmaron un consentimiento informado.
Población
Se incluyeron pacientes consecutivos entre 18 y 80 años, evaluados para diagnóstico o seguimiento de hipertensión arterial que presentaron 5 o más puntos en el cuestionario STOP-BANG11; un puntaje en la escala de somnolencia de Epworth (ESS) mayor a 10 ó alto riesgo según la escala de Berlín. Se realizó una evaluación metabólica y un estudio ambulatorio de sueño (poligrafía respiratoria auto-administrada) incluyendo en el análisis únicamente aquellos con un IAH ≥ 15 en la poligrafía respiratoria (PR). Se excluyeron aquellos pacientes con insuficiencia cardíaca sintomática, enfermedades neuromusculares, diagnóstico conocido de EPOC, uso de CPAP o alguna modalidad de soporte ventilatorio u oxígeno suplementario.
Parámetros clínicos registrados
Presión Arterial (PA): La medición de la PA fue registrada con un tensiómetro automático (OMRON 7220). Previo reposo de 5 minutos se procedió a realizar tres registros separados por 2 minutos y se consignó el promedio de las mediciones. Se realizó un monitoreo ambulatorio de la presión arterial (MAPA) de 24 horas con equipo Spacelabs Ultralite (modelo 90217, SpaceLabs, Redmond, WA). Las tomas de PA fueron programadas cada 15 minutos durante el día (8:00 am a 11:00 pm) y cada 30 minutos durante la noche (11:00 pm a 8:00 am). Se definió como normotensión a cifras de PA diurna y nocturna menores o igual a 135/85 mmHg y 120/70 mmHg respectivamente. El diagnóstico de HTA se confirmó luego del análisis del monitoreo ambulatorio de presion arterial (MAPA) discriminando la hipertensión arterial como; sistólica, diastólica o sisto-diastolica. El registro de PR y el MAPA se realizaron en noches sucesivas.
Parámetros bioquímicos: Se obtuvieron muestras de sangre venosa en ayunas por la mañana previa a la PR para determinación de glucosa, triglicéridos (TGL), colesterol total y colesterol HDL se determinaron por métodos enzimáticos estándar en un analizador Abbott ci8200 (Abbott, Abbott Park, Illinois, EE. UU).
Cuestionarios: Todos los participantes completaron sistemáticamente los cuestionarios validados en idioma español; Cuestionario de Berlín13, Escala de somnolencia subjetiva de Epworth (ESS)14 y Cuestionario STOP-BANG (SBQ)15-17.
Poligrafía Respiratoria domiciliaria auto-administrada: Se utilizaron polígrafos Apnea Link Air™ (ResMed. Australia) que cuentan con cinco canales y tres señales básicas, oximetría de pulso, flujo por cánula nasal y esfuerzo torácico, (dispositivos de nivel III de la American Academy of Sleep Medicine)18. Se consideraron válidos aquellos registros con un tiempo total de registro en el análisis manual > 4 horas. Se definió apnea como reducción del flujo aéreo de > 80% del basal ≥ 10 segundos (s) y las hipopneas se consideraron como una reducción del flujo aéreo de 50% ≥ 10 s asociadas a desaturaciones ≥ 3%19.
El IAH se definió como el número de eventos respiratorios (apneas o hipopneas) por hora de registro. El índice de desaturaciones (IDO) se calculó de igual manera sobre el tiempo total de registro y el T90 se consideró en porcentaje del TTR válido. El IDO se definió según el criterio de desaturación de 3% respecto del valor basal inmediatamente precedente y se definieron las mismas categorías de severidad que para el IAH (normales (IAH < 5/h), leves (IAH entre 6 y 14.9 eventos por hora), moderados (IAH entre 15 y 29.9/hora), severos (IAH ≥ 30 hora) y muy severos (IAH ≥ 60/hora).
Análisis Estadístico
Se agruparon los pacientes por categorías de severidad según el valor del IAH, de este modo se incluyeron pacientes con AOS muy severos (AOSms) cuando IAH ≥ 60 ev/hora; severos (AOSs) con IAH entre 30 y 59.9 y moderados (AOSm) cuando el IAH se encontró entre 15 y 29.9. Los resultados se expresaron como media y desvío estándar o mediana e intervalos intercuartilos dependiendo de la distribución de los datos. Los grupos se compararon utilizando test de ANOVA y como test de comparaciones múltiples Kruskal Wallis para las variables continuas y test de Fisher para las variables cualitativas. Se consideró significativo p < 0.05.
Resultados
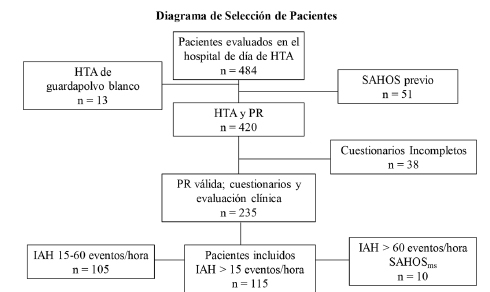
Incluimos en el estudio a 115 pacientes con AOS, de los cuales 57 presentaron AOS moderado, 48 AOS severo y 10 AOS muy severo (Figura 1).
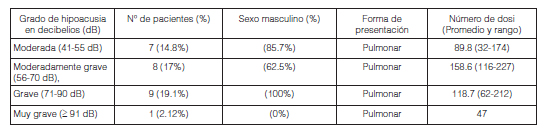
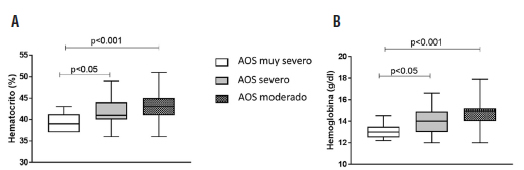
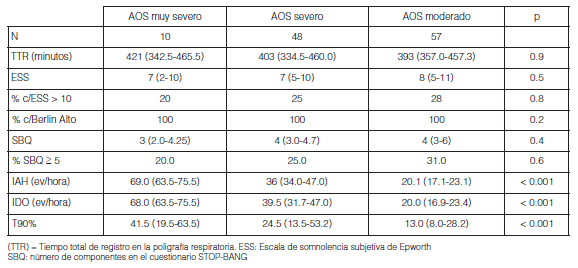
Tal como puede observarse en la Tabla 1, la mayoría de los pacientes eran hombres (86.9%) de mediana edad en los cuales fue confirmado el diagnóstico de hipertensión. No se observaron diferencias en el índice de masa corporal (IMC), perímetro de cintura, ni circunferencia de cuello entre los 3 grupos analizados. Más aún; no se observaron entre diferencias parámetros tales como glucemia, HDL, TGL, ni en el porcentaje de pacientes con diabetes. Sin embargo se observó una disminución estadísticamente significativa en el porcentaje de hematocrito y hemoglobina de los pacientes con AOS muy severo respecto de los AOS severos y AOS moderado (% de hematocrito: 39.3 ± 2.1 vs 41.9 ± 3.1 y 43.1 ± 3.1; p < 0.05 y p < 0.01 respectivamente y hemoglobina (g/dl): 13.1 ± 0.7 vs 14.2 ± 1.2 y 14.6 ± 1.1; p < 0.05 y p < 0.01 respectivamente) Figura 2 A y B.
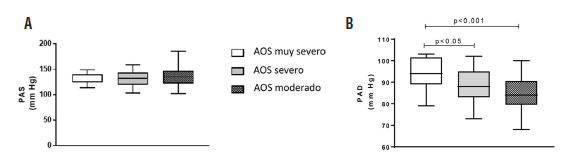
La Tabla 1 muestra un proporcional incremento en la cantidad de pacientes con HTA en relación a la severidad por IAH. Sin embargo; los resultados del MAPA demostraron un incremento estadísticamente significativo sólo en la PAD correspondiente a los pacientes con AOS muy severo en comparación con los grupos de AOS severo y moderado (94 ± 7.7 vs 87.9 ± 8.7 y 84.4 ± 8.2; p < 0.05 y p < 0.01 respectivamente) Figura 3 A y B.
En el grupo AOSms a pesar de la severidad por IAH (mediana de 69.0, con un IC 25%-75%: 63.5-75.5 eventos/hora), no se observaron diferencias significativas en la escala de somnolencia (ESS) ni en el cuestionario SBQ Tabla 2.)
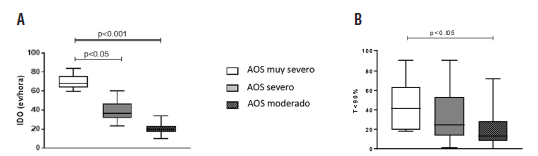
Los pacientes con AOSms mostraron un significativo incremento del índice de desaturación (IDO) respecto de los grupos con AOS severo y moderados (69.5 ± 7.8 vs 39.1 ± 9.8 y 20.4 ± 5.2; p < 0.05 y p < 0.001) respectivamente. (Figura 4A). Más aún; el porcentaje de tiempo con una saturación menor a 90% también mostró diferencia significativa entre los pacientes con AOS muy severo y moderado (44.3 ± 24.2 vs 21.3 ± 20.7; p < 0.01) (Figura 4B).
Discusión
Esta muestra estuvo constituida por 115 pacientes con AOS, IAH ≥15 y riesgo cardiovascular, entre los cuales el 10% cumplieron con los criterios establecidos por nosotros para categorizarles como AOSms.
La severidad del AOS se evalúa convencionalmente de acuerdo al IAH. Sin embargo, este indicador usado aisladamente parecería reflejar de manera insuficiente la severidad del AOS por lo cual es recomendable complementarlos con la valoración de factores modificadores de la severidad (grado de hipoxemia, fragmentación del sueño, duración y distribución de los eventos, síntomas, edad, etc.)20.
Recientemente ha sido descripta una asociación entre la severidad AOS y el incremento de especies reactivas de oxígeno21. Aunque no ha sido el objetivo de este estudio; dichos hallazgos podrían relacionarse con el incremento de la hipoxemia de los pacientes de acuerdo al aumento de la severidad de los pacientes. Los resultados de este trabajo han mostrado un incremento significativo donde se evidencia un incremento del IDO y del T < 90.
Trabajos previos han demostrado que los pacientes con AOS muy severo presentan mayor grado de hipoxemia nocturna expresado por aumento en los indicadores como el tiempo con una saturación < 90% (T < 90%) y más comorbilidades tales como la hipertensión arterial11, 12. En concordancia con dichos autores, nuestros hallazgos mostraron un significativo incremento del T < 90%, del IDO y de la proporción de pacientes con PAD > 85 en el grupo de pacientes con AOS muy severo en comparación con pacientes con AOS severo y moderado.
Preis y cols., en un estudio derivado de la base de datos del estudio Framinghan, halló relación entre parámetros antropométricos y la probabilidad de desarrollar eventos cardiovasculares vinculados al AOS. Sin embargo, en pacientes hipertensos nosotros no hallamos diferencias en variables como; la circunferencia de la cintura y el cuello, el grado de obesidad, evaluado a partir del IMC, ni en los niveles circulantes de TGL, HDL22.
Una comorbilidad frecuentemente asociada al AOS es la diabetes23. Se ha postulado que una desregulación del metabolismo de los glucanos en pacientes con AOS, aunque no es claro aún; Si esta si esta alteración guarda relación con la severidad. Nuestros hallazgos no expusieron diferencias en la glucemia en los diferentes grupos de severidad.
También ha sido demostrado por Nieto y sus colaboradores que la incidencia de la hipertensión arterial en los pacientes con AOS es mayor al incrementarse la severidad24. En concordancia con dicho reporte, nuestros hallazgos mostraron un significativo incremento de los pacientes con PAD > 85 mmHg; sin embargo no se logró poder estadístico para el porcentaje de pacientes con diagnóstico de HTA.
Nguyen y sus colaboradores evaluaron en una cohorte de pacientes los valores del hematocrito en grupos de pacientes con AOS de diferente severidad; sin embargo, no observaron diferencias estadísticamente significativas25. Llamativamente, en este estudio se encontraron diferencias significativas en el hematocrito y la hemoglobina con una relación inversa, aunque dentro del rango de normalidad y con escasa relevancia clínica.
De acuerdo a los hallazgos en nuestra muestra, los pacientes con AOSms, categorizados por un IAH ≥ 60, mostraron mayor deterioro en los indicadores de oxigenación medidos durante el sueño comparados con pacientes con AOSm y s de acuerdo a los criterios convencionales. En esta muestra limitada no identificamos diferencias significativas en los demás parámetros evaluados, como peso, circunferencia del cuello, indicadores metabólicos, pero si mayor incidencia de HTA diastólica. Rey de Castro y sus col. han descripto la necesidad de identificar variables de pronóstico para las formas muy severas de apneas del sueño12.
Llamativamente, no hemos encontrado en nuestra serie, diferencias en la presentación clínica, grado de somnolencia subjetiva ni valor en los cuestionarios de predicción entre AOSms y las formas moderadas a severas, planteando la dificultad en su identificación antes del estudio de sueño.
Limitaciones
La principal limitación del estudio estuvo relacionada con el acotado número de casos identificados como AOSms y por esta razón, los intervalos de confianza fueron amplios. Sin embargo, la población incluida representa la vida real y el conjunto de pacientes que habitualmente son derivados a centros cardiológicos especializados. Las características clínicas evaluadas en los pacientes han sido tan solo aquellas que representan la sistemática de trabajo en nuestra Unidad de Hipertensión Arterial. Nos proponemos a futuro el estudio de variables inflamatorias para comprender los mecanismos fisiológicos relacionados con este conjunto extremo de pacientes con apneas del sueño.
Otra limitación son las variables de confusión relacionadas con el AOS y el hecho de que fueron evaluados por métodos simplificados. La capacidad diagnóstica de los polígrafos respiratorios que utilizamos es limitada, aunque todos ellos incluyeron al menos las 3 señales básicas en las que se basaron la lectura manual y la interpretación final del estudio de sueño. La PR domiciliaria podría establecer diferencias entre nuestros resultados y los de otros estudios que utilizaron PSG en el laboratorio del sueño11, 12. En comparación con la PSG convencional, la PR tiene una tasa de subestimación del 10-15% para el IAH, una limitación inherente a la ausencia de señales neurofisiológicas18, 19. Los índices utilizados (IAH e IDO) difieren de los de PSG ya que son el resultado del cociente entre los eventos y el tiempo total de grabación, aunque representan un estándar de diagnóstico en nuestro medio10.
Finalmente, nuestro análisis incluyó una muestra escasa de pacientes sin obesidad lo que limita nuestra interpretación. Además, sólo consideramos una evaluación en el tiempo sin seguimiento. Estudios longitudinales serán necesarios para conocer el valor clínico y pronóstico de estas formas extremas de la enfermedad.
Conclusión
En nuestra muestra muy limitada de pacientes con AOSms, identificamos una incidencia mayor de HTA diastólica y mayor deterioro en las variables de oximetría, aunque sin diferencias en los parámetros clínicos y demás datos metabólicos estudiados.
1. Young T, Palta M, Dempsey J, Skatrud J, Weber S, Badr S. The occurrence of sleep-disordered breathing among middleaged adults. N Engl J Med 1993; 328: 1230-5.
2. Tufik S, Santos-Silva R, Taddei JA, Bittencourt LR. Obstructive sleep apnea syndrome in the Sao Paulo Epidemiologic Sleep Study. Sleep Med 2010;11(5): 441-6.
3. Peppard PE, Young T, Palta M, Skatrud J. Prospective study of the association between sleep-disordered breathing and hypertension. N Engl J Med 2000; 342: 137884.
4. Redline S, Yenokyan G, Gottlieb DJ, et al. Obstructive sleep apnea-hypopnea and incident stroke: the Sleep Heart Health Study. Am J Respir Crit Care Med 2010; 182: 269-77.
5. Peker Y, Hedner J, Norum J, Kraiczi H, Carlson J. Increased incidence of cardiovascular disease in middle-aged men with obstructive sleep apnea: a 7-year followup. Am J Respir Crit Care Med 2002; 166: 159-65.
6. Adipose tissue inflammation by intermittent hypoxia: mechanistic link between obstructive sleep apnoea and metabolic dysfunction. Ryan S. J Physiol. 2017 15; 595 (8): 2423-30.
7. Peppard PE, Young T, Palta M, et al. Longitudinal study of moderate weight change and sleepdisordered breathing. JAMA. 2000; 284: 3015-21.
8. Young T, Peppard PE, Gottlieb DJ. Epidemiology of obstructive sleep apnea. Am J Respir Crit Care Med. 2002; 165: 1217-39.
9. Epstein LJ, Kristo D, Strollo PJ et al. Adult Obstructive Sleep Apnea Task Force of the American Academy of Sleep Medicine. Clinical guideline for the evaluation, management and long-term care of obstructive sleep apnea in adults. Journal of clinical sleep medicine: JCSM: official publication of the American Academy of Sleep Medicine 2009; 5(3):263-76.
10. Nogueira F, Nigro C, Cambursano H, Borsini E, Silio J, Avila J. Practical guidelines for the diagnosis and treatment of obstructive sleep apnea syndrome. [Article in Spanish]. Medicina (B Aires) 2013; 73(4): 349-62.
11. Jurcevic D, Shaman Z, Krishnan V. A new category: very severe obstructive sleep apnea has worse outcomes on morbidity and mortality. Chest J 2012; 142: 1075A-A[4_MeetingAbstracts].
12. Rey de Castro J, Huamaní C, Escobar-Córdoba F, Liendo C. Clinical factors associated with extreme sleep apnoea [AHI>100 events per hour] in Peruvian patients: A case-control study-A preliminary report. Sleep Sci. 2015; 8(1): 31-5.
13. Netzer NC, Stoohs RA, Netzer CM, Clark K, Strohl KP. Using the Berlin Questionnaire to identify patients at risk for the sleep apnea syndrome. Ann Intern Med. 1999 Oct 5; 131: 485-91.
14. Chiner E, Arriero JM, Signes-Costa J, Marco J, Fuentes I. Validation of the Spanish version of the Epworth Sleepiness Scale in patients with a sleep apnea sindrome. Arch Bronconeumol. 1999; 35: 422-7.
15. Chung F, Yegneswaran B, Liao P, Chung SA, Vairavanathan S, Islam S, Khajehdehi A, Shapiro CM. STOP questionnaire: a tool to screen patients for obstructive sleep apnea. Anesthesiology. 2008 May; 108: 812-21.
16. Borsini E, Ernst G, Salvado A, Bosio M, Chertcoff J, Nogueira F, Nigro C.Utility of the STOP-BANG components to identify sleep apnea using home respiratory polygraphy. Sleep Breath. 2015 Dec; 19: 1327-33.
17. Borsini E, Blanco M, Bosio M, Schrappe M, Ernst G, Nosetto D, et al. Prevalence of sleep apnea and cardiovascular risk factors in patients with hypertension in a day hospital model. Clin Exp Hypertens. 2018; 40(3): 231-37.
18. Clinical Guidelines for the Use of Unattended Portable Monitors in the Diagnosis of Obstructive Sleep Apnea in Adult Patients. Portable Monitoring Task Force of the American Academy of Sleep Medicine Journal of Clinical Sleep Medicine 2007; 3: 737-47.
19. Berry, R. B., Budhiraja, R, Gottlieb, D.J.et al. Rules for scoring respiratory events in sleep: update of the 2007 AASM Manual for the Scoring of Sleep and Associated Events. Deliberations of the Sleep Apnea Definitions Task Force of the American Academy of Sleep Medicine. J Clin Sleep Med. 2012; 8(5): 597-619.
20. Borsini E, Nogueira F, Nigro C. Apnea-hypopnea index in sleep studies and the risk of over-simplification. Sleep Sci.2018; 11(1): 45-48.
21. Tóthová L', Celec P, Mucska I, Hodosy J. Short-term effects of continuous positive airway pressure on oxidative stress in severe sleep apnea. Sleep Breath 2019, in prees (doi: 10.1007/s11325-018-01777-0).
22. Preis SR, Massaro JM, Hoffmann U, D’Agostino Sr RB, Levy D, Robins SJ, et al. Neck circumference as a novel measure of cardiometabolic risk: the Framingham Heart study. J Clin Endocrinol Metab 2010; 95(8): 3701-10.
23. Reutrakul S, Mokhlesi B. Obstructive Sleep Apnea and Diabetes: A State of the Art Review. Chest. 2017; 152: 1070-86.
24. Nieto FJ, Young F, Lind BK et al. Association of Sleep-Disordered Breathing, Sleep Apnea, and Hypertension in a Large Community-Based Study. JAMA. 2000; 283(14): 1829-36.
25. Nguyen CD, Holty JC. Does untreated obstructive sleep apnea cause secondary erythrocytosis? Respir Med 2017; 130: 27-34.