Autor : Blanco MagalĂ1,2, Ernst Glenda1, Di Tullio Fernando1, Campos JerĂłnimo1, Decima Tamara1, Bosio MartĂn1, Meraldi Ana1, Chertcoff Julio1, Salvado Alejandro1 y Borsini Eduardo1,2
1Centro de Medicina Respiratoria. Hospital Británico de la Ciudad Autónoma de Buenos Aires. Argentina; 2 Unidad de Sueño y Ventilación. Hospital Británico de la Ciudad Autónoma de Buenos Aires. Argentina
Correspondencia : MagalĂ Blanco, e mail: blanco.magali@hotmail.com
Resumen
Introducción: La ventilación mecánica domiciliaria representa un estándar de cuidados en la insuficiencia de la bomba ventilatoria. El modelo de atención podría ser determinante de deficiencias en el control de calidad de este tratamiento.
Material y métodos: Con la finalidad de monitorear el cumplimiento de la ventilación mecánica domiciliaria y optimizar su eficacia, propusimos un programa mediante hospital de día conducido por médicos neumonólogos y kinesiólogos respiratorios. Se diseñó un estudio descriptivo sobre una base de datos de recolección sistemática. Participaron pacientes consecutivos con ventilación no invasiva o asistencia respiratoria mecánica invasiva asistidos en el Servicio de Neumonología entre julio de 2014 y diciembre de 2016.
Resultados: Participaron 94 pacientes; 52 hombres (55%), edad 64.4 ± 15.9 años; el 50% presentaban obesidad o sobrepeso (índice de masa corporal 28.6 ± 8.46 kg/m2). Recibían ventilación mecánica domiciliaria 80 pacientes (84%); no invasiva en 77 casos e invasiva en tres (4%). Se admitieron para evaluar la indicación de ventilación mecánica domiciliaria 14 pacientes (14.8%). Los modos de ventilación no invasiva utilizados fueron; bilevel S/T: 59 (62.7%), presión de soporte con volumen promedio asegurado (AVAPS average volume-assured pressure support ventilation); 4 (4.2%), presión positiva continua en la vía aérea (CPAP (continuous positive airway pressure): 6 (6.4%), servo-ventilación: 1 (1%). Tres pacientes recibían ventilación volumétrica.
La media de cumplimiento fue de 8.1 horas. Cuatro pacientes no utilizaban el dispositivo. Permanecieron hipercápnicos el 42.5%. Se cambió la programación en 37 pacientes (46.2%), modo ventilatorio en 2 (2.5%) y se suspendió la ventilación en dos (2.5%). En pacientes individuales los ajustes fueron clínicamente significativos.
Conclusión: El programa permitió mejorar el entrenamiento e identificar un alto porcentaje de ventilación mecánica domiciliaria ineficaz, permitiendo ajustes en la modalidad de tratamiento.
Palabras clave: Ventilación domiciliaria; Ventilación no invasiva; Monitoreo.
Abstract
Monitoring of chronic home ventilation. Experience based on a day hospital model
Introduction: Home mechanical ventilation (HMV) represents a standard of care for chronic ventilatory pump failure. The care model could be determinant in deficiencies in the control of quality of HMV.
Material and methods: In order to monitoring compliance during home mechanical ventilation and optimize its effectiveness, we proposed a program through a day hospital conducted by pulmonology doctors and respiratory physiotherapist. A descriptive study was designed on a systematic collection database. Participants were consecutive patients with NIV or mechanical invasive ventilation (MIV) assisted in the Pulmonology Service between July 2014 and December 2016.
Results: During 30 months we included 94 patients; 52 men (55%), age 64.4 ± 15.9 years and BMI of 28.6 ± 8.46 kg / m2. Fifty percent were obese or overweight. 80 were found with HMV (84%) noninvasive (NIV) in 77 cases and invasive in three (4%). 15 patients (16%) were admitted to evaluate indication of VMD. The NIV modes used were; Bilevel S / T: 59 (62.7%), AVAPS; 4 (4.2%), CPAP: 6 (6.4%), servo-ventilation: 1 (1%). Three patients received volumetric ventilation. The mean compliance objectively measured was 8.1 hours. Four patients did not use the device. Remained with hypercapnia 42.5%. The setting was changed in 37 patients (46.2%), ventilatory mode in 2 (2.5%) and HMV was suspended in two (2.5%). In individual patients adjustments were clinically significant.
Conclusion: This program allowed to improve the training and to identify a high percentage of patients with ineffective HMV, allowing adjustments in the modality of treatment.
Key words: Home mechanical ventilation; Non-invasive ventilation; Monitoring.
Introducción
La ventilación mecánica domiciliaria (VMD) consiste en el uso intermitente o continuo de un sistema de ventilación administrado a través de una interfase: nasal, facial o pieza bucal en la ventilación no invasiva, o traqueostomía para la ventilación invasiva1. Esta modalidad de tratamiento se aplica en la insuficiencia respiratoria crónica con el objetivo de disminuir la disnea, aliviar el trabajo de los músculos respiratorios y corregir la hipoxemia e hipercapnia y/o acidosis respiratoria consecuente, mejorando la ventilación alveolar y el intercambio gaseoso1-3.
La ventilación domiciliaria a largo plazo representa un estándar de cuidados para pacientes con insuficiencia crónica de la bomba ventilatoria2, 3, ya que mejora la sobrevida de aquellos con enfermedades neuromusculares y de la caja torácica4-8 además de mejorar la calidad de sueño y la calidad de vida en el síndrome de hipoventilación-obesidad8-10. En la enfermedad pulmonar obstructiva crónica (EPOC) con hipercapnia en fase estable, su papel es aún controvertido, aunque recientes aportes a la comunidad científica parecen mostrar mejoría de la supervivencia11 y disminución de las agudizaciones y re-admisión hospitalaria12, 13.
En Europa esta modalidad de tratamiento ha tenido un gran desarrollo y si bien existe gran variación en la utilización entre diferentes países la media supera los 10 tratamientos cada 100.000 habitantes14-18.
Algunos estudios han puesto en evidencia las carencias en el control de calidad de los sistemas de ventilación no invasiva en el domicilio, fundamentalmente cuando no hay equipos multidisciplinarios y dicho monitoreo se halla casi de forma exclusiva en manos de personal técnico de las empresas suministradoras de servicios, poniendo de manifiesto la escasa participación de los especialistas prescriptores y de los centros de salud en la supervisión de calidad de la terapia y del equipamiento18, 19.
No obstante, la VMD se ha extendido e incluso este crecimiento se puede apreciar en nuestro medio. Información de un centro de la Ciudad de Buenos Aires dan cuenta del perfil de indicaciones y características de los pacientes20 aunque la ausencia de un registro en Argentina nos impide conocer datos actualizados. Más aún, tampoco se dispone de información objetiva en relación al cumplimiento o monitoreo de eficacia de la VMD. Con frecuencia, el modelo de atención domiciliaria, podría ser determinante para que los pacientes pierdan contacto con los especialistas de referencia luego del alta hospitalaria20, 21.
Por otra parte, las dificultades de movilidad, necesidad de traslados complejos, barreras arquitectónicas que limitan el acceso de los pacientes, la necesidad de estudios complementarios (laboratorio analítico, examen de gases en sangre, software específicos de los ventiladores, disponibilidad de exámenes funcionales respiratorios, etc.) obstaculizan la actuación en la consulta externa de la especialidad y con frecuencia obligan la re-internación de los pacientes con ventilación no invasiva (VNI), al igual que aquellos que requieren asistencia respiratoria mecánica invasiva (ARMI).
Con la finalidad de realizar un monitoreo del cumplimiento de la terapia ventilatoria y optimizar su eficacia, nos propusimos realizar un programa para mejorar el vínculo entre los pacientes con ventilación domiciliaria crónica y el hospital de referencia mediante un sistema de hospital de día (Unidad de Observación Respiratoria: UDOR).
Los objetivos de nuestro estudio fueron describir las características de los pacientes que reciben alguna modalidad de ventilación domiciliaria crónica en un hospital de comunidad; conocer datos objetivos de eficacia de la ventilación y evaluar la factibilidad de los procedimientos de un modelo de hospital de día en pacientes con VMD.
Materiales y Métodos
Se diseñó un estudio descriptivo sobre una base de datos de recolección sistemática en un único centro universitario. Participaron pacientes consecutivos con VNI o ARMI asistidos en el Servicio de Neumonología entre julio de 2014 y diciembre de 2016. Los pacientes a quienes se les indicó alguna modalidad ventilatoria durante la internación fueron citados a integrar la UDOR cuatro semanas después del egreso hospitalario.
Se obtuvo información de la historia clínica surgida durante la permanencia en el programa UDOR del Hospital Británico de la Ciudad Autónoma de Buenos Aires (Argentina), de todos aquellos pacientes con indicación de alguna modalidad de VMD. Se registraron datos demográficos, antropométricos, antecedentes clínicos, diagnósticos, motivo de la indicación de VNI. Se realizaron las siguientes mediciones fisiológicas: gases en sangre arterial (matinal, en sedestación y vigilia y sin el uso del equipo de ventilación ni O2 suplementario) y espirometría computada con curva flujo volumen (MedGraphics. USA). Según el cociente VEF1/CVF < al límite inferior de la normalidad (LIN) se clasificaron los patrones de las espirometrías en obstructivo; (cociente < LIN y VEF1 < 80% del predictivo) o no obstructivo (cociente > LIN).
El modo y parámetros del ventilador se registraron al ingreso y egreso de la unidad y se descargaron los datos de software interno de los ventiladores usando Encore II y Direct View (Philips-Respironics. USA) o ResScan (ResMed. Australia). Cuando fue necesario se ajustaron los parámetros de ventilación y oxigenoterapia. Se controlaron material y educación del paciente y su familia.
El programa UDOR se desarrolló en el ámbito hospitalario durante un módulo de 4-6 horas por la mañana, en el laboratorio de sueño (área donde se realizan los registros de polisomnografía nocturnos).
Análisis estadístico. Los resultados se presentaron como porcentajes en las variables categóricas o media y desvío estándar en las variables numéricas. Para comparar las diferencias entre dos grupos se utilizó el test de Mann Withney o χ2 para variables cuantitativas y cualitativas respectivamente y cuando se compararon los resultados de tres o más grupos se utilizó el test no paramétrico de Kruskall Wallis junto con el test de comparaciones múltiples de Dunn´s. El análisis de los datos se realizó utilizando el software Prism 5 software (Graph Pad, La Jolla, CA).
Resultados
Durante 30 meses, se incluyeron en el programa UDOR 94 pacientes; 52 hombres (55%), con una media de edad de 64.4 ± 15.9 (percentilo 25-75%: 50-74) años y un índice de masa corporal (IMC) de 28.6 ± 8.46 kg/m2. La Tabla 1 resume las características clínico-demográficas de la población.
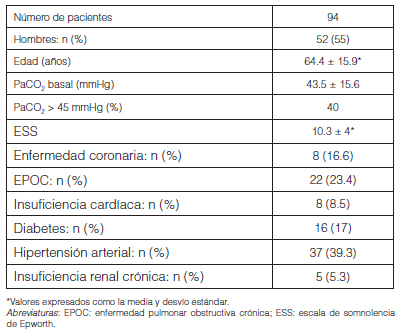
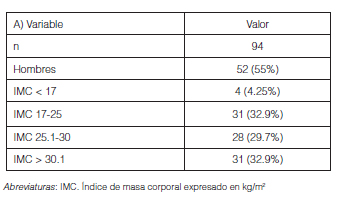
Al momento del estudio 55 pacientes habían sido fumadores (58.5%) y 6 continuaban fumando (6.4%). Treinta y un pacientes eran obesos (IMC > 30); la distribución según el IMC se muestra en la Tabla 2. Se observó que el 50% de los pacientes, presentaron obesidad o sobrepeso y que en estos pacientes prevalecieron los diagnósticos de Sindrome apnea/hipopnea obstructiva del Sueño (SAHOS) y disfunción diafragmática.
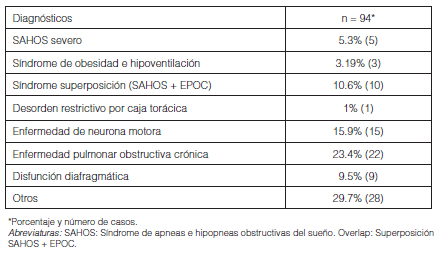
Los diagnósticos principales fueron: enfermedad de neurona motora (n = 15; 15.9%), EPOC (n = 22; 23.4%), síndrome de superposición (overlap) SAHOS/EPOC (n = 10; 10.6%), SAHOS (n = 5; 5.3%), disfunción diafragmática (n = 9; 9.5%), enfermedad restrictiva por pared torácica (n = 1; 1%), hipoventilación alveolar central (n = 1; 1%); en 28 (29.7%) pacientes se detectaron otras causas (síndrome de West, fibrosis quística, atrofia olivopontocerebelosa, síndrome de Charcot Marie Tooth, polineuropatía del paciente crítico, neumonitis intersticial) (Tabla 3).
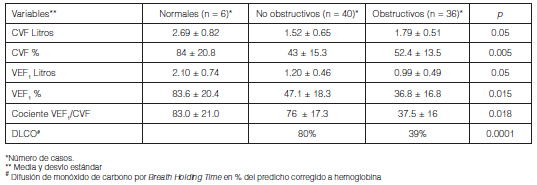
Ochenta pacientes recibían VMD al ingresar a UDOR (84%) como VNI en 77 casos y ARMI por traqueostomía en tres (4%). Finalmente, 14 pacientes (14.8%) fueron admitidos para evaluar la indicación de uso a largo plazo de VNI domiciliaria. Los datos del examen funcional respiratorio se detallan en la Tabla 4. En 53 pacientes con VNI se evaluaron indicadores respiratorios de la polisomnografía (PSG) o poligrafía respiratoria (PR) Tabla 5.

Los modos de VNI utilizados fueron; bilevel modo S/T (spontaneous/timed): 59 (62.7%); presión de soporte con volumen promedio asegurado (AVAPS) presométrico: 4 (4.2%); presión positiva continua en las vías respiratorias (CPAP9: 6 (6.4%), servo-ventilación: 1 (1%). Tres pacientes recibían ventilación volumétrica en modo asistido controlado. Se utilizaron máscaras nasales: 10 (12.6%), nasobucales; 62 (82.6%), total face; 2 (2.1%) y cánula de traqueostomía; 3 (4%). Veintitres pacientes (24.4%) usaban O2 suplementario desde fuente estacionaria mediante concentrador de O2.
La media de horas de cumplimiento objetivo (descarga de datos de built-in software) de la VNI fue de 8.1 horas (P25-75: 4.3-9.4). Cuatro pacientes no utilizaban el dispositivo a pesar de tener la indicación y el equipamiento correcto.
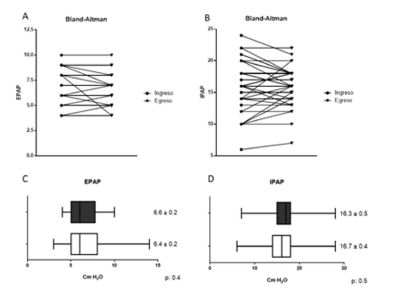
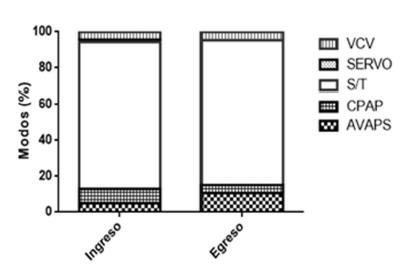
La media de la presión positiva espiratoria (EPAP) fue de 6.6 cm de H2O y en la presión positiva inspiratoria (IPAP) de 16.3 cm de H2O. El análisis de toda la población con VNI mostró que no existieron cambios significativos en los valores medios de los parámetros estudiados (Figura 1 C y D) antes y después de la evaluación en UDOR (p > 0.5). Sin embargo, en pacientes individuales los ajustes luego del análisis de datos de los software de los ventiladores fueron clínicamente significativos (Figura 1 A y B). Luego de la evaluación se cambiaron parámetros de programación en 37 pacientes (46.2%), modo ventilatorio en 2 (2.5%) y se suspendió la ventilación en dos casos (2.5%) Figura 2.
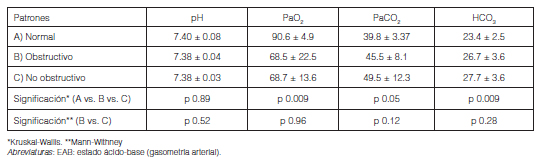
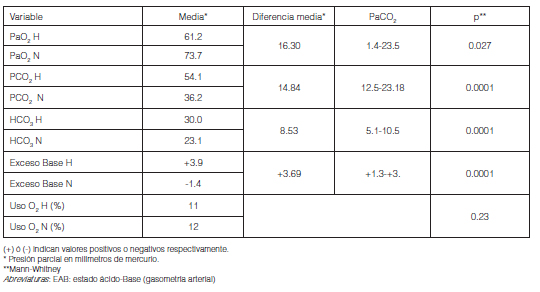
La gasometría arterial matinal en vigilia y sedestación con FIO2 0.21% en pacientes con VNI mostró (medias y desvío estándar); pH: 7.38 ± 0.04, PaO2: 66.2 ± 25.4 mmHg, PaCO2: 43.5 ± 15.6 mmHg, HCO3: 25.2 ± 7.8 mmHg. El funcional respiratorio alterado se correlacionó con mayor hipoxemia e hipercapnia (Tabla 6). Permanecieron hipercápnicos (PaCO2 > 45) cuarenta pacientes (42.5%) con VNI, quienes presentaban además mayor grado de hipoxemia y una mayor reserva alcalina (Tabla 7).
Los procedimientos más frecuentemente realizados en hospital de día fueron: gasometría arterial y estado ácido base (91.4%), espirometría computada (87%), descarga de datos de memoria (build-in software) del ventilador mecánico (78%), plan alternativo de contingencia (79.7%), pico flujo clásico y tosido (18%), interconsulta otras especialidades (16%), discusión de decisiones al fin de la vida o directivas anticipadas con el paciente y familiares (21%), entrenamiento en tos asistida con técnica de air stacking (18%), pautas de plan kinésico (10.6%), difusión de monóxido-DLCO (8.5%), laboratorio analítico (8.5%), radiografía de tórax (7.4%), cambio de cánula de traqueostomía (2.1%) y entrenamiento en ventilación por pieza bucal (2.12%).
Discusión
Este estudio expone la complejidad del manejo de pacientes con VMD en un programa basado en hospital de día. Nuestra población fue heterogénea, demostrando el protagonismo del especialista en medicina respiratoria y la versatilidad de la ventilación domiciliaria para un amplio espectro de patologías. Asimismo, la elevada proporción de comorbilidades y alteraciones de las pruebas de función pulmonar justifican el trabajo de un equipo multidisciplinario.
En las patologías vinculadas al sueño y la EPOC predominaron pacientes de mediana edad con obesidad; en sujetos con peso normal o bajo fueron más frecuentes las afecciones neuromusculares. A pesar de tratarse de enfermedades que comprometen la ventilación, sólo un 56% tuvo un estudio de sueño disponible, y este resultó patológico en todos los casos2, 21, 22.
Las técnicas de VNI han supuesto un enorme avance en el tratamiento de la insuficiencia respiratoria crónica de origen restrictivo. Los resultados disponibles muestran que la VNI mejora la calidad de vida, aumenta la supervivencia, mejora el intercambio de gases y consigue una mayor calidad de sueño. Actualmente, están bien establecidas sus indicaciones en enfermedades neuromusculares, defectos de la pared torácica, secuelas de tuberculosis o cirugías, síndrome de hipoventilación-obesidad y en otros síndromes de hipoventilación alveolar1-10. En nuestra serie este tipo de pacientes representaron el 44% de la muestra.
El período de adaptación a la VNI suele realizarse durante un ingreso hospitalario programado11, 23, aunque se ha descrito que puede también efectuarse con éxito en hospitales de día24. Quizás más importante que el lugar donde se haga la adaptación, sean la motivación, la experiencia y la dedicación del personal24. En nuestra serie, 15 pacientes (16% del total) fueron admitidos para evaluar la indicación de uso a largo plazo e iniciar adaptación de la VNI domiciliaria.
El cumplimiento de la VNI es directamente proporcional a la percepción de mejoría, a las intervenciones educativas realizadas sobre el paciente y su entorno, a la periodicidad del seguimiento y a la disponibilidad del equipo tratante y del prestador de servicio para la resolución práctica de los problemas que surjan durante la terapia. En nuestra experiencia, cuatro pacientes no cumplían el tratamiento, aunque la mayoría presentó una compliance aceptable con una media de 8.1 horas/día. Es importante señalar que el cumplimiento fue documentado mediante la memoria que poseen los respiradores y no a partir de los datos auto reportados por el paciente, que conducen frecuentemente a una sobreestimación de la utilización24. La revisión formal de los datos de cumplimiento y perfil de utilización del equipo debe ser un elemento semiológico de rutina durante la revisión clínica del paciente que recibe tratamiento con VMD cuando este recurso está disponible24, 25.
El monitoreo de la eficacia de la VMD debe incluir como mínimo una evaluación de la mejoría clínica y una apreciación mensurable de los objetivos buscados con la ventilación (corrección o mejoría de gases en sangre diurnos y de la oxigenación y ventilación nocturna) pero también el asegurarse una buena sincronía paciente-ventilador, sin eventos anormales. De tal manera, la ineficacia de la VNI puede reflejarse tanto en el plano clínico (no mejoría), como en el gasométrico (persistencia de la hipercapnia) o en el instrumental (built-in software o PSG/PR con VNI no satisfactorios). Es importante reconocer la condición cambiante de la mayoría de las patologías que requieren tratamiento con VMD. En este sentido, algunas enfermedades pueden ser inexorablemente progresivas, obligando a ajustes permanentemente.
Tal como se describe en otros países, los modos presométricos fueron los más frecuentemente usados en VNI y volumétricos para VMD invasiva. En este sentido el modo S/T fue el modo preferente y luego de la visita un 2.5% de los pacientes mudaron la modalidad de ventilación. La descarga y el análisis de datos objetivos permitieron ajustes significativos en algunos casos, situación que no había sido advertido previamente. Sin embargo, nuestro trabajo sólo describe las intervenciones y los hallazgos objetivos de una visita programada a UDOR. Por lo que la utilidad de tales intervenciones en el tiempo no han sido evaluadas y es esta una limitación de nuestro análisis.
Hallamos una relación entre el grado de compromiso de la función pulmonar evaluado por espirometría y la magnitud de los trastornos gasométricos. Tanto los defectos sugestivos de restricción como los de tipo obstructivo se relacionaron con mayor hipercapnia y aumento de la reserva alcalina,
aún en los pacientes con VMD. En este sentido es llamativo que a pesar de recibir VMD el 40% de los pacientes permanecían con algún grado de hipercapnia. Si bien nuestro trabajo no compara cambios gasométricos de manera longitudinal en esta cohorte, este dato obliga a revisar el procedimiento de la VMD ya que la gasometría representa un objetivo del tratamiento. Se ha descripto que es posible que en algunas patologías (fundamentalmente en la EPOC) uno de los objetivos de la VMD sea la mejoría (no la normalización) de los valores de CO2 y el pH como subrogante de eficacia de la ventilación11, 26.
El control del material es esencial en cada visita. Los proveedores y financiadores de la VMD deben asumir el compromiso de asegurar la correcta entrega del material necesario en condiciones óptimas de funcionamiento según las necesidades de cada paciente. Por su parte, el equipo tratante es responsable de colaborar en su mantenimiento y asegurar que el paciente y su entorno adquieran las destreza mínimas para garantizar un adecuado cuidado de los dispositivos y accesorios.
Finalmente, un aspecto complejo en los cuidados crónicos que conlleva tiempo y requiere de un entrenamiento y un espacio adecuados, son las decisiones al final de la vida. El manejo integral de pacientes con EPOC avanzado o enfermedades neuromusculares progresivas con frecuencia requieren un abordaje integral del equipo multidisciplinario27. El adecuado manejo de la información y el cabal conocimiento de las preferencias del paciente redundan en una adecuación del sistema de cuidados a sus necesidades24-27. En nuestra experiencia, la UDOR ha permitido un ámbito relajado donde mejorar el entrenamiento en las técnicas de VMD y discutir las opciones de tratamiento, diferente al ofrecido regularmente en la planta de internación, la guardia hospitalaria o al consultorio, permitiendo el contacto del paciente y su familia con especialistas en el manejo de los cuidados respiratorios. Finalmente, iniciativas como esta pueden mejorar el contacto de médicos y kinesiólogos jóvenes en formación con pacientes con patología compleja trabajando en equipo, aumentando la rentabilidad de la Unidad de Sueño, que dispone de camas con tiempo ocioso durante el periodo diurno que pueden utilizarse para el monitoreo de pacientes ventilados.
Limitaciones: Nuestra modalidad de hospital de día se limitó a un único centro. La heterogeneidad en las patologías que motivaron la ventilación crónica, el tipo de sistema de cobertura así como factores geográficos y sociales hace difícil la extrapolación a otras poblaciones. Además nosotros evaluamos los pacientes en una única visita un corto periodo luego del egreso hospitalario. Son necesarios seguimientos a largo plazo para valorar la utilidad de este tipo de estrategias.
Conclusión
La implementación del programa UDOR permitió mejorar el vínculo del paciente y su familia con el equipo tratante e identificar un alto porcentaje de pacientes con VMD ineficaz, permitiendo ajustes en la modalidad de tratamiento. Son necesarios estudios longitudinales para evaluar el impacto de este tipo de intervenciones a largo plazo.
1. King AC. Long-term home mechanical ventilation in the United States. Respir Care. 2012; 57: 921-930.
2. McKim DA, Road J, Avendano M, Abdool S, Cote F, Duguid N, et al; Canadian Thoracic Society Home Mechanical Ventilation Committee. Home mechanical ventilation: a Canadian Thoracic Society clinical practice guideline. Can Respir J. 2011; 18: 197-215.
3. Hannan LM, Dominelli GS, Chen YW, Darlene Reid W, Road J. Systematic review of non-invasive positive pressure ventilation for chronic respiratory failure. Respir Med. 2014; 108: 229-243.
4. Shneerson JM, Simonds AK Noninvasive ventilation for chest wall and neuromuscular disorders. Eur Respir J. 2002; 20: 480-487.
5. Farrero E, Antón A, Egea CJ, Almaraz MJ, Masa JF, et al. Normativa sobre el manejo de las complicaciones respiratorias de los pacientes con enfermedad neuromuscular. Arch Bronconeumol. 2013; 49: 306-311.
6. Howard RS, Wiles CM, Hirsch NP, et al. Respiratory involvement in primary muscle disorders: Assessment and management. Q J Med. 1993; 86: 175-189.
7. Howard RS, Davidson C. Long term ventilation in neurogenic respiratory failure. J Neurol Neurosurg Psych. 2003; 74: iii24.
8. Nugent A-M, Smith IE, Shneerson JM. Domiciliary-assisted ventilation in patients with myotonic dystrophy. Chest 2002; 121: 459-64.
9. Ojeda Castillejo E, de Lucas Ramos P, López Martin S, Resano Barrios P, Rodríguez Rodríguez P, et al. Noninvasive Mechanical Ventilation in Patients with Obesity Hypoventilation Syndrome. Long-term Outcome and Prognostic Factors. Arch Bronconeumol. 2014; Apr 2. pii: S0300-2896(14)00088.
10. López-Jiménez MJ, Masa JF, Corral J, Terán J, Ordaz E, Troncoso MF, et al; Grupo cooperativo. Mid- and Long-Term Efficacy of Non-Invasive Ventilation in Obesity Hypoventilation Syndrome: The Pickwick’s Study. Arch Bronconeumol. 2016; 52(3): 158-65.
11. Köhnlein T, Windisch W, Köhler D, Drabik A, Geiseler J, Hartl S, et al. Non-invasive positive pressure ventilation for the treatment of severe stable chronic obstructive pulmonary disease: a prospective, multicentre, randomised, controlled clinical trial. Lancet Respir Med. 2014; 2(9): 698-705.
12. Struik FM, Sprooten RT, Kerstjens HA, Bladder G, Zijnen M, Asin J, et al. Nocturnal non-invasive ventilation in COPD patients with prolonged hypercapnia after ventilatory support for acute respiratory failure: a randomised, controlled, parallel-group study. Thorax. 2014; 69(9): 826-834.
13. Murphy PB, Rehal S, Arbane G, Bourke S, Calverley PMA, et al. Effect of Home Noninvasive Ventilation With Oxygen Therapy vs Oxygen Therapy Alone on Hospital Readmission or Death After an Acute COPD Exacerbation: A Randomized Clinical Trial. JAMA. 2017; 317(21): 2177-2186.
14. Lloyd-Owen SJ, Donaldson GC, Ambrosino N, Escarabill J, Farre R, Fauroux B, et al. Patterns of home mechanical ventilation use in Europe: results from the Eurovent survey. Eur Respir J. 2005; 25: 1025-1031.
15. Nasiłowski J, Szkulmowski Z, Migdał M, Andrzejewski W, Drozd W, Czajkowska-Malinowska M, et al [Prevalence of home mechanical ventilation in Poland]. Pneumonol Alergol Pol. 2010; 78: 392-398.
16. Hazenberg A, Cobben NA, Kampelmacher MJ, Rischen J, Wijkstra PJ [Home mechanical ventilation in the Netherlands]. Ned Tijdschr Geneeskd. 2012; 156: A3609.
17. Datos del Observatorio Francés Antadir. Disponible en: http://observatoritrd.weebly.com/uploads/5/1/4/2/5142345/antadir_2010.pdf. Consultado 23-4-2016.
18. Farré R, Lloyd-Owen SJ, Ambrosino N, Donaldson G, Escarrabill J, Fauroux B, et al. Quality control of equipment in home mechanical ventilation: a European survey. Eur Respir J. 2005; 26: 86-94.
19. Farré R, Giró E, Casolivé V, Navajas D, Escarrabill J. Quality control of mechanical ventilation at the patient’s home. Intensive Care Med. 2003; 29: 484-486.
20. Martínez Fraga A, Jordán P, Ávalos V, Romera A, Vincent V, et al. Ventilación mecánica domiciliaria con doble nivel de presión positiva. Experiencia de un hospital de Buenos Aires. Rev Arg Med Resp. 2014; 2: 136-143.
21. Schenk P, Eber E, Funk GC, Fritz W, Hartl S, et al. Non-invasive and invasive out of hospital ventilation in chronic respiratory failure: Consensus report of the working group on ventilation and intensive care medicine of the Austrian Society of Pneumology]. Wien Klin Wochenschr. 2016; 128 Suppl 1: S1-36.
22. Rabinstein AA. Noninvasive ventilation for neuromuscular respiratory failure: when to use and when to avoid. Curr Opin Crit Care. 2016; 22(2): 94-9.
23. Luján M, Moreno A, Veigas C, Montón C, Pomares X, Domingo C. Non-invasive home mechanical ventilation: effectiveness and efficiency of an outpatient initiation protocol compared with the standard in-hospital model. Respir Med. 2007; 101: 1177-1182
24. Díaz-Lobato S, Mayorales-Alises S. Setting up and organizing a noninvasive ventilation unit for hospital and home therapy. Arch Bronconeumol. 2005; 41(10): 579-83.
25. Luján M, Sogo A, Monsó E. Software de monitorización de ventilación mecánica domiciliaria: ¿medir más o medir mejor? Arch Bronconeumol 2012; 48: 170-8.
26. Lemyze M, Bury Q, Guiot A, Jonard M, Mohammad U, Van Grunderbeeck N, et al. Delayed but successful response to noninvasive ventilation in COPD patients with acute hypercapnic respiratory failure. Int J Chron Obstruct Pulmon Dis. 2017; 12: 1539-1547.
27. Fahim A, Kastelik JA. Palliative care understanding and end-of-life decisions in chronic obstructive pulmonary disease. Clin Respir J. 2014; 8(3): 312-320.