Autor : SĂvori Martin1-2
1 Centro Universitario de NeumonologĂa, Facultad de Medicina. Universidad de Buenos Aires. 2 Unidad de NeumotisiologĂa. Hospital Gral. Agudos Dr. J. M. Ramos MejĂa. Buenos Aires.
https://doi.org/10.56538/ramr.CXYQ1701
Correspondencia :MartĂn SĂvori: E-mail: sivorimartin@yahoo.com
Un
poco de historia
El
asma y la enfermedad pulmonar obstructiva crĂłnica (EPOC) son enfermedades
heterogĂ©neas obstructivas de la vĂa aĂ©rea, cuyas fisiopatologĂas distan mucho
de ser completamente comprendidas aĂșn hoy en dĂa.
A
mĂĄs de 60 años de la generaciĂłn, casi simulÂtĂĄneamente, de dos hipĂłtesis sobre
la génesis del asma y la bronquitis crónica asociada a la EPOC y, a pesar del
tiempo transcurrido, con enfrentaÂmientos a veces personales y apasionados, se
las ha presentado generalmente como hipĂłtesis conÂtrapuestas: la afirmaciĂłn de
una, negaba la otra, y viceversa.1-8
MĂĄs
de seis décadas han pasado desde entonces, y el objetivo de este manuscrito es
revisar quĂ© conÂceptos han quedado firmes con el paso del tiempo a la luz de
las recientes investigaciones y que, a juicio del autor de este manuscrito, han
sido relevantes.
¿Qué
decĂa la hipĂłtesis britĂĄnica?
A
principios de la década de 1950, la EPOC como tal no estaba descripta y Lynne McA Reid
y Mc Lean asociaron al tabaquismo a la presencia de broncorrea, tos crĂłnica, a
cambios de la defensa mucosa bronquial, a la colonizaciĂłn bacteriana e
infecciones frecuentes que llevaban a la génesis de la bronquitis crónica
obstructiva. A esta hipĂłÂtesis se la conociĂł como âhipĂłtesis britĂĄnicaâ (Figura
1).1, 2

¿Qué
decĂa la hipĂłtesis holandesa?
Debido
a que el asma y la EPOC comparten algunos aspectos comunes, entre 1961 y 1964,
el Dr. NG Dick Orie propuso desde su tesis doctoral
en la UniÂversidad de Groningen, Holanda, que el
asma, la bronquitis crĂłnica y el enfisema eran expresiones fenotĂpicas de la
misma enfermedad y que evoluÂcionaban una a otra a medida que se envejecĂa en
relaciĂłn con diferentes factores: Bronchitis
and Asthma may be found in one patient
at the same age but as a rule there is a fluent
development from bronchitis in youth to a more asthmatic picture in adults, which in turn develops
into bronchitis of elderly patients (Figura 2).3, 4

A
raĂz del interĂ©s que despertĂł tan osada hipĂłÂtesis, se generĂł en 1962 un
Simposio Internacional en âBronquitis CrĂłnicaâ.5 De la relaciĂłn entre factores
exógenos (medio ambiente, exposición a alérgenos y humo de tabaco) y endógenos
(atopĂa e hiperreactividad bronquial), se expresarĂa de forma diferente la
bronquitis crĂłnica. Fue motivo de gran disputa entre investigadores del Reino
Unido, resto de Europa y Estados Unidos de Norteamérica hasta años recientes.5-10
Fue en 1969 que el Dr. Fletcher la
caratulĂł como la hipĂłtesis holandesa.
A MĂS DE 60 AĂOS
DESPUĂS, ÂżQUĂ NUEVA INFORMACIĂN HAY SOBRE LA HIPĂTESIS BRITĂNICA?
Cuando
se formulĂł la hipĂłtesis britĂĄnica, varios hechos no se conocĂan, o no con la
suficientemente profundidad como en la actualidad. Ellos son, a manera de
ejemplo, la evoluciĂłn al concepto de pre- EPOC, la importancia de la presencia
de sĂntomas respiratorios en estadios tempranos de la EPOC, la caracterizaciĂłn
del fenotipo exacerbador frecuente y la importancia
de la microbiota respiratoria. ToÂdos ellos en la
actualidad robustecen lo enunciado hace mås de 60 años por Lynne
McA Reid.1
SĂntomas
respiratorios crĂłnicos
Si
bien los trabajos fundamentales de Fletcher y cols. demostraron que la bronquitis crĂłnica (BC, tos y broncorrea
crĂłnica) y la obstrucciĂłn al flujo aĂ©reo crĂłnica eran dos situaciones clĂnicas
sepaÂradas que podĂan estar asociados, y que no estaba relacionada con pĂ©rdida
acelerada de la funciĂłn pulmonar, otros estudios mĂĄs recientes han reÂtomado
este concepto hasta llegar a la propuesta del estadio âpre-EPOCâ que se
desarrollarĂĄ en el acĂĄpite siguiente. La broncorrea estĂĄ asociada a mayor
declinaciĂłn del volumen espiratorio forzaÂdo del primer segundo (VEF1), y a mayor riesgo de
desarrollar EPOC en fumadores jóvenes con BC.11-14 También estå asociada a mayor
nĂșmero y gravedad de las exacerbaciones.15 Varios estudios de cohortes
han estudiado en personas con funciĂłn pulmonar preservadas, la presencia de
sĂntomas respiratorios crĂłnicos y su relaciĂłn con la evoluciĂłn hacia la EPOC.16-22
En el estudio SALPADIA-1, se observĂł que las personas con
broncorrea y funciĂłn pulmonar casi normal (GOLD 1) presenÂtaban mayor
declinaciĂłn del VEF1 y
consumo de recursos de salud en seguimiento a 3 años.16 En el Copenhagen
City Heart Study, se
determinó a 5 años que el OR de la presencia de broncorrea como factor de
riesgo de EPOC era de 1,1 (0,9-1,4) y a 15 años 1,2 (0,9-1,6), sin embargo, la
broncorrea estaba asociada a mayor declinaciĂłn del VEF1
y morbilidad (hospitalizaciĂłn, OR 5,3 para hombres, 2,9-9,6; y
5,1 para mujeres, 2,5-10,3).17 En la coÂhorte SPIROMICS, se
determinĂł que los sujetos fumadores con funciĂłn pulmonar normal ya preÂsentaban
aumento de celularidad inflamatoria en la mucosa
bronquial vs. controles.18 En la cohorte COPDGene, en fumadores con funciĂłn pulmonar normal, se
determinĂł declinaciĂłn acelerada de la funciĂłn pulmonar.19 En la cohorte del Biobank del Reino Unido, 351 874 sujetos fueron seguidos a
9 años, y se relacionó la obstrucción al flujo aéreo con la presencia de
sĂntomas respiratorios.20 Se determinĂł, entre otros
factores, que el deterioro de la funciĂłn pulmonar estaba asociada fuerteÂmente
a la presencia de sĂntomas respiratorios y comorbilidades cardiovasculares (OR
ajustados 2 [95% CI 1,91-2,14], p < 0,0001) y 1,71 [1,64-1,83], p <
0,0001).20
El deterioro de la funciĂłn pulmonar estuvo asociado a mortalidad
global (HR 1,61 [95 % CI 1,53-1,69], p < 0,0001) vs. controles.20
Sherman y cols. en 3948 sujetos seguidos
a 12 años, compararon aquellos con sĂntomas respiÂratorios (sibilancias
persistentes, tos crĂłnica, expectoraciĂłn crĂłnica o disnea) o sin estos en
relaciĂłn con el VEF1, y
ajustados por la exposiciĂłn al tabaco y la altura. Los hombres con tos crĂłnica
y las mujeres con expectoración crónica presentaron pérdida acelerada del VEF1.21 Lange
y cols., en un estudio en Copenhagen, de 13 756
seguidos a 10 años determinaron que la expectoración crónica estuvo asociado a
mayor mortalidad global dĂ©bilÂmente (RR = 1,1 mujeres y 1,3 hombres), pero en
aquellos con obstrucciĂłn grave (VEF1 40%)
fue mayor (RR 4,2)22.
En la actualidad, la terapia sugerida por las guĂas GOLD estĂĄ basada en la
clasificaciĂłn matrizal ABE, segĂșn la presencia de
disnea, alteraciĂłn de la calidad de vida y tipo y nĂșmero de exacerbaciones.23
Sin embargo, se ignora por el momento la presencia de broncorrea
o tos crónicas o el grado de obstrucción bronquial en la decisión terapéutica.
El VEF1 es un factor
independiente de mortalidad, y fue usado como criterio de inclusiĂłn para el
desarrollo clĂnico de los actuales broncodilatadores de acciĂłn prolonÂgada y
corticoides inhalados, y sus asociaciones en los Ășltimos 20 años.24
Sin embargo, recientes investigaciones demuestran, a manera de
ejemÂplo, que no tienen la misma evoluciĂłn un paciente GOLD A o B con leve o
grave obstrucciĂłn bronÂquial, sin embargo, esto no es tenido en cuenta por las
actuales recomendaciones de tratamiento farmacolĂłgico de las guĂas GOLD.25, 26
Han y cols., recientemente, en personas con exposiciĂłn a taÂbaco
(>10 paquetes-año) y CAT > 10 (sĂntomas respiratorios), demostraron que
la doble terapia broncodilatadora de acciĂłn prolongada no mejora la calidad de
vida.27
Concepto pre-EPOC
Todo
lo histĂłricamente reseñado arriba, es reÂcientemente tomado por un grupo de
reconocidos especialistas internacionales que publicaron un documento donde
proponen retomar el concepto controvertido por las GuĂas GOLD 2001 del estadio
0 y cambiarlo por âpre-EPOCâ en pacientes que no cumplen criterios actuales
GOLD de EPOC, basado en tres dominios:28-30
A.
ClĂnica: La presencia de broncorrea, tos, disnea y exacerbaciones.
B.
Funcional. Pacientes con relaciĂłn VEF1/
FVC mayor de 0,7 posbroncodilatadores, pero con
signos de atrapamiento aĂ©reo en la mediciĂłn de volĂșmenes pulmonares o
disminuciĂłn de la DLCO (difusiĂłn de monĂłxido de carbono) o signos de
obstrucciĂłn de la pequeña vĂa aĂ©rea.
C.
ImĂĄgenes: Presencia en la tomografĂa comÂputarizada de tĂłrax de enfisema centrolobulillar, engrosamiento de las paredes bronquiales
de la vĂa aĂ©rea mayor o signos de compromiso de la pequeña vĂa aĂ©rea.
Microbiota y las enfermedades
respiratorias
La
comunidad microbiolĂłgica de bacterias, honÂgos, virus y arqueas que habitan
nuestro cuerpo constituyen en su conjunto el âmicrobiota
humaÂnoâ y, si consideramos la carga genĂ©tica en su conjunto, se la nombra como
âmicrobioma huÂmanoâ.31-33 Las vĂas aĂ©reas no son
estĂ©riles y una comunidad de microorganismos la habitan e inÂteraccionan con
nuestro organismo en equilibrio, en el estado saludable. Las vĂas aĂ©reas
inferiores tienen menor biomasa de microorganismos debido a los nutrientes mĂĄs
escasos y los mecanismos inmunolĂłgicos locales de aclaramiento mucociÂliar.31-33
Los microorganismos penetran desde la orofaringe
por microaspiraciones o dispersión a través de la
mucosa.31-33 Por ello, la microbiota respiratoria tiene una directa interacciĂłn con
la del tubo digestivo, especialmente la de la vĂa aĂ©rea superior.31-33
La interacciĂłn de ambas miÂcrobiotas
tambiĂ©n se darĂa de forma sistĂ©mica a travĂ©s de diversos metabolitos que las
bacterias intestinales afectan el sistema inmune sistémico. Pero no solo
involucran a las bacterias (las mås estudiadas), sino también al micobioma y viroma pulmonar.31-33
Al desequilibrio en esta interacción huésped-microorganismos se
lo denomina âdisbioÂsisâ.31-35 Puede estar provocado por
antibiĂłticos, alteraciones nutricionales o infecciones externas que alteran la
flora residente comensal benigna. Existe evidencia cada año mås sólida de que
la alteraciĂłn del microbioma tiene un papel en vaÂrias
enfermedades en las Ășltimas dos dĂ©cadas.31-35 Tanto en enfermedades de la
vĂa aĂ©rea como asma, EPOC o fibrosis quĂstica, como en otras consideÂradas
ajenas a una relaciĂłn con microorganismos tradicionalmente, como la fibrosis
pulmonar idiopåtica, el cåncer o distrés agudo
respiratorio del adulto.31-35 En asma, la exposiciĂłn en edad
temprana a microorganismos tiene consecuencia en la sensibilidad a largo plazo.36
La
primera generaciĂłn de estudios fue desÂcriptiva y evaluĂł la secuencia gĂ©nica de
16S rRNA para caracterizar los microbiotas
del tubo digestivo y respiratorio. Luego de los estudios in vitro e in
vivo en animales, comenzaron los estudios controlados en humanos para
evaluar la interacción huésped-microorganismo en las enfermedades. Estån en
desarrollo estudios de consorcios académicos multicéntricos,
debido a la variabilidad poblacional y geogrĂĄfica que influyen en los hallazgos
y la estandarización de métodos y anålisis de datos multiómicos
mås allå de las bacterias, que incluyen virus, hongos y arqueas. También se
debe tener en cuenta la variabilidad interindividual en el curso de la
enfermedad y la respuesta a los diversos tratamientos. Estamos en la puerta de
una nueva era de la medicina de preÂcisiĂłn donde el microbioma
podrĂa contribuir al entendimiento de nuevas formas de patogenia de
enfermedades, sus diagnĂłsticos y tratamientos.32 La EPOC es un sĂndrome
complejo caracterizado por diferentes fenotipos, todos con comĂșn denomiÂnador
de la obstrucción crónica al flujo aéreo. La microbiota
en la EPOC difiere sustancialmente de la de los individuos controles sanos, que
se inÂcrementa aĂșn mĂĄs durante las exacerbaciones.35 La dinĂĄmica de los cambios
obedece a mĂșltiples factores, como son la heterogenicidad
fenotĂpica de la EPOC, los cambios fisiopatolĂłgicos, trataÂmientos impuestos
(corticoides y antibiĂłticos), el tabaquismo y las exacerbaciones.35
El 40%-50% de las exacerbaciones son gatilladas por bacterias que
incrementan la inflamaciĂłn y obstrucciĂłn de la vĂa aĂ©rea y la broncorrea. Los
géneros de bacterias involucrados mås frecuentemente son Streptococcus,
Pseudomonas, Moraxella, HaemoÂphilus, Neisseria, Achromobacter, Corynebacterium y
atĂpicos, como Mycoplasma pneumoniae y ChlaÂmydia pneumoniae.35
En particular con respecto a la EPOC, la carga bacteriana estĂĄ
relacionada con mayor incidencia de exacerbaciones y declinaciĂłn de la funciĂłn
pulmonar.36 Una determinada cepa genera
una respuesta inmune especĂfica. La apaÂriciĂłn de una cepa diferente aumenta el
riesgo de exacerbaciones.37 Bafadhel
y cols. determinaron diferencias fundamentales en la
inmunoterapia.38 El tipo de exacerbaciĂłn puede ser
predicho durante la fase estable de la EPOC. En las exacerbacioÂnes frecuentes,
el patrĂłn tiende a repetirse. El fenotipo bacteriano se encontrĂł en el 55% de
los casos; el eosinofĂlico, en el 29%; viral, 28%; y
el resto, paucinflamatoria. Los niveles de IL-6 y
IL-8 pueden predecir en los exacerbadores frecuentes
a los mĂĄs proclives a exacerbarse.38 A su vez, las infecciones
virales pueden alterar el equilibrio del microbioma,
lo que incrementa la sensibilidad a inÂfecciones bacterianas secundarias y exacerbaciones
asociadas.31-35 Las infecciones por virus sincicial resÂpiratorio, influenza A virus y rhinovirus aumentan la expresiĂłn de molĂ©culas de adhesiĂłn
bacterianas (por ejemplo, ICAM-1, PAFR, CEACAM-1) en las células epiteliales,
que promueven el desarrollo de H. influenzae, S pneumoniae y P. aeruginosa.39,
40 Los
virus respiratorios tambiĂ©n deterioran el aclaraÂmiento mucociliar
y dañan las células epiteliales, ya que alteran la primera barrera de defensa
de la mucosa del ĂĄrbol respiratorio y permiten la inÂvasiĂłn a travĂ©s de ella de
bacterias patĂłgenas.39, 40 Interesantemente, las
relaciones del microbioma del tracto gastrointestinal
en modelos animales, los metabolitos de bacterias comensales del tubo digestivo
protegen contra infecciones por virus respiratorios y, a su vez, otros
producidos por el microbioma respiratorio lo protegen
de infeccioÂnes bacterianas y virales.39,
40 Los
hongos como el gĂ©nero Aspergillus han sido como etiologĂa de
exacerbaciones en asma, EPOC, fibrosis quĂstica y bronquiectĂĄsicos.31
Infecciones
respiratorias y fenotipo exacerbador
La
historia de infecciones graves en la niñez estå asociada a reducción de la
funciĂłn pulmonar y presencia de sĂntomas respiratorios en la adultez.41 Existe
evidencia de que la infecciĂłn por virus de la inmunodeficiencia humana (VIH)
representa un riesgo aumentado de desarrollar EPOC (OR 1,14, IC95% 1,05-1,25),
asĂ como la tuberculosis.42,
43 Desde
los trabajos de Soler Cataluña y cols. donde se
demostraba claramente cómo tener 1-2 exacerbaciones en el año previo, o incluso
mĂĄs, en comparaciĂłn a no tenerlas presentaba un riesgo aumentado de mortalidad
y hospitalizaciĂłn44.
DoÂnaldson y cols. demostraron que el subgrupo de
pacientes que se exacerban frecuentemente tiene un declive acelerado de su
funciĂłn pulmonar.45 Pero, ademĂĄs,
todo ello, se asociaba a peor calidad de vida.46
El estudio ECLIPSE brindĂł informaciĂłn complementaria acerca de
cĂłmo el subgrupo de pacientes exacerbadores
frecuentes en el año preÂvio, a lo largo de tres años de seguimiento, tenĂan
mĂĄs probabilidades de seguir exacerbĂĄndose, a la vez que lo inverso pasaba en
los que nunca se habĂan exacerbado.47 Las guĂas
GOLD a partir del año 2011 consideraron esta condición como fenotipo que
permitiĂł calificar el mayor riesgo de morbimortalidad, y de condicionar su
tratamiento farmacolĂłgico especial.23
MĂS DE 60 AĂOS
DESPUĂS, ÂżQUĂ NUEVA INFORMACIĂN HAY SOBRE LA HIPĂTESIS HOLANDESA?
Muchos
avances en el campo de la genética en asma y la EPOC, el impacto del desarrollo
neonatal en la funciĂłn pulmonar, la exposiciĂłn a gases de bioÂmasa, la
presencia de hiperreactividad bronquial en EPOC, el fenotipo agudizador eosinofĂlico en la
EPOC (o superposiciĂłn asma-EPOC) y el eosinĂłfilo como
biomarcador tendrĂan o tienen implicancias en el
manejo actual. Han robustecido lo expuesto como hipĂłtesis holandesa hace mĂĄs de
60 años por Dick Orle.3-10
Avances en genética
en asma y EPOC
La
revolución en investigación genética ha sido de los mås maravillosos y råpidos
avances en la comÂprensiĂłn de la fisiopatologĂa y etiologĂa de muchas
enfermedades, entre ellas del asma y la EPOC, en los Ășltimos veinte años a
partir del desarrollo completo del Proyecto del Genoma Humano.
En
2011, Dirkje Postma retomĂł
el tema de cĂłmo se deberĂa ver la hipĂłtesis holandesa a la luz de los avances
en genética y los factores ambientales comunes al asma y EPOC.48
A partir de la carga genética, los diferentes factores
ambientales (alĂ©rÂgenos, irritantes, tabaco, etc.), desencadenaban diferentes
velocidades de crecimientos fetales del tejido pulmonar y luego del nacimiento,
la genĂ©tica en su relaciĂłn con los factores ambientales (epigeÂnĂ©tica)
permiten expresar los diferentes fenotipos clĂnicos (Figura 3).48
Mås de diez años después de la generación de la hipótesis
holandesa, Fletcher y Peto, en su famoso estudio,
habĂan determinado un grupo de personas que, por mĂĄs que estuvieran expuestas
al humo de tabaco, no desarrollarĂan EPOC (âno susceptiblesâ los llamaron), y
otros que sĂ (âsusceptiblesâ).11 Kaneko y cols. han revisado la
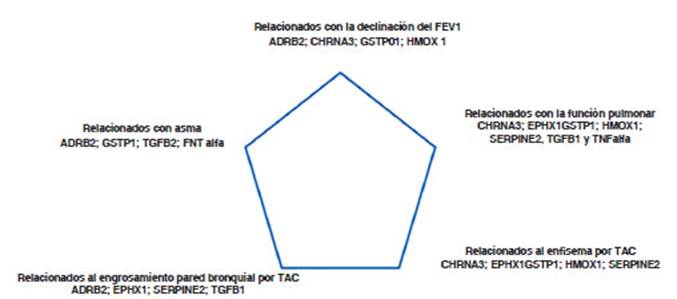
lista de genes comunes codificantes al desarrollo de asma y EPOC.49 Por lo menos
diez vĂas de señalizaÂciĂłn molecular han sido determinadas en la gĂ©nesis
asociada del asma y la EPOC, y cada uno estĂĄ relaÂcionada con varios genes
regulatorios (Tabla 1).49 MĂĄs
recientemente, Agusti y Hogg
resumieron los veintidĂłs genes que estĂĄn mĂĄs relacionados con el desarrollo de
la EPOC50.
Ellos son: TGFB2, PID1, RARB, EEFSEC, FAM13A, GSTCD, HHIP, TET2, DSP,
HTR4, ADAM19, AGER, ADGRG6, ARMC2, SFTPD, RIN3, THSD4, CHRNA5, CCDC101, CFPDP1,
MTCL1 y CYP2A6. Entre estos genes, se detallan los que se relacionan con
otra teorĂa famoÂsa que explica tambiĂ©n parte de la fisiopatologĂa de la EPOC:
la de âproteasas y antiproteasasâ.23,
39, 40, 50
Desde el siglo pasado, la acciĂłn de las proteasas y la
destrucciĂłn del tejido elĂĄstico pulmonar ha sido relacionada con el enfisema.23, 39, 40, 50 Las prinÂcipales
proteasas son la elastasa del neutrĂłfilo y la
proteinasa-3. Las proteasas serinas son potentes
estimulantes de la producciĂłn de muco e inducen
broncorrea en los pacientes con bronquitis crĂłnica. MĂĄs recientemente, se ha
determinado que las metaloproteinasas MMP-1 y nueve derivadas
de macrĂłfagos y neutrĂłfilos estĂĄn sobreexpresadas en
los pacientes con enfisema, e inducidas su sĂntesis por la acciĂłn del tabaco.23, 39, 40, 50 Sin embargo,
el tejido pulmonar normal estĂĄ protegido de ellas por la actividad de las antiproteasas. El mayor inhibiÂdor de las proteasas serinas es la proteĂna alfa-1 antitripsina,
una alfa-1 globulina. El modelo de origen genético del enfisema por déficit de
la alfa-1 antitripsina ha sido extensamente estudiado
y hoy posible de diagnĂłstico precoz y terapia sustitutiva con la proteĂna.23, 39, 40, 50 Otro factor
de importancia génica es la longitud acortada de los telómeros
que estĂĄ relacionado con la mayor susceptibilidad del enfisema.51, 52 Morla y cols. en un interesante estuÂdio controlado con personas normales
demostraron que la longitud de los telĂłmeros se
acorta en los fuÂmadores (p = 0,05), y en especial a mayor carga taÂbĂĄquica
(p < 0,001), y con obstrucciĂłn bronquial.52
Incluso se ha determinado cuĂĄles mutaciones del gen regulador de
la telomerasa conllevan mayor riesgo de enfisema,
fibrosis pulmonar idiopåtica, falla primaria en médula ósea y pérdida de pelo,
y se heredan con dominancia autosĂłmica.52

Desarrollo neonatal y
funciĂłn pulmonar
La
trayectoria de la evoluciĂłn de las trayectorias del crecimiento de la funciĂłn
pulmonar estĂĄ estaÂblecida desde la gestaciĂłn, nacimiento, infancia y
adolescencia.48,
53, 54 El
50% de los pacientes que desarrollan EPOC no estarĂa vinculada a aceleraÂciĂłn
de la pérdida de la función pulmonar, sino a anormal crecimiento del pulmón
gestacional y en la infancia temprana.55
Los genes envueltos en el desarrollo pulmonar, junto con la
exposiciĂłn materna al tabaco o gases de biomasa tienen importantes influencias
en el desarrollo de asma y EPOC.48,
56, 57 La
expresiĂłn de genes diferentes durante el desarrollo de la vĂa aĂ©rea uterina,
como la señal de los genes Wnt, ha sido asociada a la
disminución de la función pulmonar en la niñez y asma,58, 59 la aparición de hiperreactividad bronquial y
sensibilización alérgica en diferente grado, que desencadenan cambios
inflamatorios que retroalimenten el daño estructural de la vĂa aĂ©rea (remodelamiento, enfisema, enfermedad de la pequeña vĂa
aérea, inflamación bronquial y broncorrea, etc.) hasta llegar a la obstrucción
bronquial y expresar diferentes fenotipos.50
Del 4% al 12% de la poblaciĂłn general no tiene el VEF1 que estĂĄ
dentro del predicho para su género y edad; muchos de ellos tendrån limitación
al flujo aéreo y aceleración de la pérdida del VEF1, con incidencia mås alta y a mås temprana
edad, que coexistirĂĄn con enfermedades cardĂacas y metabĂłlicas y mayor
mortalidad.60 AsĂ no llegar
al mĂĄximo VEF1 en la
adultez temprana identifica un grupo de mayor riesgo de desarrollar EPOC y
otras enfermedades prevenibles y tratables.61
ExposiciĂłn a gases de
biomasa y contaminaciĂłn ambiental
Si
bien la principal etiologĂa de la EPOC en OcciÂdente es el tabaquismo, en
pueblos rurales y zonas urbanas sin acceso a gas natural, la combustiĂłn de
biomasa (30%-75% combustión de biomasa es hogareña) es un reconocido factor de
EPOC, incluso en algunas ocupaciones laborales.23, 62-64 En el estudio PLATINO, el 12% de los pacientes
con EPOC y el 29,7% en el estudio EPOC.AR no tenĂan antecedentes de tabaquismo,
pero sĂ declaraban antecedente de exposiciĂłn a gases de biomasa el 16% en
PLATINO y el 42% en EPOC. AR.65,
66 La
combustión de madera, estiércol, carbón vegetal, residuos de cosecha, libera
mĂĄs de 250 compuestos orgĂĄnicos, lĂquidos volĂĄtiles y gases, el 90% en rango
inhalable (monĂłxido de carbono,amonĂaco,
ĂĄcido cianhĂdrico, formalÂdehĂdo, Ăłxidos de nitrĂłgeno y azufre, benceno,
hidrocarburos aromĂĄticos policĂclicos [benzoÂpireno],
kerosene).23,
62-64 El
riesgo de EPOC es 2,44 ante la exposiciĂłn a gases de biomasa. Se ha estimado
que la exposiciĂłn de mĂĄs de 100 h/año es suficiente para generar sĂntomas respiratorios
y mås de 200 h/año obstrucción al flujo aéreo.62-64 La EPOC vinculada a la inhalación de gases de
biomasa tiene una diferente expresiĂłn fenotĂpica en comparaciĂłn al del
tabaquismo. Se ha obserÂvado mayor presencia de sĂndrome de superposiÂciĂłn asma-EPOC
e hiperreactividad bronquial, bronquiectasias, menor enfisema y mĂĄs presencia
de bronquitis crĂłnica e hipertensiĂłn pulmonar. En las pruebas funcionales
respiratorias menor compromiso del VEF1,
con menor deterioro anual de Ă©l y no tanto compromiso de la prueba de DLCO2.3, 62-64 En cuanto a
la relaciĂłn entre el deÂsarrollo de EPOC y la contaminaciĂłn ambiental,
recientemente la AsociaciĂłn Estadounidense de TĂłrax ha revisado toda la
evidencia, y la considerĂł todavĂa insuficiente como para establecer una
relaciĂłn causa-efecto.67 Con respecto
al asma en niños existe fuerte evidencia de que la exposición prolongada por
contaminaciĂłn ambiental del trĂĄnsito de diĂłxido de nitrĂłgenoy
carbĂłn negro estĂĄ relacionada con la apariciĂłn de sĂntomas por asma, y sugestivo
en adultos, aunque aĂșn insufiÂciente evidencia. En asma, la poluciĂłn ambiental
de partĂculas de diĂĄmetro aerodinĂĄmico menor de 2,5 um
y el ozono, generan remodelaciĂłn de la vĂa aĂ©rea y aumento de su incidencia y
gravedad.67
EPOC e hiperreatividad bronquial
Varios
estudios longitudinales han demostrado que el asma es factor de riesgo para el
desarrollo de obsÂtrucciĂłn al flujo aĂ©reo crĂłnica y EPOC, como el de Tucson que
demostrĂł doce veces mĂĄs alto el riesgo, ajustado por la exposiciĂłn al
tabaquismo.68 Incluso el
patrón de crecimiento de la función pulmonar en niños con asma estå asociado al
desarrollo de EPOC a edad adulto temprana, hecho que ya habĂa sido anticipado
por Dick Orie.3,
4, 69 Por
otra parte, en el European Community
Respiratory Health Survey, la hiperreactividad bronquial (HRB) es luego del
tabaquismo es el factor independiente mĂĄs asociado al desarrollo de EPOC.70 La HRB no
necesariamente estĂĄ asociada al asma y de forma independiente estĂĄ asociada al
mayor riesgo de EPOC, mortalidad respiratoria y mayor declinaÂciĂłn de la
funciĂłn pulmonar en EPOC leve.71,
72
Fenotipo
superposiciĂłn ASMA-EPOC o agudizador eosinofĂlico en EPOC
En
España, en el año 2012, Soler Cataluña y cols. publicaron
un documento sobre la superposiciĂłn asma-EPOC.73
Las guĂas GESEPOC en ese mismo año incorporan el concepto,
estableciendo criterios mayores y menores. Se deberĂan cumplir con dos mayores
o un criterio mayor y dos menores.74 Los criterios
mayores fueron la prueba de broncodilaÂtadores muy positiva (> 400 mL del VEF1
o >15% de incremento), eosinofilia
en esputo y anteceÂdentes personales de asma. Los criterios menores fueron
niveles plasmĂĄticos de IgE total elevados,
antecedentes personales de atopĂa y prueba con broncodilatadores al menos en
dos ocasiones con incremento del VEF1
> 200 mL o 12%.74
A partir del 2014, las guĂas GINA y GOLD incorporaron
simultĂĄneamente el concepto fenotipo superpoÂsiciĂłn asma-EPOC, teniendo en
cuenta que este subgrupo de pacientes tienen peor calidad de vida,
exacerbaciones frecuentes, deterioro acelerado de la funciĂłn pulmonar, alta
mortalidad y consumo de recursos de salud.75
Dependiendo de los criteÂrios usados, diferentes estudios
encontraron una prevalencia entre el 15% y el 55%, pero en la vida real
probablemente sea cercano al 15 %-20% de los pacientes diagnosticados en la
vida real en atenÂciĂłn mĂ©dica. Los criterios propuestos fueron edad mayor de 40
años, pero con sĂntomas en la infancia o juventud; disnea al esfuerzo
persistente pero variable; obstrucción a flujo aéreo no totalmente reversible y
variable; historia familiar, personal de alergias, atopĂas o asma; sĂntomas que
mejoran con tratamiento, pero que pueden progresar con mayor requerimiento de
Ă©l; presencia de exacerbaciones y comorbilidades; eosinofilia
en el esputo o neutrofiÂlia. Se señalĂł la
problemĂĄtica en los pacientes añoÂsos y fumadores con antecedentes de asma de
hacer el diagnĂłstico diferencial entre ambas patologĂas, y se expresĂł a la
superposiciĂłn ASMA-EPOC no como una nueva enfermedad, sino como la forma de
expresiĂłn fenotĂpica de enfermedades de la vĂa aĂ©rea, en las que subyacen
complejos mecanismos fisiopatológicos en simultåneo. Sin y cols. también
publicaron un documento de consenso sobre los criterios de definiciĂłn la
superposiciĂłn ASMA-EPOC, en el que reĂșnen tres criterios mayores y, por lo
menos, uno menor: los criterios mayores fueron persistente obstrucciĂłn al flujo
aéreo (VEF1 FVC
< 0,7 o del LLN) en individuos de 40 años o mayores; por lo menos, diez
paquetes-año de tabaquismo o exposición a biomasa o historia de asma antes de
los 40 años o respuesta a broncodiÂlatadores en la espirometrĂa
mayor de 400 mL del VEF1.76 Los criterios
menores fueron historia de atopĂa documentada o rinitis alĂ©rgica; respuesta de
broncodilatadores en la espirometrĂa mayor a 200 mL del VEF1
y el 12% del basal en dos mĂĄs ocasiones; eosinofilia
mayor de 300 cél./ul.76
En la evoluciĂłn del concepto, las guĂas GESEPOC a partir de la
ediciĂłn 2021 abandonan el concepto de ACOS y detallan que el fenotipo agudizador contiene una forma eosinofĂlica
(antiguo ACOS) y no eosinofĂlica.77 Se definiĂł
como fenotipo agudizaÂdor a todo paciente con EPOC
que presente en el año previo dos o mås agudizaciones ambulatorias, o una o mås
agudizaciones graves, que precisen atenciĂłn hospitalaria. Estas exacerbaciones
deben estar separadas al menos cuatro semanas desde la resoluciĂłn de la
exacerbaciĂłn previa o seis semanas desde el inicio de los sĂntomas para
diferenciar el nuevo evento de una recaĂda o de un fracaso teraÂpĂ©utico,
considerando la eosinofilia como mayor de 300 cé.l/ul.77
Eosinofilia como biomarcador en asma grave y EPOC, y tratamiento
El
eosinófilo como célula estå involucrado en complejas
funciones de la inmunidad innata y adaptativa a infecciones (bacterias, virus,
hongos y parĂĄsitos), e involucrado en la patogĂ©nesis de neoÂplasias y
enfermedades alérgicas.78,
79 Es
una cĂ©lula multifuncional que interactĂșa con variadas cĂ©lulas (linfocitos TH0,
basófilos, endoteliales, macrófagos, plaquetas, fibroblastos y mastocitos), liberando moléculas y mediadores variados, con
propiedades proinflamatorias, citotĂłxicas,
quimioatractivas, proÂadherentes,
regulaciĂłn de la permeabilidad vascular y broncoconstrictoras.23,78-80 Diversos factores afecÂtan la variabilidad del
nĂșmero de eosinĂłfilos en sanÂgre perifĂ©rica, pero
pareciera ser mayor que valores mĂĄs altos, y despreciable con <100
células/uL.80 En EPOC, el
nĂșmero de eosinĂłfilos en sangre perifĂ©rica estĂĄn en
directa relaciĂłn con la magnitud del efecto de los CI sobre la prevenciĂłn de exacerbaciones.23, 80, 82 Por debajo de
100 cĂ©lulas/ul no habrĂa tal efecto. Por arriba de
300 cĂ©lulas/uL serĂa el mayor efecto buscado. Entre
100 y 300 se deben buscar otros predictores de respuesta.23, 80, 82, 83 En los pacientes con exacerbaciones frecuentes,
las GuĂas GOLD sugieren para inicio de tratamiento a los LAMA como monoterapia
para escalar a LAMA/LABA o LABA/ICS.23
Se prefieren estos Ășltimos en pacienÂtes con historia de asma,
una exacerbación grave en el año previo o eosinofilia
mayor de 300/ul.23 Si han tenido
mås de dos exacerbaciones moderadas o uno con hospitalización en el año previo
con mĂĄs de 100 eosinĂłfilos/ul,
pueden ser tratados con ICS/ LABA.23 Los que estĂĄn
tratados con LAMA/LABA y siguen exacerbĂĄndose pueden escalar en caso de tener esos
factores a triple terapia.23 Entre 100 y
300 eosinĂłfilos/ul existen
factores que podrĂan predecir una mejor respuesta a CI como exfumaÂdores,
exacerbadores con corticoides sistémicos, mås de dos
exacerbaciones moderadas o una grave o coexistencia de asma y, por el
contrario, el tabaquista actual, antecedentes de neumonĂa o enfermedades micobacterianas, exacerbaciones tratadas con antibiĂłticos.83
En
otro ejemplo de cĂłmo ambas hipĂłtesis comparten conceptos, existe evidencia
creciente en pacientes con EPOC que el bajo recuento de eosinĂłfilos
estĂĄ asociado a presencia mayor de proÂteobacterias,
especialmente Haemophilus, y mayor
incidencia de infecciones bacterianas y neumonĂa.80
En
el asma grave, se han definido dos patrones fenotĂpicos inflamatorios: T2 alto
(presente en el asma alĂ©rgica y eosinofĂlica) y no
T2, o tambiĂ©n llaÂmado T2 bajo.84,
85 Ambos
fenotipos T2 alto suelen mostrar cierto grado de superposiciĂłn. Los anteÂcedentes
clĂnicos (inicio temprano, antecedentes familiares y personales de enfermedades
atĂłpicas) y la fracciĂłn de Ăłxido nĂtrico exhalado, eosinofilia
e IgE aumentada son buenos biomarcadores
del fenotipo T2 alto. El asma T2 alérgica representa el 40%-50% del asma grave
y tiene una base atĂłÂpica, orquestada por la activaciĂłn de las cĂ©lulas T
colaboradoras tipo 2 (Th2), la producciĂłn de interÂleuquinas
(IL) 4, IL-5 e IL-13 y el cambio de isotipo en los
linfocitos B hacia la producciĂłn de IgE. El asma T2 eosinofĂlica representa mĂĄs del 25% del asma grave. Pueden
asociarse con rinosinusitis crĂłnica y pĂłlipos
nasales. El asma grave con T2 bajo se caracteriza por eosinĂłfilos
bajos en sangre perifĂ©rica y en esputo, con un perfil paucigranuÂlocĂtico
o con neutrofilia, que se puede asociar a limitaciĂłn
crónica del flujo aéreo con atrapamiento y asociación con tabaquismo.86 Se han
desarrollado y comercializado diversos anticuerpos monoclonaÂles para el
fenotipo T2 alto.81 El primer
anticuerpo monoclonal desarrollado para el fenotipo alérgico mediado por IgE fue omalizumab. Luego se han
desarrollado otros biolĂłgicos que suprimen la resÂpuesta eosinofĂlica
en pacientes con asma grave (inhibidores de la IL4, 5 y 13): mepolizumab y resÂlizumab son
inhibidores de la IL 5, benralizumab es inhibidor del
receptor α de la IL 5 y dupilumab inhibidor de
la subunidad α del receptor de IL4 que interfiere la acciĂłn de las IL4 y
IL13.81 En nuestro
paĂs, se comercializan omalizumab, mepolizumab, benralizumab y dupilumab.
A
diferencia del asma, todavĂa no hay comerÂcializado ningĂșn biolĂłgico a raĂz de
los pobres resultados en los estudios clĂnicos vinculados a la existencia del
fenotipo T2 alto en EPOC.23,
87 Tanto
mepolizumab (estudios METREX y METREO), como benralizumab (estudios GALATHEA y TERÂRANOVA), no han
encontrado beneficios clĂnicos significativos. Los estudios con dupilumab estĂĄn en curso. Diferentes biolĂłgicos estĂĄn
siendo ensayados en estudios fase II para la inflamaciĂłn neutrofĂliÂca
no-T2, como anti-IL8, etarnacept e infliximab (anti-FNTalfa), sin
lograr hasta ahora resultados alentadores como para pasar a estudios Fase III.23, 87
CONCLUSIONES
Ambas
hipótesis formuladas hace mås de 60 años, vistas en su origen como posiciones
acadĂ©micamenÂte antagĂłnicas, a la luz de los avances cientĂficos podemos
afirmar varias dĂ©cadas despuĂ©s, que tienen mucha fundamentaciĂłn cientĂfica que
las avalan y, por sobre todo, complementan.39, 86 Pero existen otras consideraciones que
detallan sus inexactitudes a la luz del conocimiento cientĂfico actual, como lo
son en la hipĂłtesis britĂĄnica, que solo consideraron algunos pocos factores
(tabaquisÂmo e infecciones respiratorias) en la gĂ©nesis de la bronquitis
crĂłnica obstructiva. QuizĂĄs el concepto mĂĄs controvertido de la hipĂłtesis
holandesa fue considerar a ambas enfermedades como una evoÂluciĂłn continua, ya
que hay sobrada evidencia en concluir en la mayorĂa de los casos a que corresÂponden
a dos enfermedades diferentes, aunque heterogéneas con sustanciales diferencias
clĂnicas y fisiopatolĂłgicas, sin dejar de considerar que si hay un subgrupo de
pacientes en que se superponen muchos aspectos fisiopatolĂłgicos y clĂnicos, por
lo que algunos autores ya estĂĄn proponiendo para el futuro considerar como mĂĄs
Ăștil, atractivo y provocador en la clasificaciĂłn de enfermedades obstructivas
crĂłnicas, la clasificaciĂłn segĂșn los diferentes endotipos
expresados.88 Lejos de ver
amÂbas hipĂłtesis como modelos teĂłricos antagĂłnicos, el avance en la genĂ©tica
hasta llegar al diagnóstico de un subtipo de origen genético del enfisema y su
traÂtamiento sustitutivo, el entendimiento del impacto del desarrollo neonatal
en la funciĂłn pulmonar del adulto, la exposiciĂłn a la biomasa del medioamÂbiente
y su interacción génica, el microbioma con su
interacción con el huésped y su relación con la fisiopatogenia
de la enfermedades respiratorias y exacerbaciones, el impacto de la
hiperreactividad bronquial e inflamaciĂłn eosinofĂlica
y su potenÂcial impacto en la predicciĂłn de exacerbaciones y del tratamiento de
un subgrupo de pacientes con fenotipo exacerbador, la
metabolĂłmica, son todos buenos motivos para concluir
que, cuando fueron formuladas ambas hipĂłtesis, nadie hubiera imaginado que mĂĄs
de sesenta años despuĂ©s las dos teorĂas tenĂan algo de razĂłn y sirvieron para
entender mejor la génesis del asma y la EPOC.39, 89
Conflicto
de intereses
Conferencias
para actividad de educación médica continua en asma y EPOC para Astra Zeneca, Glaxo
SmithKlane y ELEA.
BIBLIOGRAFĂA
1. Reid L. Pathology of chronic
bronchitis. Lancet. 1954;1:275-
8. https://doi.org/10.1016/S0140-6736(54)91030-2
2. MacLean K H. The histology of generalized emphysema. Australas
Ann Med. 1957;6:124-40. https://doi.org/10.1111/
imj.1957.6.2.124
3. Orie
NGM, Sluiter ID, De Vries
K, Tammeling GJ, Witkop J. The
host factor in bronchitis. In: Bronchitis. N.G.M. Orie,
H.J. Sluiter eds,
Royal Vangorcum, Assen,
1961, pp. 43-59.
4. Orie
NG. Appendix on terminology of bronchitis. In: BronÂchitis
II. N.G.M. Orie, H.J. Sluiter
eds, Royal Vangorcum, Assen, 1964, p. 398.
5. Orie
NGM, Sluiter HJ. Bronchitis: An international symÂposium.1962.
6. Postma
D, Quanjer P. In memoriam Dick Orie. Eur Respir J. 2006;891-2.
https://doi.org/10.1183/09031936.00115706
7. Postma
D, Marike Boezen H.
Rationales for the Dutch Hypothesis: Allergy and Airway Hyperresponsiveness
as genetic factors and their interaction with environÂment in the development
of asthma and COPD. Chest. 2004;126:
96S-104S. https://doi.org/10.1378/chest.126.2_suppl_1.96S
8. Hargreave
FE, Parameswaran K. Asthma, COPD and bronÂchitis are
just components of airway disease. Eur Respir J. 2006; 28: 264-7.
https://doi.org/10.1183/09031936.06.0005 6106
9. Barnes PJ. Against the Dutch
hypothesis: asthma and chronic obstructive pulmonary disease are distinct
diseases. Am J Respir Crit Care Med. 2006; 174: 240-3.
https://doi.org/10.1164/rccm.2604008
10. Kraft M. Asthma and chronic
obstructive pulmonary disÂease exhibit common origins in any country. Am J Respir Crit
Care Med. 2006; 174: 238-40. https://doi.org/10.1164/rccm.2604007
11. Fletcher C, Peto R. The natural history of chronic
airflow obstruction. BMJ. 1977;1:1645-8. https://doi.org/10.1136/bmj.1.6077.1645
12. Gershon
AS, Warner L, Cascagnette P, Victor
JC, To T. Lifetime risk of developing COPD: a longitudinal populaÂtion study. Lancet. 2011;378:991-6.
https://doi.org/10.1016/ S0140-6736(11)60990-2
13. Allinson
JP, Hardy R, Donaldson GC, Shaheen SO, Kuh D, Wedzicha JA. The presence of chronic mucus hypersecreÂtion
across adult life in relation to COPD development. Am J Respir Crit Care Med. 2016;193:662-72. https://doi.org/10.1164/rccm.201511-2210OC
14. Guerra S, Sherrill DL, Venker C, Ceccato CM, Halonn M, Martinez FD: Chronic
bronchitis before age 50 years preÂdicts incident airflow limitation and
mortality risk. Thorax. 2009;64:894-900.
https://doi.org/10.1136/thx.2008.110619
15. Kim V, Han MK, Vance GB, et
al. The chronic bronchiÂtis phenotype of COPD: an analysis of the COPDGene Study. Chest. 2011;140:626-33. https://doi.org/10.1378/chest.10-2948
16. Bridevaux
PO, Gerbase MW, Probst-Hensch
NM, Schindler C, Gaspoz JM, Rochat
T. Long-term decline in lung funcÂtion, utilization of care and quality of life
in modified GOLD 1 COPD. Thorax. 2008;63:768-74. https://doi.org/10.1136/thx.2007.093724
17. Vestbo
J, Prescott E, Lange P, et al. Association of chronic mucus hypersecretation
with FEV1 decline and COPD morbidity. Am J Respir Crit Care Med 1996;153:1530-5.
https://doi.org/10.1164/ajrccm.153.5.8630597
18. Woodruff PG, Barr G, Bleecker E, et al. Clinical signifiÂcance of symptoms in
smokers with preserved pulmonary function. New Engl J
Med. 2016;374:1811-21.
https://doi.org/10.1056/NEJMoa1505971
19. Parekh TM, Bhatia S, Cherrington A, et al. FacÂtors influencing decline in
quality of life in smokers without airflow obstruction: The COPDGene
Study. Respir Med. 2020;161:105820.
https://doi.org/10.1016/j.rmed.2019.105820
20. Higbee
DH, Dodd JW. Prevalence, risk factors and clinical implications of preserved
ratio impaired spirometry. Lancet Respir
Med. 2022;10:149-57. https://doi.org/10.1016/S2213-2600(21)00369-6
21. Sherman CB, Xu X, Speizer FE, Ferris BC,
Weiss ST, DockÂery DW. Longitudinal lung function decline in
subjects with respiratory symptoms. Am Rev Respir
Dis. 1992;146:655-9. https://doi.org/10.1164/ajrccm/146.4.855
22. Lange P, Nyboe
J, Appleyard M, Jensen G, Schnohr
P. Relation of ventilator impairment and of chronic mucus hypersecretion
to mortality from obstructive lung disease and from all causes. Thorax. 1990;45:579-85.
https://doi.org/10.1136/thx.45.8.579
23. Global Initiative for Chronic
Obstructive Lung Disease. Global Strategy for the Diagnosis,
Management and PreÂvention of COPD 2022. Acceso el 18 Septiembre de 2022 en
https://goldcopd.org/2022-gold-reports-2/
24.
SĂvori M, FernĂĄndez R. ClasificaciĂłn de EPOC GOLD
2018: ÂżOtra oportunidad perdida? Rev Amer Med Respir. 2018;2:140-2.
25. Gedenbjerg
A, Szepligeti SK, Holm Wackerhausen
LM, et al. Prediction of mortality in patients with COPD with the new GOLD 2017
classification: a cohort study Lancet Respir Med.
2018;6:204-12. https://doi.org/10.1016/S2213-2600(18)30002-X
26.
SĂvori M, FernĂĄndez R, Toibaro
J, VelĂĄzquez Gortaire E. Supervivencia en una cohorte
de pacientes con EPOC acorde a la clasificaciĂłn GOLD 2017. Medicina Buenos Aires.
2019:79:20-8.
27. Han MK, Ye W, Wang D, et al. Bronchodilators
in tobacco-exposed persons with symptoms and preserved lung function. New Engl J Med. 2022;387:1173-84.
https://doi.org/10.1056/NEJMoa2204752
28. Mannino
D. GOLD Stage 0 COPD: Is it real? Does it matter? Chest.
2006;130:309-10. https://doi.org/10.1016/S0012-3692(15)51839-4
29. Vestbo
J, Lange P. Can GOLD Stage 0 provide information of prognostic value in COPD?
Am J Respir Crit Care Med.
2002;166:329-32. https://doi.org/10.1164/rccm.2112048
30.
Han M, Agusti A, Celli B,
et al. From GOLD 0 to
Pre-COPD. Am J Respir
Crit Care Med. 2021;203:414-23.
https://doi.org/10.1164/rccm.202008-3328PP
31. Rogers GB, Wesselingh S. Precision respiratory medicine and the microbiome. Lancet Respir Med.
2016;4:73-82. https://doi.org/10.1016/S2213-2600(15)00476-2
32. Rogers GB, Shaw D, Marsh R, et al. Respiratory microÂbiota:
addressing clinical questions, informing clinical practice. Thorax.
2015;70:74-81.
https://doi.org/10.1136/thoraxjnl-2014-205826
33. Anonymous editorial. Harnessing the microbiome for lung
health. Lancet Respir Med. 2019:7:827.
https://doi.org/10.1016/S2213-2600(19)30307-8
34. Budden KF, Shukla SD, Rehman SF, et al. Functional effects of the microbiota in chronic respiratory disease. Lancet Respir Med. 2019;7:1-14.
https://doi.org/10.1016/S2213-2600(18)30510-1
35. Toraldo
DM, Conte L. Influence of the lung microbiota dysbiosis in COPD exacerbations: the controversial use of
corticosteroid and antibiotic treatment and the role of eoÂsinophils
as a disease marker. J Clin Med Re. 2019;11:667- 75. https://doi.org/10.14740/jocmr3875205
36. Gloor
GB, Hummelen R, Macklaim
JM, et al. Microbiome profiling by Illumina sequencing of combinatorial sequence-tagged PCR
products. PlosOne. 2010;5:1-15.
https://doi.org/10.1371/journal.pone.0015406
37. Sethi
S, Evans N, Grant BJB, Murphy TF. New strains of bacteria and exacerbations of
COPD: New Engl J Med. 2002;347:465-71.
https://doi.org/10.1056/NEJMoa012561
38. Bafadhel
M, McKenna S, Terry S. et al. Acute exacerbaÂtions of COPD: identification of
biologic clusters and their biomarkers. Am J Respir Crit Care Med. 2011;184:662-71.
https://doi.org/10.1164/rccm.201104-0597OC
39. Rennard
SI. Chronic obstructive pulmonary disease: linkÂing outcomes and pathobiology
of disease modification. Proc Am Thorac
Soc 2006;3(3): 276-80.
https://doi.org/10.1513/pats.200512-129SF
40. Tam A, Din DD. Pathobiologic mechanisms of COPD. Med Clin
N Am. 2012;96:681-98.
https://doi.org/10.1016/j.mcna.2012.04.012
41.
De Marco R, Accordini S, Marcon
A, et al. Risk factors for COPD in a European cohort of young
adults: Am J Respir Crit
Care Med. 2011;183:891-7.
https://doi.org/10.1164/rccm.201007-1125OC
42. Bigna
JJ, kenne AM, Asangbeh SL, Sibetcheu AT. Prevalence
of COPD n the global population with HIV: a systematic reÂview and
meta-analysis. Lancet Glob Health. 2018;6:e193- e202. https://doi.org/10.1016/S2214-109X(17)30451-5
43. Byrne AL, Marais BJ, Mitnick CD, Lecca L, Marks GB.
Tuberculosis and chronic respiratory disease: a systemÂatic review. Int J Infect Dis. 2015;32:138-46.
https://doi.org/10.1016/j.ijid.2014.12.016
44. Soler
Cataluña JJ, MartĂnez GarcĂa
MA, RomĂĄn SĂĄnÂchez P, Salcedo
E, Navarro M, Ochando R. Severe acute exacerbations
and mortality in patients with COPD. Thorax. 2005;60:925-31. https://doi.org/10.1136/thx.2005.040527
45. Donaldson GC, Seemungal TA, Bhowmik A, et al.
RelationÂship between exacerbation frequency and lung function decline in
chronic obstructive pulmonary disease. Thorax. 2002;57:847-52. https://doi.org/10.1136/thorax.57.10.847
46. Spencer S, Calverley PMA, Burge PS: Impact of preventing exacerbations
on deterioration of health status in COPD: Eur Respir J. 2004;23:698-702.
https://doi.org/10.1183/09031936.04.00121404
47.
Hurst JR, Vestbo J, Anzueto A, et al. Susceptibility to exacerbation in chronic obstructive pulmonary disease. N Engl J Med. 2010;363:1128-38.
https://doi.org/10.1056/NEJMoa0909883
48. Postma
D, Kerkhof M, Boezen M, Koppelman G. Asthma and Chronic Obstructive Pulmonary
Disease: common genes, common environments? Am J Respir
Crit Care Med. 2011;183:1588-94.
https://doi.org/10.1164/rccm.201011-1796PP
49.
Kaneko Y, Yatagai Y, Yamada H, et al. The search for comÂmon pathways underlying asthma and COPD. Int J COPD 2013;8:65-78.
https://doi.org/10.2147/COPD.S39617
50. Agusti
A, Hogg J. Update on the pathogenes of ChronÂic
Obstructive Pulmonary Disease. New Engl J Med. 2019;381:1248-56. https://doi.org/10.1056/NEJMra1900475
51. Alder J, Guo
N, Kembou F, et al. Telomere length is a determinant
of emphysema susceptibility. Am J Respir Crit Care Med. 2011;184:904-11.
https://doi.org/10.1164/rccm.201103-0520OC
52. MorlĂĄ
M, Busquets X, Pons J, Sauleda
J, MacNee W, Agusti AGN. Telomere shortening in smokers with and without COPD. Eur Respir J. 2006;27:525-8. https://doi.org/10.1183/09031936.06.00087005
53. Barker DJ, Godfrey KM, Fall
C, Osmond C, Winter Pd, Shaheen
SO. Relation of birth weight and childhood reÂspiratory
infection to adult lung function and death from chronic airways disease.
BMJ. 1991; 303:671-5.
https://doi.org/10.1136/bmj.303.6804.671
54. MartĂnez
F. Early-life origin of Chronic Obstructive PulÂmonary Disease. New Engl J Med. 2016;375;871-8.
https://doi.org/10.1056/NEJMra1603287
55. Lange P, Celli B, AgustĂ A, et al. Lung function trajectoÂries leading to
chronic obstructive pulmonary disease. N Engl J Med.
2015;373:111-22. https://doi.org/10.1056/NEJMoa1411532
56. Boy E, Bruce N, Delgado H.
Birth weight and exposure to kitchen wood smoke during pregnancy in rural
Guatemala. Environ Health Perspect. 2002;110:109-14. https://doi.org/10.1289/ehp.02110109
57. Sunyer
J, Plana E, Dharmage S, Heinrich J, Jarvis D, DeMarco R, Norback D, Raherison C, Villani S, et al. Early life origins of chronic obstructive pulmonary disÂease.
Thorax. 2010;65: 14-20.
https://doi.org/10.1136/thx.2008.112136
58. Postma
DS, de Vries K, Koeter GH, Sluiter HJ. IndepenÂdent influence of
reversibility of air-flow obstruction and nonspecific hyperreactivity
on the long-term course of lung function in chronic air-flow obstruction.
Am Rev Respir Dis. 1986;134:276-80.
59. Sharma S, Tantisira
K, Carey V, Murphy AJ, Lasky-Su J, Celedon JC, Lazarus R, Klanderman
B, Rogers A, Soto- Quiros M, et al. A role for Wnt signaling genes in the
pathoÂgenesis of impaired lung function in asthma. Am J Respir Crit Care Med. 2010;181:328-36. https://doi.org/10.1164/rccm.200907-1009OC
60. AgustĂ
A, Noell G, Brugada J, Faner R. Lung function in early adulthood and health in
later life: a transgeneratio cohort analysis. Lancet Respir Med. 2017; 5:935-45.
https://doi.org/10.1016/S2213-2600(17)30434-4
61. AgustĂ
A, Faner R. Lung function trajectories in health and
disease. Lancet Respir Med. 2019;7:358-64.
https://doi.org/10.1016/S2213-2600(18)30529-0
62.
Juneman A, Legarreta G.
Inhalación de humo de leña: una causa relevante pero poco reconocida de EPOC. Rev Arg Med
Respir. 2007;2:51-7.
63.
Silva R, Oyarzun M, Olloquepui J.et al. Mecanismos paÂtogĂ©nicos
en la EPOC causada por exposiciĂłn a humo de biomasa.Arch
Bronconeumol. 2015;51:285-92.
https://doi.org/10.1016/j.arbres.2014.10.005
64.
Torres Duque CA, GarcĂa RodrĂguez MC, GonzĂĄlez GarcĂa;.
EPOC por humo de leña: ¿un fenotipo deiferente o una
entidad distinta? Arch Bronconeumol.
2016;52:425-31.
https://doi.org/10.1016/j.arbres.2016.04.004
65.
Menezes AM, PĂ©rez Padilla R, Jardim
JR, et al. COPD in five Latin American cities (the PLATINO
Study): a prevalence study. Lancet. 2005;365:1875-81. https://doi.org/10.1016/S0140-6736(05)67632-5
66.
Echazarreta A, Arias S, del Olmo R, et al.
Prevalencia de EPOC en 6 aglomerados urbanos de Argentina: el estudio EPOC.AR. Arch Bronconeumol. 2018;54:260-9. https://doi.org/10.1016/j.arbres.2017.09.018
67.
Thurston G. Balmes JR, Garcia E, et al. Outdoor air pollution and new onset airway disease: An Official American
Thoracic Society Workshop Report. Ann Am Thorac Soc.
2020;17:397-98.
https://doi.org/10.1513/AnnalsATS.202001-046ST
68. Silva GE, Sherrill DL, Guerra
S, Barbee RA: Asthma as a risk factor for COPD in a longitudinal study. Chest. 2004;126:59-65.
https://doi.org/10.1378/chest.126.1.59
69. McGeachie
MJ, Yates KP, Zhou X, et al. Patterns of growth and decline in lung function in
persistent childhood asthma. N Engl J Med. 2016;374:1842-52. https://doi.org/10.1056/NEJMoa1513737
70. Hospers JJ, Postma DS, Rijcken B, et al.
Histamine airway hyperresponsiveness and mortality
from chronic obstructive pulmonary disease: a cohort study. Lancet.
2000;356:1313- 7. https://doi.org/10.1016/S0140-6736(00)02815-4
71. Rijcken
B, Schouten JP, Weiss ST, Speizer FE, Van der Lende R. The relationship of nonspecific
bronchial response to respiratory symptoms in a random population sample.
Am Rev Respir Dise.
1987;136:62-8. https://doi.org/10.1164/ajrccm/136.1.62
72. Tashkin
DP, Altose MD, Connett JE,
et al. Methacholine reactivity predicts changes in
lung function over time in smokers with early chronic obstructive pulmonary
disease. The Lung Health Study Research Group. Am J Respir Crit Care Med. 1996;153:1802-11. https://doi.org/10.1164/ajrccm.153.6.8665038
73.
Soler-Cataluna JJ, CosĂo B, Izquierdo JL,
LĂłpez-Campos JL, MarĂn JM, AgĂŒero R, et al. Documento de consenso sobre el
fenotipo mixto EPOC-asma en la EPOC. Arch Bronconeumol. 2012;48:331-7.
https://doi.org/10.1016/j.arbres.2011.12.009
74.
Miravitlles M, Soler Cataluña JJ, Calle M, et al.
GuĂa espaÂñola de la EPOC (GesEPOC) Tratamiento
farmacolĂłgico de la EPOC estable. Arch Bronconeumol. 2012;48:247-57. https://doi.org/10.1016/j.arbres.2012.04.001
75. Global Strategy for Asthma
Management and PrevenÂtion, Global Initiative for Asthma (GINA). Diagnosis of
Asthma, COPD and Asthma-COPD overlap syndrome (ACOS). 2015. Global Initiative for Asthma website. Acceso el 27 de
Septiembre de 2022 en http://www.ginÂasthma.org/.
76.
Sin JD, Miravitlles M, Mannino
DM, et al. What is asthma- COPD overlap syndrome? Towards a consensus definition from a around table discussion. Eur
Respir J. 2016;48:664- 73.
https://doi.org/10.1183/13993003.00436-2016
77.
Miravitlles M, Calle M, Molina J, et al.
ActualizaciĂłn de la GuĂa Española de la EPOC (GesEPOC).Tratamiento
farmacolĂłgico. Arch Bronconeumol. 2022;58:69-81.
https://doi.org/10.1016/j.arbres.2021.03.005
78. Asano K, Ueki S, Tamari M, et
al. Adult-onset eosinoÂphilic airway diseases. Allergy. 2020;75:3087-99.
https://doi.org/10.1111/all.14620
79. Tefferi
A. Blood eosinophilia: a new paradigm in disÂease, classification, diagnosis
and treatment. Mayo
Clin Proc. 2005;80:75-83. https://doi.org/10.1016/S0025-6196(11)62962-5
80.
Singh D, AgustĂ A, MartĂnez F, et al. Blood eosinophils and COPD: A Global Initiative for Chronic
Obstructive Lung Disease Science Committee: 2022 review. Am J Respir Crit Care Med. 2022;206:17-24. https://doi.org/10.1164/rccm.202201-0209PP
81.
SĂvori M, Pascansky D. Asma
grave T2 alto: anĂĄlisis del diseño de los estudios clĂnicos de los nuevos
biolĂłgicos. Rev Am Med Respir. 2022;1:98-115.
82. Mycroft K, Krenke R. Eosinophils in
COPD-Current concepts and clinical implications. J Allergy Clin ImÂmunol Pract.
2020;8:2565-74.
https://doi.org/10.1016/j.jaip.2020.03.017
83. Stolz
D, Miravitlles M. The right treatment for the right
paÂtient with COPD: lessons from the IMPACT trial. Eur
Respir J. 2020;55:2000881https://doi.org/10.1183/13993003.00881-2020
84. Edris
A, De Feyter S, Maes T, Joos G, Lahousse L. MonoÂclonal
antibodies in type 2 asthma: systematic review and network meta-analysis. Respiratory Research. 2019; 20: 179.
https://doi.org/10.1186/s12931-019-1138-3
85. Agache
I, Beltran J, Akdis C, et al. Efficacy and safety of
treatment with biologics (benralizumab, dupilumab, mepolizumab, omalizumab and reslizumab) for
severe eosinophilic asthma. Allergy.
2020;75:1023-42. https://doi.org/10.1111/all.14221
86. Kuo
CS, Pavlidis S, Loza M, Baribaud F, Rowe A, Pandis I, et
al; U-BIOPRED Study Group. T-helper cell type 2 (Th2) and non-Th2 molecular
phenotypes of asthma using sputum tranÂscriptomics in
U-BIOPRED. Eur Respir J.
2017;49:1602135. https://doi.org/10.1183/13993003.02135-2016
87. Donovan T, Milan SJ, Wang R, Bancho E, Bradley P, Crossingham
I. Anti-IL-5 therapies for chronic obstrucÂtive pulmonary disease. Cochrane
Database Sys Rev. 2020;12:CD013432.
https://doi.org/10.1002/14651858.CD013432.pub2
88. Soler
X, Ramsdell JW. Are asthma and COPD a continuum of
the same disease? J All Clin Immunol Pract. 2015; 489- 95. https://doi.org/10.1016/j.jaip.2015.05.030
89.
Ghebe M, Bafadhel M, Desai D, et al. Biological
clustering supports both ââDutchââ and ââBritishââ hypotheses of asthma and
chronic obstructive pulmonary disease. J Allergy Clin Immunol. 2015;135:63-72. https://doi.org/10.1016/j.jaci.2014.06.035