Autor : Pascansky, Daniel1-2, SĂvori, MartĂn1-2, Capelli, Luciano1-2
1 Unidad de NeumotisiologĂa, Hospital de Agudos Dr. J. M. Ramos MejĂa, Ciudad AutĂłnoma de Buenos Aires 2Centro Universitario NeumonologĂa Dr. J. M. Ramos MejĂa. Facultad de Medicina, Universidad de Buenos Aires. Argentina.
https://doi.org./10.56538/ramr.LYBB1788
Correspondencia : Daniel Pascansky, Unidad de NeumotisiologĂa, Hospital General de Agudos Dr. J. M. Ramos MejĂa, Urquiza 609, 1221 Buenos Aires, Argentina e-mail: vdpascan@gmail.com
RESUMEN
No existe información sobre la estructura y costos
anuales de una hospitalización por agudización de la EPOC en
nuestro país actualmente
Objetivos: Determinar la estructura de costos de los pacientes hospitalizados por EPOC
reagudizada en un hospital público de la Ciudad Autónoma de
Buenos Aires (CABA) en el año 2018.
Materiales y métodos: Se evaluaron pacientes con EPOC reagudizada (GOLD), inÂternados durante
2018 en nuestro hospital. Se determinaron costos directos (perspecÂtiva del
financiador), según costos de medicamentos y la modulación de
internación clínica y Unidad de Terapia Intensiva (UTI) del
Gobierno de CABA a junio de 2021, valor dólar Banco Nación al 30
de Junio 2021 de $101,17.
Resultados: Se internaron 26 pacientes, edad 64 ± 9,56 años, masculino 73%, 61%
tabaquistas actuales y 39% extabaquistas (101,8 ±
47,1 paq.-año), seguro social 31%, FEV1% 31 mediana
(23-42) y FEV1/FVC
0,46 ± 0,12. La duración de internación fue: guardia 1 d
(1-1,75); piso, 9 d (4-12); y UTI, 13 d (11-29,5), con mortalidad 23% (n =
6).
El costo final fue 1462,62 dólares/paciente,
mediana (RIQ 25%-75%,763,85-2915,95), 162,44
dólares/d/paciente, y el costo total (n = 26) fue USD 117 480. El
costo de UTI fue 9898,28 dólares/paciente, mediana (RIQ 25%-75%,
6700,94-35 780,25). El costo total (n = 3) fue USD 75 064,11.
Conclusión: Los pacientes con EPOC reagudizada que se hospitalizan son en su
mayoría hombres, más de 60 años, alta carga
tabáquica y obstrucción grave. El costo directo desde la
perspectiva del financiador fue de USD 1462 por paciente; el costo del paciente
que se hospitaliza en UTI fue casi siete veces superior. Se deben instruÂmentar
programas sistematizados de manejo de la EPOC para identificar pacientes con
factores de riesgo, educar y permitir acceso a la medicación.
Palabras claves: EPOC, Exacerbaciones, Hospitalizaciones, Costo directo, Gastos
ABSTRACT
There is not information about
the annual and structure of costs of a hospitalization of COPD exacerbation in
our country actually.
Objective: To determine the structure of direct costs in hospitalized patients due
to COPD exacerbations in a public hospital of Buenos Aires in 2018.
Methods: Patients hospitalized of COPD exacerbation (GOLD) in 2018 were analyzed
in our hospital. Direct costs were determined (financier perspective), due to
modulation of the Health Ministry of Buenos Aires City Government, stratified
by Intensive Care Unit hospitalization and in room at June 2021, in dollars
(dol.), parity at June 30th 2021 was 1 dollar = 101,17$ (price Banco
Nación).
Results: 26 patients were hospitalized: age 64 ± 9.56 years, male gender 73%, 61%
actual smokers and 39% ex-smokers (101.8 ± 47.1 pack-y, social health assurance
31% (n = 8); FEV1%
31 median (23-42) and FEV1/FVC
0,46 ± 0,12. Ward length of hospitalization (median) was 1 day (1-1,75), 9 days
in room (4-12), 13 days in UCI (11- 29,5) with mortality rate 23% (n = 6).
Final direct cost by patient was
1462,62 dol, median (IQR 25%-75%,763,85-2915,95),at 162,44 dol./day/patient.
Total cost (n = 26) was 117 480 dol. UCI cost was median 9898,28
dol./patient (IQR 25%-75%, 6700,94-35 780,25). Final UCI total cost (n =
3) 75 942,3 dol.
Conclusion: Patients with COPD exacerbation hospitalized were mainly males, sixty
years old, heavy smokers and severe airway obstruction. With financier
perspective, direct cost of hospitalization was 1462 dol./patient, almost seven
times higher in UCI. Disease management program must be implemented to manage
COPD, to identify patients at risk, to educate and to assure access to drugs.
Key words: COPD, Exacerbations, Hospitalizations, Costs, Expense
Recibido: 02/05/2022
Aceptado: 03/11/2022
La Enfermedad Pulmonar Obstructiva Crónica (EPOC)
es un gran problema de Salud Pública debido a que existe creciente
evidencia del auÂmento de diferentes parámetros epidemiológicos
de preocupación.1 El tabaquismo
es la principal causa de EPOC.2,
3 La
prevalencia de tabaquismo ha ido descendiendo desde tasas cercanas al 40% a
principios de este siglo hasta valores cercanos al 22% de la población
general según la Encuesta Nacional de Salud de nuestro país.4 La edad de
comienzo del tabaquismo en nuestro país es de 14 años, la edad de
consumo regular es de 18 años y se observa una tendencia al aumento del
consumo, particularmente en los sectores de personas jóveÂnes y de
escasos recursos.2,
4 Claramente
la cesación tabáquica sigue siendo la principal
intervención terapéutica que mejora la morbimortalidad.2, 3 Es importante
destacar el subdiagnóstico reflejado en varios
estudios europeos, que es de alrededor del 75% del total de pacientes con EPOC.5-7 En el
estudio PLATINO de cinco ciudades de LatiÂnoamérica, el 82% de los
pacientes con EPOC, desconocían que padecían esta enfermedad y en
el estudio de prevalencia argentino EPOC.AR fue del 77,4%.8, 9 La prevalencia de la EPOC en la
población general urbana en la Argentina es del 14,3%, pero en una
muestra poblacional de más de 40 años con exposición al
tabaco (estudio PUMA) es mayor (29,6%), por lo que se estimaría entre
2,5 y 3 millones de pacientes con EPOC.10
Con respecto a la mortalidad, según la OMS,
continúa siendo la tercera causa de muerte, y el 80% de estas se
produce en países de bajos o medianos recursos.11
Estudios preliminares acerca de mortalidad por EPOC en nuestro
país, demuestran un crecimiento del 112% con respecto a 1980 y llega, en
1998, a casi 27 muertes por 100 000 habitantes, aproximaÂdamente 5000 muertos,
especialmente en el sexo femenino.12 Recientemente,
el Instituto Nacional de Epidemiología Respiratoria Emilio Coni informó aproximadamente 30 000
hospitalizaciones anuales en parte del sector público en el año
2015.13
Con respecto a la morbilidad, la EPOC es la quinta causa
de internación hospitalaria en la ArÂgentina en mayores de 60
años.3 En Estados
Unidos de Norteamérica se han incrementado entre 1978 y 1994 las
internaciones hospitalarias de 259 000 a 500 000 por año, especialmente
en mayores de 65 años.15 Como
enfermedad incapacitante, la EPOC se incrementará en el mundo desde el
actual puesto 12.° al 5.° puesto.16 El costo
creciente de las enferÂmedades crónicas ha requerido que se estudie el
impacto de las enfermedades en el sistema de salud, la estructura de costos y
los abordajes tendientes a optimizar el sistema, dado que la demanda es siempre
mayor y está insatisfecha y los costos en salud van creciendo año
a año. La progresiva proÂlongación de la esperanza de vida, el
uso de técnicas diagnósticas cada vez más onerosas y
tratamientos más caros ha debido ponderarse en relación al ahorro
que generan en la reducción del consumo de recursos de salud, el aumento
de la sobrevida y la mejoría en los diferentes marcadores de salud, como
la calidad de vida.16-22 El Instituto
Nacional de Salud (NHLBI) de Estados Unidos reconoció un gasto de USD 23
900 millones por la EPOC, el 61,5% por costos directos. El costo por persona
fue de USD 1522 por persona por año, un costo tres veces mayor que el de
asma y 2,5 veces mayor que los no-EPOC.15, 21 Los mayores costos fueron los directos por
hospitalización y visitas de emergencia a guardia (72,8%).22 También
Guest y cols., en un estudio sobre costos en enfisema
en Gran Bretaña del Instituto Nacional de Salud del Reino Unido,
determinó un gasto de ÂŁ 19 millones (aproximaÂdamente USD 34 millones)
para tratar 134 000 reagudizaciones por enfisema (costos directos): un 50% por
costos hospitalarios para tratar el 3% de las reagudizaciones totales.23 El promedio
del costo por internación fue de USD 3600 versus USD 128 en las
reagudizaciones tratadas ambulatoriamente. Debido a ello, se han elaborado estrategias
para reducir el número de internaciones y su duración.23, 24 El promedio
de estadía hospitalaria fue de 9,9 d. La estimación promedio por
internación fue de ÂŁ 3000 (USD 5700) en contraste con las ÂŁ 100 (USD
190) de costo por tratarlas ambulatoriamente.24
Existen otras múltiples publicaciones europeas y
estadounidenses recientemente presentadas, acerca de la estructura de costo en
la EPOC, pero todas con el denominador común del alto porcentaje de la
hospitalización por la reagudización y la oxigeÂnoterapia, que
incide gravemente en el costo total de esta enfermedad.25-44
En la Argentina, existe solo una publicación de
hace veinte años atrás acerca del impacto en los costos directos
de las hospitalizaciones por EPOC reagudizada, de 33 pacientes en el año
1999 en un hospital público del Gobierno de la Ciudad de Buenos Aires.36 El costo por
egreso fue de USD 2451, con un promedio de estadía de 15 d, a costo de
USD 163 por día de internación.36
El objetivo de este estudio es describir el costo directo
por hospitalización de una reagudización de EPOC y determinar la
estructura en un hosÂpital público de la Ciudad de Buenos Aires en el
año 2018.
MATERIAL Y MÉTODOS
Se revisaron las historias clínicas de pacientes
internados por EPOC reagudizada en todas las áreas del Hospital General
de Agudos Dr. J. M. Ramos Mejía de la Ciudad Autónoma de Buenos
Aires (CABA) desde el 1 de enero de 2018 al 31 de diciembre de 2018. Se
incluyeron adultos mayores de 18 años. Pacientes con EPOC
(definición GOLD: relación FEV1/FVC < 0,70 y FEV1 < 80%
predicho posbroncodilatador2),
mayores de 40 años, con antecedentes de tabaquismo por cigarrillo mayor
de 20 paquetes-año. Se excluyeron pacientes con antecedentes de otras
enfermedades respiratorias.
Se determinaron los costos directos desde la perspectiva
del financiador, teniendo en cuenta los costos de medicaÂmentos y la
modulación de internación clínica y unidad de terapia
intensiva (UTI) del Gobierno de la Ciudad de Buenos Aires (GCBA) a junio 2021.
El valor de la moduÂlación del Gobierno de la Ciudad de Buenos Aires
para los hospitales públicos a junio 2021 era de ARS 14 143 (USD 139)
para la internación en piso por paciente y por día; en guardia no
crítica, ARS 2957 (USD 30); guardia con estudios, ARS 5231 (USD 51,5); guardia
crítica, ARS 33 070 (USD 325); en UTI, sin asistencia respiratoria
mecánica (ARM), ARS 29 527 (USD 290); y con ARM, ARS 33 070 (USD 325)
por paciente y por día.45
Dentro de cada módulo ya estaba preestablecido determinado
número y tipo de prestaciones (bioquímica, imágenes,
electrocardioÂgrama, espirometría, ARM,
oxígeno, material descartable, medicamentos, etc., además de la
alícuota dependiente de sueldos, impuestos y tasas, cargos
administrativos, amorÂtizaciones de equipos, costos de alimentación y
lavandería, etc.). Cuando se realizó una consulta o
práctica diagnósÂtica adicional o se utilizó algún
tratamiento (por ejemplo, medicamentos) por fuera de lo modulado, se
determinó el costo desde la perspectiva del financiador según
vademéÂcum farmacéutico KAIROS y listado de prestaciones en el
nomenclador del GCBA.46
Debido a la variación de la paridad peso/dólar, se
informarán los resultados en dólares. La paridad cambiaria para
el cálculo del costo en dólares que se usó fue al cambio
oficial del Banco Nación al 30 de junio de 2021 ($ 101,17 = USD 1).
El valor de eosinofilia
obtenido fue previo a la admiÂnistración de corticoides
sistémicos en el laboratorio de la guardia.
La espirometría se
realizó en el último día de hospitaliÂzación antes
del alta hospitalaria.
Se empleó estadística descriptiva. Para las
variables cuantitativas por su distribución no gaussiana, se
utilizó la mediana como medida central y el rango intercuartilar
25%-75% (RIQ 25%-75%) como medida de dispersión. Para que tuvieran
distribución gaussiana, se utilizó la media como medida central y
la desviación estándar como medida de dispersión, y, para
las variables cualitativas, el porcentaje.
RESULTADOS
Durante el año 2018 se internaron 26 pacientes; de
ellos, 23 en sala y 3 en UTI. Las características demográficas se
presentan en la Tabla 1.
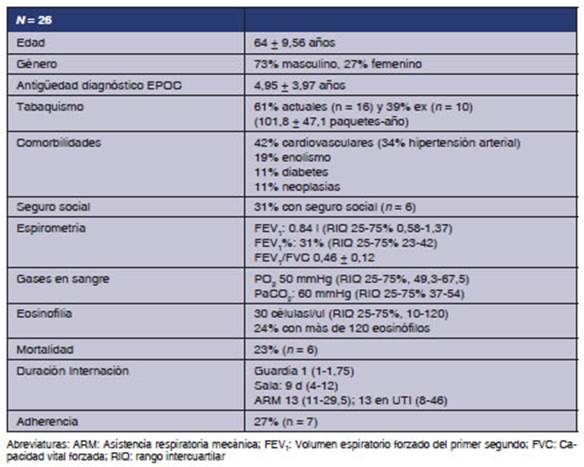
La mayor parte (n = 18 pacientes [70%]) perteÂnecían
al área programática del hospital. Del total, solo eran
atendidos en nuestro hospital el 38,6% (n = 10) antes de su consulta. La
adherencia al seÂguimiento antes de la internación fue pobre (27%).
Al ingreso, el 50% (n = 13) estaban en trataÂmiento
con broncodilatadores de acción corta beta 2 adrenérgicos; el 23%
(n = 6), con asociación de broncodilatadores de acción
corta beta 2 adreÂnérgicos y anticolinérgicos; el 15% (n =
4), con asociación de broncodilatadores de acción larga beta 2
adrenérgicos y corticoides inhalados; y el 11% (n = 3), con
broncodilatador de acción larga anticolinérgico. No hubo
pacientes tratados con triple terapia.
De los 26 pacientes, tres de ellos se internaron dos
veces (11,5%).
Análisis de costo directo
El costo final directo por paciente hospitalizado en sala
fue de USD 1462,62 (RIQ 25%-75%, 763,85- 2915,95), lo que, llevado a los 26
pacientes que se internaron, el costo total directo fue de USD 117 480, esto es
USD 162,44 por día por paciente.
El costo final directo por paciente hospitalizaÂdo en UTI
fue de USD 9898,28 (RIQ 25%-75%, 6700,94-35 780,25). Teniendo en cuenta que
solo tres pacientes se internaron en UTI, hubo una importante dispersión
del costo total directo por paciente. El total de lo gastado para tres
pacientes fue de USD 75 064,11.
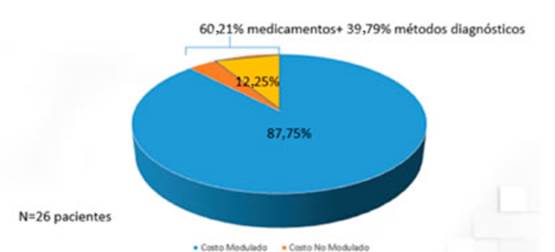
Con respecto a la estructura del costo directo, el 87,75%
de este había sido considerado dentro del módulo clínico
del GCBA. Sin embargo, del resto (12,25%), el 60,21% fue por medicamentos no
conÂsiderados en el módulo; y el 39,8%, por prácticas
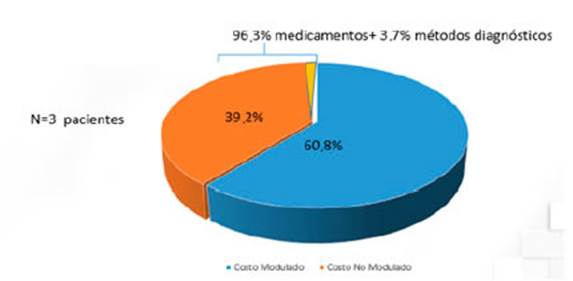
diagnósticas no moduladas (Figura 1). En cambio, si se considera la
internación en UTI, el 39,2% del costo directo fue no modulado
(más de tres veces que el paciente internado en sala). El costo por medicamentos (antibióticos especialmente) fue la
principal causa (96,3%) del costo no modulado directo (Figura 2).
DISCUSIÓN
Se ha determinado el costo directo de hospitalizaÂción
por EPOC reagudizada en un hospital público de la Ciudad Autónoma
de Buenos Aires. En una muestra fue de 26 pacientes, mayoritariamente
masculinos en la séptima década de la vida, con enfermedad
recientemente diagnosticada y alta carga tabáquica como
obstrucción grave al flujo aéreo. El costo en sala general fue de
USD 1462 por paciente y casi siete veces más que en interÂnación
de UTI. Los pacientes internados en sala entraban dentro del módulo
previsto de costo, mientras que los de UTI tenían un porcentaje mayor
por fuera de él, debido al uso de medicaÂmentos de alto costo. El perfil
de tratamiento farmacológico de la mayoría de los pacientes de
hospitales públicos de CABA se encuentra por fueÂra de las recomendaciones
de las guías actuales, ya que, fundamentalmente, se basa en el uso de
broncodilatadores de acción corta, con seguridad, por dificultad en el
acceso a la medicación y la pobre adherencia en el seguimiento.
Para la Unión Europea, los costos directos
totales anuales de las enfermedades respiratorias son el 6% del presupuesto
total en salud; la EPOC explica el 56% de ellos (38 600 millones de euros).2, 47
En EsÂtados Unidos, se estiman los costos directos totales
anuales por EPOC en USD 29 500 millones y los inÂdirectos, USD 20 400 millones
.2, 48 De ellos, la mayor
proporción es por la atención de las exacerbaciones de EPOC, lo
que determina una relación directa con la gravedad de la enfermedad.
Probablemente, en los países subdesarrollados el costo indirecto sea
mayor que el impacto negativo en el directo.2,
36-43
Como la mortalidad ofrece solo una limitada
perspectiva del impacto de una enfermedad sobre el ser humano, Murray y cols.
diseñaron un indiÂcador DALY (Disability-Adjusted
Life Year) estuÂdiado
en el Global Burden of Disease
Study, que es para una enfermedad determinada la
suma de años perdidos por muerte prematura ajustados por la gravedad de
la enfermedad y el deterioro concoÂmitante de la calidad de vida vivida.49 Así, la EPOC en 2005
fue la octava causa de DALY perdidos en el mundo y se estimó que en el
2013 fue la quinta enfermedad en mundial, pero segunda en Estados Unidos luego
de la enfermedad coronaria.49
Las Guías Españolas del
Manejo de Asma (GEMA) han determinado los diferentes compoÂnentes del costo
directo e indirecto del asma en salud, pero que se puede extrapolar a otra
enferÂmedad obstructiva crónica, como la EPOC. Relatan cuarenta y siete
características recomendables que utilizar en la realización de
un estudio de costos (Tabla 2).50 Este estudio cumple con esas
recomenÂdaciones. Se ha usado una metodología mixta para determinar los
costos directos: modulación de los costos provistos por el GCBA
(método top-down) y, además de
la revisión de cada historia clínica, costeando los consumos del
paciente por fuera de la modulación (método botton
-up). En nuestro esÂtudio, se han recolectados datos primarios directos de
la historia clínica, lo que constituye un detalle de valor.50
Como ya se ha comentado, hemos reaÂlizado el estudio de costos
desde la perspectiva del financiador (GCBA) en el ámbito de un hospital
público general de agudos, por lo que sus concluÂsiones solo se
podrían extrapolar a ese sistema de salud. La comparación de
costos entre los países o la extrapolación directa no se
aconsejan, pues su estructura varía de país en país por
sistemas de salud y estructura de costos diferentes, aunque nos puede dar una
idea de la magnitud del problema y del peso cualitativo de cada variable.50

Bilde y cols. publicaron un estudio del gasto per
cápita del Medicare en el que se comparan los pacientes EPOC con los
no-EPOC. Determinaron que el gasto fue de USD 8482 versus USD 3511 (2,5 veces
superior). El 50% del gasto en EPOC se consume en el 10% de los pacientes.51
Otros autoÂres han comunicado el impacto económico de la
EPOC sobre el Sistema de Salud Norteamericano. El promedio de días/cama
fue de 7,75 d, pero con mayores tasas de reinternaciones
y mayores gasÂtos. El gasto medio fue de USD 6469 por paciente (costos
directos); de los cuales, el 68% de ellos se debieron a hospitalizaciones.48, 52
Ya se relató que el Instituto Nacional de Salud (NHLBI) de
Estados Unidos reconoció un gasto para la EPOC de USD 23 900 millones;
de los cuales, 14,7 mil millones fueron costos directos (61,5%) y 9,2 por
indirectos (38,5%). El costo por persona fue de USD 1522 por año, un
costo tres veces mayor que el de asma y 2,5 veces mayor que los pacientes
no-EPOC.15, 21 El índice
de internación fue de 21,2 pacientes por cada 1000 personas. Los mayores costos directos fueron por
hospitalización y visitas de emergencia a guardia (72,8%). El resto se
dividió: el 15% en visitas ambulatorias y el 12,2% por costo de drogas.
Pero la distribución del gasto en EPOC fue muy desproporcionada: el 10%
de los pacientes gastaron el 73% del total de gastos.15, 21 El aumento de interÂnaciones se observó
en mayores de 45 años. En el informe del NHLBI, dentro de las
enfermedades respiratorias, se compara la distribución de los costos
directos e indirectos de la EPOC en relación con el asma, influenza,
neumonía, tuberculosis y cáncer de pulmón.15
La EPOC gasta el doble que el asma y, comparada con influenza,
cáncer de pulmón o neumonía, presenta mayor
proporción de gastos directos.15
Guest y cols., en el primer estudio
sobre costos en enfisema de Gran Bretaña, del Instituto Nacional de
Salud del Reino Unido, se determinó un gasto de ÂŁ 19 millones
(aproximadaÂmente USD 34 millones) para tratar 134 000 reaÂgudizaciones por
enfisema (costos directos): el 50% por costos hospitalarios para tratar el 3%
de las reagudizaciones totales.23 El costo por
internación promedio fue de USD 3600 versus USD 128 en las
reagudizaciones tratadas ambulatoriamente. Ello ha permitido elaborar
estrategias para reducir el número de internaciones y su
duración.17
NuevaÂmente, Guest y cols. realizaron
un estudio similar al anterior, pero teniendo en cuenta los costos de EPOC en
general en el Sistema Nacional de Salud del Reino Unido. Se determinó un
gasto de ÂŁ 817,5 millones (USD 1553 millones aproximadamente) solo de costos
directos.24 Esto
equivale a ÂŁ 1154 por persona por año, alrededor de USD 2300 por persona
por año.24
El promedio de estadía fue de 9,9 d. Los costos
hospitalarios fueron el 35% del total para tratar menos del 2% de las reagudizaÂciones.24 La
estimación promedio por internación fue de ÂŁ 3000 (USD 5700) en
contraste con las ÂŁ 100 (USD 190) de tratarlas ambulatoriamente.24 Probablemente,
este análisis subestima el costo real para la sociedad pues no
están considerados los costos indirectos (pérdida de
productividad, ya que la EPOC tiene 6 veces más ausentismo laboral que
el asma), los costos directos para el paciente (viajes), ni los intangibles
(calidad de vida). Si se analiza la distribución de gastos direcÂtos en
el Reino Unido, el 47,5% fue para compra de medicamentos; el 24,5%, para
oxigenoterapia domiciliaria; el 17,8%, aranceles hospitalarios; y el 10,2%,
honorarios ambulatorios médicos.23, 24
Con respecto a la hospitalización de la EPOC en la
Argentina, el Instituto Nacional de EpiÂdemiología de Enfermedades
Respiratorias Dr. Emilio Coni ha comunicado que en el
año 2015 se determinaron casi 30 500 hospitalizaciones por EPOC
reagudizada en una muestra que incluye instituciones públicas del
país.13 En el GCBA,
en el año 2013, hubo 1066 internaciones y, en 2014, 996
hospitalizaciones por EPOC reagudizada.53
En el estudio anterior de costos en pacientes con EPOC
reagudizado hace veinte años atrás, para 33 pacientes, el costo
directo total por paciente por internación fue de USD 2451. La
estructura del costo hospitalario se distribuyó de la siguiente manera:
costos de atención final constituyeron el 75% del costo total; el 57% de
estos correspondió a sueldos (el 17,55%, médicos; el 37,41%,
enferÂmería; y el 1,51%, administrativos) y el 13%, a medicamentos,
descartables y prácticas médicas (medicamentos: 8,8% del total).36 El 25%
restante se debió a la transferencia de costos de otros serÂvicios y
servicios generales, con 12,48% de gasto en personal.36
El día de internación fue de USD 163, que es igual
al costo del día de internación del estudio actual (USD 162), es
decir que permaneció estable a lo largo de dos décadas. Cabe
aclarar que la oxigenoterapia brindada en la guardia, sala geneÂral y UTI
representa un alto costo hospitalario en todos los estudios de costos de la
enfermedad. En nuestro caso, se encuentra considerado dentro del módulo
de internación como también con respecto al uso de
ventilación invasiva y no invasiva dentro del módulo de UTI. A la
fecha de realización del estudio, no teníamos disponibilidad de
cánula de alto flujo de oxígeno.
Con respecto al promedio de días de
internación de nuestro estudio actual, ha disminuido a 9 d, que es mucho
menor que el promediado en nuestra misma institución veinte años
atrás (15 d). Ahora, es similar al publicado internacionalmente (9,9 d)
en Gran Bretaña y 7,75 d en Estados Unidos.22-24, 36 Una posible explicación es que la normatización del tratamiento y la permanente
educación del persoÂnal de salud en nuestra institución para el
manejo adecuado y actualizado del paciente con EPOC, a la vez que la
disponibilidad de tratamientos farÂmacológicos más efectivos ha
permitido disminuir de manera significativa la estancia hospitalaria.
Diferentes guías internacionales (GOLD, ALAT, GESEPOC y otras), y la del
Ministerio de Salud de nuestro país resumen las recomendaciones para el
efectivo manejo de la EPOC, donde la terapia con broncodilatadores es la piedra
angular.2, 3, 54, 55
Tanto las guías internacionales como la nacional
identifican un grupo de pacientes que comparte como antecedente el haber tenido
una hospitaliÂzación en el año previo o más de una exacerbación
ambulatoria que requirió antibióticos o corticoides
sistémicos (GRUPOS E de las guías GOLD). Dado el peor
pronóstico de los pacientes que han sufrido exacerbaciones frecuentes en
mayor deterioro de la función pulmonar, síntomas, calidad de vida
y mortalidad, el fenotipo exacerbador frecuente es
reconocido como factor de riesgo de peor pronósÂtico por todas las
guías y ameritan un tratamiento más intensivo y con el uso
incluso de corticoides inhalados. 2,
3, 54-57
Otros factores reconocidos como riesgo de hospitalizaciones en
EPOC son la difiÂcultad de acceso al tratamiento farmacológico, la falta
de adherencia, los errores de inhalación y las comorbilidades.2, 3, 54, 55 En nuestro
estudio, solo 10% de los pacientes tenían seguro social. También
la alta prevalencia de errores de administración de los medicamentos
inhalados de los pacientes con enfermedades obstructivas crónica, como
el asma y la EPOC, es reconocida en todo el mundo.58 Usmani y cols.
determinó que la edad avanzada, el bajo nivel socioeconómico y
educativo, la falta de instrucción previa de la correcta inhaloterapia y la presencia de comorbilidades fueron los
factores asociados a error en la técnica de administración y, por
lo tanto, asociado a mal control del asma y aumento del consumo de recursos de
salud.59 Con
respecto a las comorbilidades, fueron muy prevaÂlentes en nuestro estudio
(Tabla 1), y se reconoce que inciden en el peor pronóstico de la
enfermedad, tanto en el fenotipo exacerbador (grupo
E) como en el no exacerbador (Grupo B).2, 3, 54, 55, 60, 61
Entre las limitaciones de este estudio, se puede definir
que la recolección de datos desde la historia clínica fue
retrospectiva. Otra limitación es que la extrapolación de sus
conclusiones para otros sistemas de salud de nuestro país u otras
regiones (validez externa) no es aconsejable debido a la ya referida estructura
de costos diferentes. No se han evaluado los costos indirectos (que se presumen
son más altos que los directos por lo anteriormenÂte revisado), y que no
se determinaron los costos desde otras perspectivas (paciente o sociedad). Si
bien se calcularon los costos inicialmente en pesos, la inestabilidad cambiaria
y devaluaciones sufridas por nuestro país en los últimos tiempos
determinaron que hayamos comunicado los resulÂtados en dólares. Por
último, la modulación usada por el GCBA no permitió
desagregar la estructura interna de costos para saber qué variables y
con qué peso han sido consideradas.
En conclusión, luego de veinte años, se ha
vuelto a realizar un estudio de costos directos de la exacerbación de
EPOC hospitalizada en un hospital público de la CABA. La muestra
está compuesta, en su mayoría, por hombres mayores de 60
años, con pobre seguimiento, alta carga taÂbáquica y
obstrucción grave al flujo aéreo. El costo directo desde la
perspectiva del financiador fue de USD 1462 por paciente; el costo del paciente
que se hospitaliza en UTI es casi siete veces superior. Pero hay que tener en
cuenta que solo tres paÂcientes se internaron en UTI y se encontró una
gran dispersión en el costo por paciente. La mayor parte del costo fue
previsto por el modulado para los internados en sala, pero mucho menor en UTI,
debido al uso de medicamentos de alto costo. Se ha comprobado una
reducción significativa en la estancia hospitalaria, pero con un costo
día-cama que ha permanecido estable a lo largo de 20 años (USD
162-163). Probablemente el costo indirecto sea mucho mayor. Se señala la
necesidad de incorÂporar este tipo de estudios en ámbito hospitalario
con el fin de recolectar datos que permitan una mejor administración de
los recursos disponibles. Incorporar la problemática de costos en todos
los sectores involucrados puede contribuir a que se administren los recursos
disponibles, planificar, programar y sistematizar la atención de los paÂcientes,
lo que mejora la producción y la calidad del producto final con igual o
menor presupuesto. Particularmente, por ser el mayor componente del costo
directo de atención del paciente con EPOC, se deben instrumentar
programas de manejo sistematizado de la EPOC con el objetivo de identificar
pacientes con factores de riesgo, educar en adherencia y permitir el acceso a
la medicación a fin de disminuir internaciones por reagudizaciones y,
por qué no, mortalidad.
Conflicto de intereses:
El Dr. Daniel Pascansky ha
participado en programas de educación médica continua para GSK, AstraZeneca, ELEA, Casasco y Novartis.
El Dr. Martín Sívori
ha participado en programas de educación médica continua para
GSK, AstraZeneca, TEVA y ELEA.
El Dr. Luciano Capelli no declara conflicto de intereses.
BIBLIOGRAFÍA
1. Ball P, Make B. Acute
exacerbation of chronic bronchitis: An international comparison. Chest
1998;113:199S-204S. https://doi.org/10.1378/chest.113.3_Supplement.199S
2. Global Strategy for the Diagnosis,
Management, and Prevention of Chronic Obstructive Pulmonary Disease. NHLBI/WHO. Workshop Report.
2023. Acceso en www.goldcopd.com. Consultado el 14 Noviembre de 2022.
3. Figueroa Casas JC, Schiavi
E, Mazzei JA, et al. RecomenÂdaciones para la prevención,
diagnóstico y tratamiento de la EPOC en Argentina. Medicina (B Aires)
2012;72 (Supl.I):1-33.
4. Cuarta Encuesta Nacional de Salud. Ministerio de
Salud. Argentina. 2018. Acceso en
https://www.indec.gob.ar/ftp/cuadros/publicaciones/enfr_2018_resultados_definitivos.pdf.
Consultado el 10 de Marzo 2022
5. Sullivan S, Ramsey S, Lee T.
The economic burden of COPD. Chest 2000;117:5S-9S.
https://doi.org/10.1378/chest.117.2_suppl.5S
6. Miravitlles M, Soriano JB, Garcia Rio F, et al. Prevalence of COPD in Spain: impact of undiagnosed COD on quialÂity of
life and daily life activities (EPISCAN). Thorax 2009;64:863-8. https://doi.org/10.1136/thx.2009.115725
7. Sobradillo Peña V, Miravitlles
M, Gabriel R, et al. GeoÂgraphic
Variations in Prevalence and Underdiagnosis of COPD: Results of the IBERPOC
Multicentre EpidemiologiÂcal Study. Chest 2000;118:981-9. https://doi.org/10.1378/chest.118.4.981
8. Menezes AMB, Perez-Padilla R, Jardim JB, et
al. Chronic obstructive pulmonary disease in five Latin
American cities (the PLATINO study): a prevalence study. LanÂcet 2005;366:1875-81.
https://doi.org/10.1016/S0140-6736(05)67632-5
9. Echazarreta AL, Arias SJ,
del Olmo R, et al. Prevalencia de EPOC en 6 aglomerados urbanos de Argentina:
el estudio EPOC.AR. Arch Bronconeumol
2018;54:260-9. https://doi.org/10.1016/j.arbres.2017.09.018
10. Schiavi E, Stirbulov R, Hernández Vecino R, Mercurio S, Di Boscio V, PUMA Team. COPD Screening in Primary Care in Four Latin American Countries:
Methodology of the PUMA Study. Arch Bronconeumol 2014;50:469-74.
https://doi.org/10.1016/j.arbr.2014.09.010
11. World Health Organization.
World Health Statistics 2022. Acceso 1 Octubre de 2022 en
https://www.who.int/data/gho/publications/world-health-statistics
12. Sivori M, Saenz C, Riva Posse C. Mortalidad
por Asma y EPOC en la Argentina de 1980 a 1998. Medicina (B Aires)
2001;61:513-21.
13. Bossio JC, Arias S.
Actualización de datos epidemiológicos sobre la EPOC. Instituto
Nacional de Epidemiología “Dr. Emilio Coni”.2020. (información
personal).
14. Mannino DM, Buist AS. Global burden of
COPD: risk facÂtors, prevalence, and future trends. Lancet 2007;370:765- 73.
https://doi.org/10.1016/S0140-6736(07)61380-4
15. Foster TS, Miller JD, Marton
JP, Caloyeras JP, Russell MW, Menzin J. Assessment of the economic burden of
COPD in the US: a reviews and synthesis of the literature. J COPD 2006;3:211-8.
https://doi.org/10.1080/15412550601009396
16. Newhouse JP. Medical care
costs: how much welfare loss? J Econ
Persp 1992; 6: 3-21.
https://doi.org/10.1257/jep.6.3.3
17. Sculpher MJ, Pang FS, Manca A, et al. General disability in economic evaluation studies in healthcare: a
review and case studies. Health Technol Assess 2004;8:1-19.
https://doi.org/10.3310/hta8490
18. Hilleman DE, Dewan N,
Malesker M, Friedman M. PharmaÂcoeconomic evaluation of COPD. Chest
2000;118:1278-85. https://doi.org/10.1378/chest.118.5.1278
19. Starkie JH, Briggs AH,
Chambers MG. Pharmacoeconomics in COPD: lessons for the future. Int J COPD
2008;3:71-8.
20. Del Negro R. Optimizing
economic outcomes in the manÂagement of COPD. Int J COPD 2008;3:1-10.
https://doi.org/10.2147/COPD.S671
21. Chapman KR. Epidemiology and
costs of chronic obstrucÂtive pulmonary disease. Eur Respir J 2006; 27:
188-207. https://doi.org/10.1183/09031936.06.00024505
22. Sharafkhaneh A, Petersen NJ,
Yu HJ, Dalal AA, Johmson Ml, Hanania NA. Burden of COPD in a government health
care system. Int J COPD 2010;6:125-32.
23. Guest J. Assessing the cost
of illness of emphysema. Dis Manage Health Outcomes 1998;3:81-8.
https://doi.org/10.2165/00115677-199803020-00004
24. Guest J. The annual cost of
chronic obstructive pulmoÂnary disease to the UK´s National Health Service. Dis
Manage Health Outcomes 1999;5:93-100.
https://doi.org/10.2165/00115677-199905020-00004
25. Miravitlles M, Murio C,
Guerrero T, Gisbert R. Costs of chronic bronchitis and COPD: a 1-year follow-up
study. Chest 2003;123:784-91. https://doi.org/10.1378/ chest.123.3.784
26. Jansson S, Andersson F, Borg
S, et al. Costs of COPD in Sweden according to disease severity. Chest
2002;122:1994- 2002. https://doi.org/10.1378/chest.122.6.1994
27. Pelletier-Fleury N, Lanoe JL,
Fleury B, Fardeau M. The cost of treating COPD patients with long-term oxygen
therapy in a French population. Chest 1996;110:411-6.
https://doi.org/10.1378/chest.110.2.411
28. Nielsen R, Johannssen A,
Bendiktsdottir B, et al. The economic burden of COPD in a US Medicare
population. Respir Med 2008;102:1248-56. https://doi.org/10.1016/j.rmed.2008.04.009
29. Akazawa M, Halpern R, Riedel
A, et al. Economic burden prior to COPD diagnosis: a matched case-control study
in United States. Respir Med 2008;102:1744-52.
https://doi.org/10.1016/j.rmed.2008.07.009
30. Miravitles M, Broisa M, Velasco M, et al. An economic analysis of pharmacological treatment of COPD in Spain.
Respir Med 2009;103:714-21. https://doi.org/10.1016/j.rmed.2008.11.019
31. Nielsen R, Johannssen A,
Bendiktsdottir B, et al. Present and future costs of COPD in Iceland and
Norway: results from the BOLD study. Eur Respir J 2009;34:850-7.
https://doi.org/10.1183/09031936.00166108
32. Del Negro RW, Tognella S,
Tosatto R, et al.. Costs of COPD in Italy: the SIRIO study (social impact of
respiratory inÂtegrated outcomes). Respir Med 2008;102:92-101.
https://doi.org/10.1016/j.rmed.2007.08.001
33. Izquierdo Alonso JL, de
Miguel Diez J. Economic impact of pulmonary drugs on direct costs on stable
COPD. J COPD 2004;1:215-23. https://doi.org/10.1081/COPD-120039809
34. Miller JD, Foster T,
Boulanger L, et al. Direct costs of COPD in the US: an analysis of medical
expenditure panel survey (MEPS) data. J COPD 2005;2:311-8.
https://doi.org/10.1080/15412550500218221
35. Gerdtham UG, Andersson LF,
Ericcson A, et al. Factors affecting COPD-related costs: a multivariate
analysis of a Swedish COPD cohort. Eur J Health Econ
2009;10:217-26. https://doi.org/10.1007/s10198-008-0121-6
36. Saénz C, Sivori M, Blaho E, Sanfeliz N. Costos en la EPOC: Experiencia en el Hospital Dr.J.M.Ramos Mejia y
revisión de la literatura. Rev Arg Med
Respir 2001:1:45-51.
37. Bakerly ND. Cost analysis of
an integrated care model in the management of acute exacerbations of COPD.
Chronic Respir Dis 2009;6:201-8. https://doi.org/10.1177/1479972309104279
38. Effing T, Kestejens H, Van
der Valk P, et al. Cost-effecÂtiveness of self-treatment of exacerbations on
the severity of exacerbations in patients with COPD: the COPE II study. Thorax
2009;645:956-62. https://doi.org/10.1136/thx.2008.112243
39. Steuten L, Lemmens K, Nieboer
A, Vrijhoef H. IdentifiyÂing potentially cost-effective chronic care programs
for people with COPD. Int J COPD 2009;4:87-100.
https://doi.org/10.2147/COPD.S3047
40. Puig Junoy J, Casas A,
Font-Planells J, et al. The impact of home hospitalization on healthcare costs
of exacerbations in COPD patients. Eur J Health Econ 2007; 8:325-32.
https://doi.org/10.1007/s10198-006-0029-y
41. Schermer TR, Saris CD, van
den Bosch WJ, et al. ExacerbaÂtions and associated healthcare cost in patients
with COPD in general practice. Monaldi Arch Chest Dis 2006;65:133- 40.
https://doi.org/10.4081/monaldi.2006.558
42. Simoni-Wastila L, Yang HW,
Blancehtte CM, et al. HosÂpital and emergency department utilization associated
with treatment for COPD in a managed care Medicare utilization. Curr Med Res
Opin 2009;25:2729-35. https:// doi.org/10.1185/03007990903267157
43. Simoens S, Decramer M.
Pharmacoeconomics of the manageÂment of acute exacerbations of COPD. Exp Pon
PharmacothÂer 2007;8:633-48. https://doi.org/10.1517/14656566.8.5.633
44. Guarascio AJ, Ray SM, Finch
CK, Self TH. The clinical and economic burden of COPD in USA. ClinEcon Outcomes Res 2013;5:235-45
45. Nomenclador del Ministerio de Salud del Gobierno de
la Ciudad Autónoma de Buenos Aires. Datos Personales. Junio 2021.
46. Manual Farmacéutico Kairos.
Junio 2021
47. Afolabi AO, Watson B,
Procter S, Wright AJ. The Cost to the
Health Service of Chronic Obstructive Pulmonary Disease. Eur Resp J
2000;16,31S:13.
48. Strassels S, Smith D,
Sullivan S, Mahajan P. The costs of treating COPD in the United State. Chest
2001;119:334-52. https://doi.org/10.1378/chest.119.2.344
49. Murray CJ, Atkinson C, Bhalla
K, et al. The state of US health,1990-2010: burden of diseases, injuries and
risk factors. JAMA 2013;310:591-608.
https://doi.org/10.1378/chest.119.2.344
50. Trapero Bertran M, Oliva
Moreno J, y Grupos de Expertos GECA. Guía metodológica para la
estimación de los costes en asma. Luzan 5, SA de Ediciones.2017.
51. Bilde L, Svenning R, Dollerup
J, Bække Borgeskov J, Lange P. The cost of treating patients with COPD in
Denmark - A population study of COPD patients compared with non- COPD controls.
Respir Med 1999;101:539-46. https://doi.org/10.1016/j.rmed.2006.06.020
52. Hoogendoorn M., Rutten-van
Mölken MP., Hoogenveen RT et al. A dynamic population model of disease
progression in COPD. Eur Respir J 2005;26:223-33.
https://doi.org/10.1183/09031936.05.00122004
53. Dirección de Estadísticas en Salud del
Ministerio de Salud del Gobierno de la Ciudad Autónoma de Buenos Aires.
2021.
54. Montes de Oca M, Lopez
Varela V, Acuña A, et al. Guía de práctica clínica
de la EPOC ALAT 2014: Preguntas y respuestas. Arch Bronconeumol 2015;51:403-16. https://doi.org/10.1016/j.arbres.2014.11.017
55. Miravitlles M, Soler
Cataluña JJ, Calle M, et al Guía español de la EPOC (GesEPOC) 2017. Arch BroncoÂneumol
2017;53:324-335. https://doi.org/10.1016/j.arÂbres.2017.03.018
56. Vestbo J, Anderson W, Coxson
HO, et al. Evaluation of COPD longitudinally to identify predictive surrogate
end-points (ECLIPSE). Eur Respir J 2008;31:869–73.
https://doi.org/10.1183/09031936.00111707
57. Soler-Cataluña JJ,
Martínez-García MA, Román Sánchez P, Salcedo E,
Navarro M, Ochando R. Severe acute exacerÂbations and mortality in patients
with chronic obstructive pulmonary disease. Thorax 2005;60:925-31. https://doi.org/10.1136/thx.2005.040527
58. Sivori M, Balanzat A, Casas JP, et al. Inhaloterapia:
RecoÂmendaciones para Argentina 2021. Medicina Buenos Aires 2021;81 (Supl II):1-32.
59. Usmani OS, Lavorini F,
Marshall J, et al. Critical inhaler errors in asthma and COPD: a systematic
review of impact on health outcomes. Respir Res 2018;19: 10.
https://doi.org/10.1186/s12931-017-0710-y
60. Sivori M, Fernández
R, Toibaro J, Velasquez Gortaire E. Supervivencia en una cohorte de pacientes con
EPOC acorde a la clasificación GOLD 2017. Medicina Buenos Aires
2019;79:20-8.
61. Jimenez J, Sivori M. Evaluación de las comorbilidades por los
índices de Charlson y COTE en la EPOC y su
relación con la mortalidad. Revista Americana de Medicina Respiratoria
2022;22:3-9.