Autor : Gasteneguy Rodrigo1, GonzÃĄlez Claudio2, Saadia Otero Marcela3, FernÃĄndez Florencia4, TurÃģn Gonzalo5, Castro Ignacio6 ,Larrateguy Santiago7, Armelino Javier8, Miguel Mauricio9, Alvarez Marcelo10 COLABORADORES: Cigarra Cecilia1, Lebus Janina2, OlguÃn Emilia3, Conti Ernesto4, Cuello Juan Ignacio5
AUTORES 1 Hospital Municipal de Coronel SuÃĄrez âDr. RaÚl A. Caccavoâ. Coronel SuÃĄrez. Buenos Aires. 2Hospital General de Agudos JosÃĐ M. Ramos MejÃa. CABA. 3 Hospital de RehabilitaciÃģn Respiratoria MarÃa Ferrer. CABA. 4Hospital General de Agudos Enrique TornÚ. CABA 5Hospital Italiano de Buenos Aires. CABA. 6Hospital Bouquet Roldan. NeuquÃĐn. 7Centro Privado de Medicina Respiratoria. Universidad Adventista del Plata. ParanÃĄ. Entre RÃos. 8Hospital de ClÃnicas JosÃĐ de San MartÃn. 9Sanatorio BritÃĄnico. Centro de KinesiologÃa CrÃtica. Rosario. Santa Fe. 10Hospital Zonal General de Agudos Julio de Vedia. 9 de Julio. Buenos Aires. COLABORADORES 1Hospital Interzonal General de Agudos Petrona Villegas de Cordero. San Fernando. Buenos Aires 2 Consultorio NeumokinÃĐsico Avellaneda. Santa FÃĐ 3Hospital Italiano de San justo. Buenos Aires 4Instituto Cordis. Resistencia. Chaco. 5Hospital Municipal âEva PerÃģnâ de Coronel Dorrego. Buenos Aires.
https://doi.org/10.56538/ramr.MIND9052
Correspondencia : Dr. Rodrigo Gasteneguy. E-mail: mgasteneguy@gmail.com
Recibido: 16/09/2021
Aceptado: 27/03/2022
INTRODUCCIÓN. FUNDAMENTOS Y JUSTIFICACIÓN DEL DOCUMENTO
En diciembre del año 2019, en la localidad china
de Wuhan se detectó el priÂmer caso de enfermedad por el virus
SARS-Cov-2.1 A diferencia
del carácter limitado de las dos últimas epidemias, la del
Síndrome Respiratorio de Medio Oriente (MERS) y el Síndrome
Respiratorio Agudo Grave por Coronavirus (SARS-CoV), la rápida
expansión del SARS-CoV-2 obligó a la Organización Mundial
de la Salud (OMS) a declarar la situación de pandemia en marzo de 2020.2
Según los reportes de la evolución de la
pandemia disponibles en el centro de la Universidad John Hopkins (UJH), al
momento de la redacción de este documento se han registrado en el mundo
alrededor de 160 millones de casos y 3,3 millones de muertes.3
Durante el primer año, la pandemia produjo 1,8 millones de
muertes en todo el mundo, frente a las 2,6 millones producidas por todas las infecciones
respiratorias bajas en 2019. 4
Mientras la mortalidad producida por todas las
infecciones respiratorias en 2017 (último registro disponible) fue de
64.869 personas, sólo la produÂcida por el SARS-CoV-2 en un año de
pandemia alcanzó 53.741 muertes.5,6
Además de la mortalidad producida por el
SARS-CoV-2, deben considerarse otros dos niveles más de impacto: el
primero es el que genera la enfermedad aguda, que exige la intervención
de la herramienÂta rehabilitación en forma temprana, como en la UCI y
las salas de internación. El segundo nivel de impacto se refiere a la
enfermedad crónica, a la multiplicidad de secuelas funcionales
físicas, psíquicas y neurocognitivas que en los pacientes críticos
suele expresarse como el Síndrome Post- Cuidados Intensivos (DAUCI).
Un estudio de carácter nacional sobre una muestra
de 207.000 pacientes con datos compleÂtos, atendidos entre marzo y octubre de
2020, nos permite tener una estimación aproximada acerca de
cuántos pacientes que sufrieron enfermedad por SARS-CoV-2
requerirían rehabilitación.7
Se hospitalizaron un 20,1% de ellos (41.703 pacienÂtes), de los
cuales 2,7% (5.652 pacientes) ingreÂsaron a la UCI. Sólo entre estos
sobrevivientes de la UCI, unos 2.800 pacientes, la intervención
rehabilitación en ese contexto, luego en la sala de cuidados intermedios
y después en la modaÂlidad ambulatoria presencial o virtual,
estaría justificada.
Además de los pacientes egresados de la UCI,
debería incluirse en la indicación a aquellos que tuvieron formas
moderadas o graves que requirieÂron distintos niveles de oxigenoterapia en
salas de cuidados intermedios o generales.
Por lo expuesto, urge la implementación temÂprana
de esta intervención, principalmente en las áreas
respiratoria, cardiovascular, neuromotora, cognitiva y psicológica,
intervenciones estas que minimicen las secuelas y propendan a alcanzar la
máxima autonomía del paciente y la mayor calidad de vida posible.8
En todos los casos, se enfatiza además sobre la
necesidad de que la rehabilitación sea una interÂvención continua.
Se recomienda mantener una línea de trabajo común a lo largo de
las distintas etapas de la evolución de la enfermedad. Sea el caso de
pacientes que inician esta intervención en la UCI, la mantienen en la sala
de cuidados generales y la continúan en el período de
externación, como en aquellos que comienzan en la sala de cuidados
generales y la prolongan ambulatoriamente.
El objetivo de este documento es ofrecer a los
profesionales comprometidos en la Rehabilitación Respiratoria de estos
pacientes, un conjunto de recomendaciones, que avaladas por el estado del
conocimiento actual y refrendadas por nuestros expertos temáticos,
constituya una herramienta factible de ser implementada en centros de difeÂrentes
complejidades de nuestro país.
PRESENTACIÓN CLÍNICA DE LA INFECCIÓN POR SARS-COV-2
La infección por SARS-CoV-2 puede presentarse de
manera asintomática o sintomática. En esta última,
podremos encontrar desde formas leves y moderadas hasta formas graves con
neumonía y SDRA (Síndrome de Dificultad Respiratoria AguÂda), con
insuficiencia respiratoria y falla multiorgáÂnica. También se
podrán presentar complicaciones a largo plazo luego de la
infección por SARS-CoV-2 provocando el Síndrome Post-COVID (SpC) o
el Síndrome COVID Persistente (CP).
Aproximadamente el 80% de los pacientes con COVID-19
desarrollan una enfermedad leve a moderada, el 15% progresa a etapas graves que
requieren soporte de oxígeno y el 5% desarrolla una enfermedad
crítica que incluye el SDRA, shock séptico y fallo
multiorgánico.9 La edad y
diversas comorbilidades como la diabetes, obesidad, enferÂmedades pulmonares y
cardiovasculares y algunos polimorfismos genéticos se correlacionan con
un mayor riesgo de insuficiencia respiratoria.10-12
Debemos tener en cuenta además que aproxiÂmadamente
el 50% de las personas con neumonía grave por COVID-19 desarrollan un
SDRA, siendo la fibrosis pulmonar una complicación habitual.13 Estos
pacientes desarrollarán un deterioro de la función pulmonar con
insuficiencia respiratoria irreversible asociado a un mal pronóstico.14
A. REHABILITACION RESPIRATORIA EN PACIENTES CON COVID-19 INTERNADOS EN LAS
UNIDADES DE CUIDADOS CRITICOS
Los pacientes que padecen COVID-19 y requieren para su
tratamiento, internación en una Unidad de Cuidados Intensivos (UCI) con
o sin necesidad de ventilación mecánica invasiva (VMI), demandan
una asistencia temprana de la atención kinésica. No solamente
para el manejo del tratamiento venÂtilatorio, sino también respecto a la
rehabilitación motora para lograr que el paciente, al alta de la UCI,
pueda retornar a sus tareas habituales.
En este apartado se sugiere establecer pautas generales
expresadas a partir de cómo evaluar el impacto de la
rehabilitación en estos pacientes, qué evaluaciones se pueden
utilizar y cómo se aborda el proceso de rehabilitación en el
paciente COVID-19 en las UCI.
Lo primero que se decide, es la organización del
plan de rehabilitación que deberá ser en forÂma individualizada y
personalizada. Para ello se contemplará:
1. Establecer una adecuada titulación de la analÂgesia
y sedación de acuerdo al modo ventilatorio implementado,
evolución de la patología y el estado de oxigenación del
paciente.
2. Implementar un modo y seteo del ventilador adecuado para
el paciente (evitar la asincronía paciente/ventilador), sobre
distensión e hipoÂventilación.15
3. Dosificar la terapia kinésica de acuerdo al
estado clínico del paciente.
4. Monitorear con criterios de seguridad estrictos.16
5. Programar la Rehabilitación Precoz junto al
equipo interdisciplinario.
En el abordaje de los puntos críticos de este
apartado, con fines didácticos se utilizan cuatro preguntas gatillo.
1. Cuáles son los objetivos de un programa de rehabilitación
en la UCI?
El objetivo principal de un programa de rehabiÂlitación
precoz (RP), (definiendo la RP como una intervención dirigida a
proporcionar un estímulo motor, sensitivo y propioceptivo, que genere en
el paciente una disminución del impacto negativo del ingreso en UCI), es
evitar la pérdida de la funÂcionalidad que tenía el paciente
previo al ingreso al área crítica.17
Ello se completa proponiendo los objetivos de comenzar
tempranamente con la RP como la dismiÂnución de la sedación y la
analgesia, mantención de los rangos articulares, sedestación,
bipedestación y marcha. Para luego avanzar con las AVD.
Estas metas deben proponerse al ingreso del paciente en
el área crítica y evaluarse al alta de la misma.
Para una correcta organización de los objetivos
propuestos, se puede implementar el paquete de medidas conocido como el âABCDEF
Bundleâ, esÂpecialmente en el destete temprano, la prevención y el
tratamiento del delirium y la rehabilitación precoz.18
Ello permite coordinar los cuidados del paciente para
independizarlo de la VMI y de la UCI.
2. ÂŋCuáles son los criterios de inicio de la rehabilitación?
El kinesiólogo debe adaptarse a las condiciones en
que se encuentre el paciente ya sea con intubación orotraqueal o
traqueotomía, ventilación mecáÂnica invasiva o no
invasiva, terapia de alto flujo humidificado o cualquier otra forma de soporte
de oxigenoterapia. Es imprescindible considerar la presencia de las vías
de administración de medicamentos, drenajes, monitoreo y estabilidad hemodinámica.
Se requiere de una condición médica
estable, presencia de una vía aérea sin complicaciones y reÂquerimiento
asegurado de oxígeno, como también comenzar la sesión de
Rehabilitación Respiratoria (RR) asegurando la aplicación de
medicación en caso de ser necesario.
Se pueden definir los criterios en:19
1. Frecuencia cardíaca menor al 50% de la FC
máxima teórica (FCMT).
2. Presión arterial con una variabilidad menor al
20% (evitar descompensación hemodinámica).
3. Electrocardiograma normal.
4. Saturación parcial de oxígeno > a 90%
y con una disminución de la misma menor de 4 puntos al momento de
realizar la RP.
5. PaO2/FiO2 > a 300
(índice de tolerancia de la RP con buena reserva respiratoria, valores
menores disminuye dicha reserva, estado de alerta)
6. Patrón respiratorio adaptado.
7. Ventilación mecánica estable.
8. Vía aérea estable.
9. Ausencia de fiebre.
3. ÂŋCómo se evalúa al paciente que inicia
rehabilitación en las UCI?
La evaluación debe incluir la función respiratoria,
la muscular y el estado del sensorio. Los instruÂmentos recomendados son los
siguientes:
1. Evaluación de la disnea a través de la
escala MRCm.20
2. Evaluación del estado muscular a través
de la escala MRC.21
3. Valoración de sedación y analgesia y
estado de alerta del paciente: Escala Analógica Visual (EVA), Escala
sobre Conductas Indicadoras de Dolor (ESÂCID) Richmond Agitation-Sedation Scale
(RASS), y escala del delirio (CAM-ICU).22-24
4. ÂŋCuáles son los componentes del plan de rehabilitación
precoz en la UCI?
Deben respetarse los estadios según el modelo de
niveles de complejidad de Morris25.
El plan se compone de los siguientes pasos.
âĒ Incluir dos estímulos diarios desde el ingreso
del paciente al área crítica hasta el alta.
âĒ El nivel inicial, (paciente con sedación proÂfunda),
incluye la movilización pasiva de los miembros y los cuidados
posicionales.
âĒ Una vez que el paciente comienza a recuperar el estado
de conciencia se inician los ejercicios activos asistidos y la progresión
funcional de acuerdo vaya logrando los objetivos, esta proÂgresión
será: sentarse al borde de la cama, una vez que tiene control de tronco
comenzar con bipedestación y luego progresar a la deambulaÂción
con asistencia y lograr actividades fuera de la cama.25,26
âĒ Incluir a los familiares en el proceso de rehaÂbilitación
a través de video llamadas, que sean capaces de colaborar tanto con la
progresión funcional como con el aporte de elementos proÂpios del
paciente (reloj, lentes, libros, radio, etc.)
âĒ Llevar un registro de los eventos adversos a fin de
evitar su repetición.
B. REHABILITACION RESPIRATORIA EN LA SALA DE INTERNACION
Como ya fue mencionado, se calcula que entre el 14% y el
20% de los pacientes infectados por SARS-Cov-2 requerirán hospitalización
en una Sala de Internación general, por lo que las complicaciones
asociadas a la inmovilización podrían generar un impacto negativo
en la calidad de vida.7,27 Es imÂprescindible,
entonces que los pacientes reciban terapias de rehabilitación
respiratoria durante la atención hospitalaria, con el fin de prevenir y
manejar oportunamente tanto los efectos del desacondicionamiento físico
como los relativos a la aparición de secuelas.28
Cuando el paciente es derivado desde la UCI a Cuidados Intermedios
o a la sala de internación, la RR deberá ser un continuo lineal
con la iniciada en la UCI, o bien en aquellos pacientes que se internen en
primera instancia en la Sala de internación, se requerirá a su
ingreso al programa de rehabilitaÂción las siguientes condiciones:
1. Se deberá continuar con el tratamiento de RR si
el paciente procede de la UCI, o bien establecer el mismo cuando el paciente se
interne directaÂmente en la Sala de Internación.
2. Se realizará una evaluación para
identificar aquellos factores pronósticos del Síndrome DAUCI, del
Daño Crónico por COVID, del SínÂdrome Post-COVID y el
Síndrome COVID perÂsistente, en el caso de los pacientes procedentes de
la UCI.29
3. Se deberán plantear los objetivos de la rehabiÂlitación.27,30
4. Se deberá conocer la evolución del
paciente.
5. Se recomendará comparar los parámetros y
aplicaciones propias de la RR en sus diferentes etapas.
En este apartado, se enuncian tres preguntas gatillo que
intentan abordar el a quiénes, cómo y cuándo
se realiza la RR en pacientes en salas de internación generales.
1. ÂŋCuáles son las condiciones para iniciar la RR en pacientes con
COVID-19 en salas de internación?
De acuerdo a lo mencionado, alrededor del 3-5% de los
pacientes moderadamente enfermos desarrollaÂrán una enfermedad grave o
incluso crítica luego de 7 a 14 días de iniciada la
infección31,32 .
Los parámetros a evaluar en el paciente que
proviene de la UCI son:31-33
1. El tiempo trascurrido desde el inicio de los
sínÂtomas.
2. El tipo y la cantidad de síntomas.
3. Los valores de saturación de oxígeno.
4. La intensidad y extensión del compromiso raÂdiológico
pulmonar
5. El requerimiento de oxígeno suplementario y su
forma de administración.
6. La necesidad de utilizar ventilación
mecánica invasiva o no invasiva.
7. El tiempo de ventilación y sus posibles compliÂcaciones.
8. La coexistencia de complicaciones renales, heÂmatológicas,
neurológicas o de cualquier otro tipo y el tipo de tratamiento recibido.
9. En los pacientes cuyo ingreso fue de inicio en la sala
de internación, establecer conducta obserÂvacional de acuerdo a
evolución del paciente.
A. CRITERIOS DE EXCLUSIÓN Y
CRITERIOS DE FINALIZACIÓN DEL EJERCICIO
A.1 CRITERIOS DE EXCLUSIÓN27,31
â Paciente febril.
â Un tiempo de consulta inicial ≤ 7 días en
aquellos pacientes internados directamente en la Sala de internación.
â Una duración desde el inicio de la enfermedad
hasta la aparición de la disnea, por progresión de la enfermedad
o cuadro clínico en plena acÂtividad ≤ 3 días.
â Progresión de opacidades en la
radiografía de tórax al menos del 50% en 24 a 48 horas.
â Una SO2
≤ 90% con oxígeno suplementario.
â Una Frecuencia Cardiaca < 40 o > 130 lpm.
â Una presión arterial en reposo < 90/60 o >
140/90 mmHg.
â Una frecuencia respiratoria > a 24 rpm.
â La falta de consentimiento del paciente.
A.2 CRITERIOS DE FINALIZACIÓN
DEL EJERCICIO27,
31, 33
â Un valor en la Escala de Borg modificada > 3 en la
puntuación de la disnea en la etapa inicial de la RR.
â Una caída de la SpO2 > 4%.
â Signos de opresión torácica.
â Alteraciones en la mecánica ventilatoria y/o
aparición de utilización de músculos accesorios.
â Dificultad para respirar, mareos, dolor de caÂbeza,
visión borrosa, palpitaciones, sudoración profusa y trastorno del
equilibrio.
â Otras condiciones que el médico determine que no
son adecuadas para el ejercicio.
2. ÂŋCómo deben evaluarse los pacientes que se incluyen en la
intervención rehabilitadora?
Las diferentes evaluaciones que se describen a conÂtinuación
serán seleccionadas dependiendo del conÂtexto laboral en el que se
desarrolle cada profesional.
Existen diferentes dominios en el ámbito de la
evaluación:
1. EVALUACIÓN DEL ESTADO
GENERAL DEL PACIENTE
Se observará el tipo respiratorio, estado de masas
musculares, movilidad y amplitud articular, estaÂdo del sensorio y la
posibilidad de colaborar en la rehabilitación.
2. EVALUACIÓN DE LA DISNEA
Para la evaluación del nivel de disnea podemos usar
varias escalas validadas y sencillas.
2.1 Escala de Borg modificada: a fines de evaluar el nivel de esfuerzo percibido por los paÂcientes y
poder prescribir y controlar la intensidad de la actividad realizada27.
2.2 Escala analógica visual34
3. EVALUACIÓN DE LA CAPACIDAD
DE EJERCICIO
Si las reservas cardiorrespiratoria y metabólica
del paciente lo permiten se podrá realizar:
3.1 SIT-TO-STAND TEST 1â (STS): este test permitirá evaluar la desaturación inducida por el
ejercicio.35
3.2 5R-STS: el punto de corte de normalidad es de ≤ 12 segundos.36
3.3 TEST TIME UP and Go (TUG): el punto de corte de anormalidad para el riesgo de caída
será ≥ 16 segundos.37
3.4 4 - METRE GAIT SPEED o Velocidad
de marcha en 4 metros: este test
evaluará el tiempo requerido para caminar 4 metros a la velocidad
habitual. Se considerará anormal un tiempo > de 0.8 m/seg.38
4. VALORACION DE FUERZA
3.1 Escala Medical Research
Council (MRC)27.
3.2 Método de repeticiones.39-41
4. EVALUACIÓN DE LAS
ACTIVIDADES DE LA VIDA DIARIA (AVD)
4.1 PCFS29
4.2 Índice de Barthel42
4.3 Índice de Katz43
3. ÂŋCuándo y cómo realizar el entrenamiento muscular
periférico en estos pacientes?
Se sugiere iniciar la rehabilitación en forma temÂprana
en los pacientes provenientes de la UCI y en aquellos que se internen
directamente en la Sala en los primeros 3 días luego de estabilizado el
paciente. Es importante además mantener un adecuado control del dolor,
para favorecer el alcanÂce de los objetivos.27
El diseño de los programas de RR para pacienÂtes
con COVID-19 debe respetar los principios generales de entrenamiento
relacionados con la intensidad, duración, frecuencia, especificidad y
reversibilidad del ejercicio.30,44
Para ello, a partir de las evaluaciones realizadas en
cuanto a su capacidad de ejercicio se deberá programar en forma
personalizada los objetivos y alcances a lograr con el paciente45.
MONITOREO DEL PACIENTE: Realizar el monitoreo del paciente antes, durante y al finaÂlizar la
sesión de rehabilitación. Las variables a monitorear
serán:
0.1 SpO2:
la misma deberá ser mayor de 90% con o sin oxígeno suplementario,
con una tolerancia de variabilidad menor al 4% durante la sesión.27
0.2 Presión arterial: la misma deberá
presentar una tolerancia de variabilidad no mayor al 20% durante la
sesión.46
0.3 FC: se sugiere una tolerancia de variabilidad no
mayor al 80% de la FCMT(secuelas
por COVID-19.52-53.
0.4 FR: la misma no deberá ser mayor a 24 rpm.46
0.5 De ser posible reiniciar la sesión cuando los
parámetros mencionados vuelvan a la normaÂlidad.27
1. EJERCITACIÓN DE LA FUERZA
MUSCULAR
1.1 Se sugiere comenzar con grupos musculares grandes
(cintura escapular y pelviana).43
1.2 Se incorporará ejercitación del
equilibrio, propiocepción y coordinación. Se controlará
además el riesgo de caídas.27
1.3 Intensidad del ejercicio: se comenzará con
ejercicios de movilización activa, continuando con ejercicios del propio
cuerpo con series de intensidades bajas (60% de la máxima alcanÂzada con
el método de repeticiones) y se irá aumentando la misma
según la respuesta muscular del paciente. Se sugiere una cantidad de 3
series por grupo muscular con un tiempo de pausa de 2 minutos entre cada serie.47,48
1.4 Se sugiere utilizar el entrenamiento funcioÂnal.49-51
1.5 Se recomienda que la frecuencia sea de dos veces al
día.27
1.6 En cuanto a la duración de la sesión,
se reÂcomienda iniciar con 20 minutos y progresar hasta los 30 minutos.
2. EJERCITACIÓN DE LA
CAPACIDAD AERÓBICA
2.1 Dado el poco espacio que presentan las habiÂtaciones
de las salas de internación, se sugiere la realización de
ejercicios en el lugar o con desplazamientos cortos, buscando además la
seguridad epidemiológica.
2.2 La intensidad del ejercicio se sugiere que sea
progresiva hasta alcanzar el 80% de la FCMT.
2.3 Los métodos de entrenamiento podrán ser
continuos o intermitentes.27
2.4 Se recomienda una frecuencia de dos veces al
día.27
2.5 La duración de la sesión,
preferentemente no deberá ser menor a 20 minutos con progresión
hasta 30 minutos.
REHABILITACIÓN RESPIRATORIA
AL MOMENTO DEL ALTA HOSPITALARIA
Es de suma importancia que antes del alta hosÂpitalaria
se realice un informe que refleje las necesidades más inmediatas del
paciente, como la seguridad de movilidad en el domicilio, el control de los
síntomas, la necesidad de oxígeno suplemenÂtario, la adecuada
nutrición, el apoyo psicológico y social y las necesidades a
corto y mediano plazo como la mejora de las funciones física y emocional
y la vuelta al trabajo.17
C. REHABILITACION RESPIRATORIA EN PACIENTES AMBULATORIOS CON SINDROME
POST-COVID-19 Y SINDROME COVID LARGO O PERSISTENTE
Este apartado tiene por objeto abordar la rehabiÂlitación
respiratoria de pacientes que padecieron enfermedad por SARS-Cov-2 y se
encuentran daÂdos de alta de la internación, así como
también a aquellos que han cursado la enfermedad en forma ambulatoria
pero que evolucionaron y persisten con disnea.
En este capítulo se utilizan cinco preguntas
gatillo sobre cuestiones de interés para los proÂfesionales a cargo de
la modalidad ambulatoria de los Programas de Rehabilitación Respiratoria
(PRR)
1. ÂŋQué significan el Síndrome Post-COVID-19 y el
Síndrome COVID Largo o Persistente?
De acuerdo a diferentes estudios internacionales, la
duración de los síntomas de la infección por COÂVID-19
tiene una media de 11 días para pacientes no hospitalizados y de 13 a 25
días para aquellos que requirieron internación52. Sin embargo, luego de la
resolución de la infección vírica, se ha obserÂvado que
algunos síntomas y signos tienden a prolongarse en el tiempo. Se define
el Síndrome post- COVID-19 (en adelante, SpC) como aquel conjunto
de signos y síntomas que aparecen luego de que fue resuelta la
infección aguda.53-61 Incluye
síntomas persistentes que podrían estar relacionados con la
inflamación residual (en la fase convaleciente), con el daño
orgánico y con los efectos inespecíficos de la hospitalización
o ventilación prolongada (DAUCI) y COVID Largo o Persistente (SP).52-53
La primera descripción que alertó sobre la
imÂportancia del SpC data de una encuesta a pacientes realizada en Estados
Unidos entre abril y mayo del año 202054. La denominación de SpC surge
de este trabajo y fue refrendada por Greenhalgh en una publicación
posterior.55
Autores españoles proponen considerar cuatro
etapas de la enfermedad por SARS-CoV2 y delimiÂtar dichos cuadros
clínicos de acuerdo al tiempo de evolución.56
De esta manera, los síntomas relacioÂnados con la
infección aguda estarían limitados a las primeras 4 semanas; el
SpC agudo indicaría la persistencia de los síntomas por 5-12
semanas; las formas con sintomatología prolongada se desÂdoblarían
en dos: Síndrome Post-COVID Largo (SL), de 12-24 semanas de
evolución y el nombrado Persistente (SP), que se prolongaría
más allá de las 24 semanas desde el inicio de los
síntomas.56
No obstante, aún no hay aún una
denominación aceptada universalmente en las definiciones de SpC y SP.
Dos guías españolas definen como SpC al conjunto de hallazgos
sistémicos que van más allá de las 4 semanas desde el
inicio del primer síntoÂma, siendo requisito indispensable que los
signos y síntomas hayan formado parte de la infección aguda.52-53 La
guía NICE del Reino Unido toma en consideración el SP a partir de
las doce semanas y la guía de la OMS, lo hace a partir de la cuarta o
quinta semana.57,58
La frecuencia del SP está estimada en el 10-35% de
los pacientes en general, aunque en aquellos hospitalizados graves puede
alcanzar al 80% de ellos.53,54,59
2. ÂŋCómo diferenciar el SpC y el SP de otros cuadros clínicos
que pueden simularlos?
Resulta importante distinguir un cuadro post- COVID de
situaciones que pueden ser semejantes, aunque no comparten o su temporalidad
y/o su presentación clínica.
A. En el caso en que los síntomas y signos estuÂvieran
presentes antes del inicio del cuadro por COVID-19.
B. En la situación en la que estos aparezcan desÂpués
de la infección y no hayan formado parte de ella (síntomas
post-virales).
C. En el caso en que síntomas o signos aparezcan después
de la infección, que no hayan formaÂdo parte del cuadro inicial y se
deban al daño orgánico generado por la misma (secuelas por
COVID-19.52-53 A diferencia del
SP, los pacientes que han evolucionado con secuelas orgánicas suelen ser
varones de más edad, presentan comorbilidades previas y su
evolución no se da en brotes como el SP.53
D. Por último, la situación que surge del
daño sistémico u orgánico por una infección grave (Daño
Crónico Post-Covid-19)52
3. ÂŋCuál es la presentación y el perfil clínico del
paciente con SP que es derivado a un Programa de Rehabilitación
Respiratoria?
López León y col. realizaron una
revisión sisteÂmática y meta análisis de la literatura
disponible sobre síntomas y signos prolongados ocasionaÂdos por la
infección por COVID-19.60 Sobre 15
trabajos, 6 correspondían a pacientes hospitaÂlizados y su seguimiento
fue de 14-110 días. Se identificaron 55 signos o síntomas persistentes
relacionados con la infección viral, siendo los más frecuentes:
fatiga (58%), dolor de cabeza (44%), trastornos de la atención (27%),
caída de cabello (25%) y disnea (24%). En 7 estudios (n=1915 pacientes),
el 80% de ellos tuvieron al menos un síntoma persistente.60
En relación al perfil del paciente que es
derivado habitualmente a los PRR con diagnóstico de SP, una encuesta
sobre 3.762 pacientes de 56 países, describió síntomas
hasta 7 meses después del inicio de la infección aguda.62 La
mayoría llevaba al menos 3 meses de evolución, una media de 14
síntomas por paciente y un promedio de 9 órganos afectados61.
En lo que se refiere al nivel de discapacidad con
que suelen auto percibirse los pacientes, una encuesta española revela
que referían una discapacidad del 50%.62
El desglose por actiÂvidad mostró frecuentes limitaciones
para el aseo personal y las actividades de la vida diaria, que fueron
más marcadas aún en lo atinente a las obligaciones familiares y
las actividades de esparcimiento.62
4. ÂŋCuándo, dónde y cómo evaluar inicialmente a un
paciente con SpC y SP?
La evidencia sobre cuál es el mejor abordaje para
los pacientes con SpC y SP que llegan a un PRR, es todavía escasa.30,52,57,58,63-65,66-70 No obstante,
existe unanimidad de criterio sobre ciertas cuestiones importantes.
En primer lugar, desde este documento sosteÂnemos que en
aquellos pacientes que estuvieron hospitalizados por largo tiempo o que
tuvieron requerimiento de oxígeno o soporte ventilatorio, la
rehabilitación respiratoria ambulatoria o domiÂciliaria debería ser
una estrategia continua con lo iniciado en la UCI o en la sala de cuidados
generales.
En segundo lugar, en razón de la multiplicidad de
órganos afectados en el SP, el cuantioso númeÂro de
síntomas reportados por los pacientes y el tiempo de evolución de
los mismos, es necesario un abordaje multidisciplinario de quien
padeció COVID-19 y llega a un PRR.30,53,57,58,63-70
En tercer lugar, parece claro que, siempre que sea
viable, la rehabilitación debe estar centrada en el paciente.30,53,57,63-70 Esto implica
que dónde será evaluado dependerá de cuáles
sean las posibilidaÂdes y necesidades del paciente.
A. Evaluación no presencial
de pacientes con SpC y SP
Si bien existe acuerdo sobre la utilidad del uso de la
Telemedicina en ciertos colectivos que aplican a los PRR, no existe a la fecha
un protocolo estandarizado y validado sobre cómo evaluar y entrenar de
manera virtual a los pacientes con SpC y SP. La bibliografía consultada
se apoya en recomendaciones de experÂtos.44,52,53,57,63,70 Tres puntos básicos deben ser tenidos
en cuenta al momento de incluir a un paciente en un PRR a distancia: la indicación,
de acuerdo a la situación particular del paciente; los criterios a
reunir para que pueda acceder en condiciones de equidad a la
intervención; las características de las herramientas a
utilizar en la evaluación.44,67-70
La tabla 1 describe las indicaciones, los criterios de
inclusión que aseguren la equidad al paciente y las herramientas a
utilizar en el proceso.
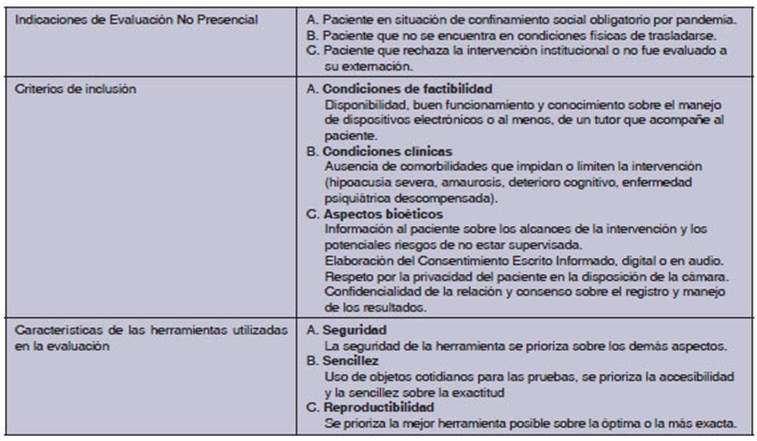
Se propone la evaluación de estos pacientes
estandarizada en pasos.
El primer paso consiste en la evaluación de los antecedentes personales y de
enfermedad actual aportados en la epicrisis de la historia clínica de
internación.30,44,52,53,57,63,66,68-70 Deberían
estar conÂsignadas las comorbilidades preexistentes y como antecedentes de enfermedad actual el tiempo de
evolución del padecimiento y los síntomas iniciales, los
días de estadía, la extensión y gravedad del compromiso,
el requerimiento o no de oxigenoteÂrapia (dispositivos y flujos utilizados), la
aplicación o no de ventilación no invasiva e invasiva
(días de ventilación efectiva), el tratamiento instituido y su
respuesta, las anomalías de laboratorio de relevancia clínica y
pronostica y el listado de comÂplicaciones y potenciales secuelas registrados a
su egreso hospitalario.44,66,68,69
La importancia del número de
síntomas iniciales se relaciona con un mayor riesgo de sufrir SP. La
presencia de cinco o más síntomas en la primera semana de
evolución, aumenta 3,53 veces el riesgo de padecer una enfermedad
prolongada con resÂpecto a los pacientes que presentan menos de ese
número de síntomas.44,64,66,68,69
El segundo paso incluye la
estimación virtual del estado general del paciente: su aspecto, el estado
de masas musculares, la mecánica ventilatoria, la identificación
de limitaciones a movimientos y el estado del sensorio.69
El tercer paso permite establecer el
nivel de disnea y su capacidad de ejercicio.
Se le solicita al paciente que identifique su
nivel de disnea de acuerdo a las escalas de disnea de Borg y la escala de
disnea modificada del Medical Research Council (MRCm).67-70 Para evaluar su reÂquerimiento
o no de oxígeno, se solicita al paciente la medición en reposo y
sentado de su saturación de oxígeno (SpO2).
Si los valores hallados son iguales o mayores al 96%, se le pide que con el
oxímetro colocado realice una caminata de cuarenta pasos en una
superficie plana. En el caso de pacientes que no cuenten con un oxímetro
o como informaÂción complementaria de aquellos que lo poseen, se
aconseja que en la actividad física no superen los 4 (cuatro) puntos en
la percepción de disnea de la Escala de Borg.69
Además de la estimación de su
disnea y la SpO2, se
deberá monitorear la frecuencia cardíaca (FC) de reposo y
después de cada serie de ejercicios. Dado que la actividad no es
supervisada, se sugiere la fórmula de 220 pulsaciones menos la edad del
paciente.
Una segunda alternativa para evaluar la caÂpacidad
de ejercicio, es la realización de manera remota de la prueba Sitto
Stand (STS). Si bien fue desarrollada y validada para pacientes con EPOC,
dada su seguridad y sencillez, ha sido propuesta en publicaciones sobre
rehabilitación a distancia.69-71 Desde la modalidad menos
exigente de 5R a las de STS30â y STS1â, estas pruebas permiten evaluar la
contracción concéntrica y excéntrica del cuádriÂceps,
el estado de equilibrio e incluso la variante de 1â correlaciona con la Prueba
de Caminata de Seis Minutos (PC6M).65,71
El cuarto paso consiste en la
evaluación de fuerza muscular y el estado nutricional, frecuenÂtemente
alterado por la sarcopenia del SpC y el DAUCI.30,44,52-55,57,60,64,66,68-70
Se propone el método de
evaluación de fuerza en 8 RM, la evaluación de 3-4 grupos
musculares por tren, y el monitoreo con la Escala Analógica Visual, FC,
y SpO2. A los fines de
estimar la capaciÂdad del paciente de afrontar actividades cotidianas, se
propone evaluar las cargas usando el peso del propio paciente.
En relación al estado nutricional, se
valora el ÍnÂdice de Masa Corporal (IMC), que junto con la obserÂvación
de sus masas musculares nos permitirá tener una idea aproximada sobre el
estado nutricional del paciente.69 A esto debe agregarse el
seguimiento virtual y el consejo del nutricionista sobre el régimen
alimentario más apropiado para ese paciente.
El quinto paso consiste en la
evaluación de las Actividades de la Vida Diaria (AVD)
Siempre en línea con la idea de
utilizar los instruÂmentos más sencillos en la evaluación, se
propone utilizar el índice del estado funcional de pacientes con COVID
denominado Post-COVID Functional Status, a realizar al alta de
internación y luego a 4, 8 y 24 semanas de la externación (PCFS).29
El sexto paso se refiere a la evaluación
de la esfera psicológica, sobre la que existe consenso en el uso del
Cuestionario de Ansiedad y Depresión Hospitalaria (HAD), un instrumento
validado en la lengua española y propuesto la evaluación no
presencial de pacientes con SP.68,72,73
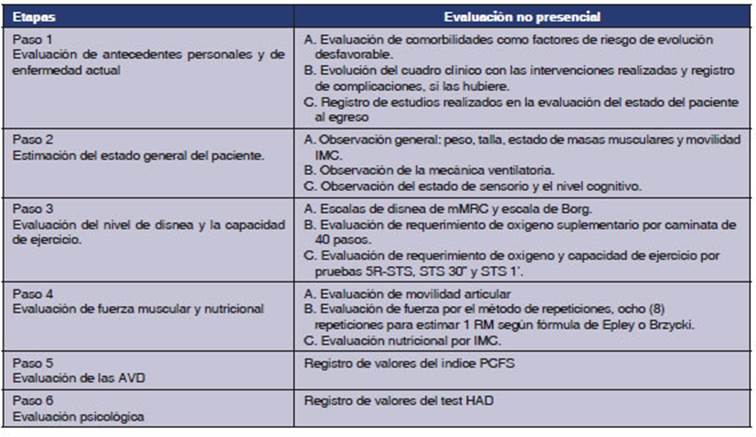
La tabla 2 describe los pasos en la
Evaluación No Presencial de pacientes con COVID-19.
B. Evaluación presencial
de pacientes con síndromes SpC y SP
La evaluación presencial de pacientes
con SpC y SP comparte con la no presencial los pasos iniciales sobre la
información de la epicrisis y la observación general y particular
del paciente.
En el caso de la evaluación de la
disnea y la capacidad de ejercicio, en esta modalidad puede realizarse la PC6M
o el Shuttle Test, tanto para estimar aquellas variables como para identificar
el impacto logrado por la rehabilitación.75
Para la estimación de la FC de
entrenamiento sugerimos la fórmula de Karnoven, que considera los
valores de reposo, la reserva cardíaca y el valor máximo
alcanzado.
Como pruebas necesarias para determinar
qué intensidad de actividad aeróbica va a presÂcribirse se
utilizan el Test Incremental (TI) en cicloergómetro o en cinta
deslizante y el Test de Carga Constante (TCC). El TI es sensible a
intervenciones y tiene implicaciones pronosticas de acuerdo a la severidad del
paciente.75
El TCC es la herramienta más sensible para detectar el
impacto de los PRR sobre patologías respiratorias de diversos
orígenes.75
En la evaluación de la fuerza muscular
y el estado nutricional, la modalidad presencial perÂmite adicionar el uso de
máquinas, pesos libres o implementos de valoración funcional como
cintas de suspensión, esferas, bosús y trabajo con el peso del
propio cuerpo.44,45
En el aspecto del asesoramiento nutricional,
de contarse con el recurso disponible, sería deseaÂble tener una carta
antropométrica que permita analizar los efectos de la
intervención sobre la composición corporal del paciente.
En la evaluación de las AVD se propone
en primera instancia el PCFS, como segunda opción los índices de
Barthel y Katz y como alternativa siguiente los cuestionarios El Short Forme
Course 36 ítems (SF36) y el Cuestionario
Respiratorio de Saint George (SGRQ). Se sosÂtiene
aquí también el cuestionario HAD para la evaluación
psicológica.
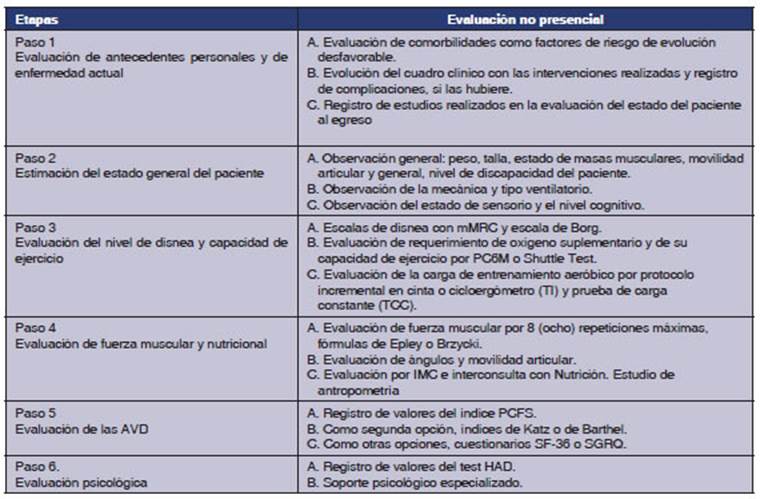
En la tabla 3 se resumen los aspectos de la
reÂhabilitación presencial.
3. ÂŋCómo rehabilitar a un paciente con SpC y SP?
No existe aún un consenso generalizado
sobre cuál es la mejor modalidad para rehabilitar a los pacienÂtes con
SpC y SP. Un concepto merece subrayarse en este apartado.
Diversas publicaciones sugieren qué
tipo de entrenamiento podría realizarse a través de la tele
rehabilitación y de la rehabilitación presencial, e incluyen no
sólo el entrenamiento muscular periférico sino también el
soporte nutricional y psicológico y aspectos concernientes a la
educación del paciente.30,52,53,57,58,63,66-70
A. Rehabilitación
respiratoria en la modalidad no presencial
La Telemedicina ha aportado recomendaciones para el
apartado de la rehabilitación respiratoria, tanto en el caso de un
programa de ejercicios suÂpervisado a distancia por un profesional como en el
caso de un protocolo no supervisado.69,70
Los criterios de exclusión para la
rehabilitación respiratoria no presencial de pacientes con SpC son.69
â Pobre estado cognitivo (Test Mínimo del Estado
Mental igual o menor a 24 puntos).
â Presencia de enfermedad cardíaca o
neurológica inestable.
â Alteraciones severas de la movilidad articular u otros
defectos musculo-esqueléticos que le impidan realizar los gestos
solicitados.
â Pacientes discapacitados que vivan solos y no cuenten
con ayuda alguna.
â Pacientes con trastornos evidentes del equiliÂbrio.
â Pacientes sin conocimientos básicos en el manejo
de dispositivos para el contacto virtual.
A1. Rehabilitación
respiratoria no presencial asincrónica
La información sobre qué tipo de
ejercicio realizar y cómo, se provee a través de videos o
cartillas que deben ser provistas al paciente. De la misma manera, se debe
suministrar una planilla donde figuren los ejercicios a realizar. En esta el
paciente debe registrar en cada uno de los ejercicios indicaÂdos para esa
sesión, el nivel de disnea y fatiga por la escala de Borg que le
generan. De ser posible, también debería registrar el nivel de
SpO2 y FC al final de las series de ejercicios o caminata.44,65,69
Los dos soportes que confluyen con el entreÂnamiento
muscular para sostener este PRR no presencial, son el educativo y el
psicológico.
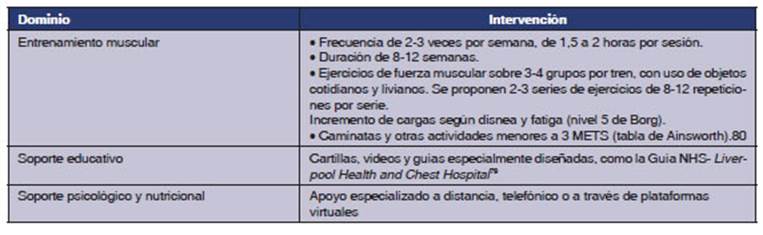
En la tabla 4 se describen los aspectos salientes de esta
modalidad de rehabilitación.44,45,66,69,79,80
A2. Rehabilitación
respiratoria no presencial sincrónica
En esta modalidad el profesional puede suÂpervisar el
trabajo del o de los pacientes de dos maneras.
Por un lado, conectándose en videoconferencia con
grupos de 4-6 participantes y observando cómo se realiza la actividad.
Por otro lado, conectándose individualmente con el paciente y
supervisándolo 2 (dos) veces por semana en la actividad consenÂsuada,
quedando otras dos sesiones semanales a cargo del propio paciente.69
B. Rehabilitación
respiratoria en la modalidad presencial
Al finalizar con la evaluación del paciente, el
profesional debe encontrarse en condiciones de elegir qué modalidad de
entrenamiento es el más apropiado para él o para ella.
B1. Entrenamiento de resistencia aeróbica
Si bien no contamos aún con un protocolo espeÂcífico
para el entrenamiento de esta capacidad en pacientes que han sufrido enfermedad
por COVID-19, se sugieren las modalidades de uso habitual en pacientes con
enfermedades pulmoÂnares intersticiales difusas (EPID), patologías que
suelen tener semejanzas con el daño pulmonar por SARS-CoV-2 y el DAUCI.
En este contexto, puede utilizarse bien la modaÂlidad del
Método Continuo Variable (MCV) como la de Método Intermitente.81
Una reciente actualización realizada por la Base
de Datos Cochrane de Revisiones Sistemáticas soÂbre la RR en las EPID,
incluyó 16 estudios con 357 pacientes con EPID y 319 de grupo control.81
La rehabilitación mejoró la PC6M con una media de 40 (Âą
32,7-47,4) metros, la capacidad de trabajo, el consumo de oxígeno, la
disnea y las AVD medidas por el cuestionario SGRQ y el cuestionario CRQ,
beneficios que en cinco trabajos persistían entre 6-12 meses de
finalizada la intervención.82
B2. Entrenamiento de la fuerza
muscular
Ya sea utilizando el recurso de máquinas de muscuÂlación,
cargas libres o elementos de entrenamiento funcional, el entrenamiento de la
fuerza muscular se puede iniciar con cargas del 50% de la máxima
tolerada en la evaluación, a menudo basada en las fórmulas de
cálculo de 1 RM de Epley o Brzycki, progresando hasta llegar 12
repeticiones y luego 3 series al 80% de la fuerza máxima estimada.44,81,82
B3. Soporte educativo y nutricional
En esta modalidad presencial se recomiendan reÂuniones
educativas sobre aspectos que tienen que ver con las posturas, el manejo de la
disnea y la tos en las AVD, el tipo respiratorio, las técnicas de ahorro
de energía en la realización de los ejercicios físicos, el
uso adecuado de cánulas y máscaras de oxígeno, el
reconocimiento de signos de alarma durante actividades físicas, entre
otros temas de interés.30,44,52,53,55,57,58,63,66,68,69,78,79,81
B4. Soporte psicológico
En esta modalidad presencial, deberá contarse
también con un profesional de Psicopatología familiarizado con la
problemática de estos pacientes.30,44,52,53,55,57,58,63,66,68,69,78,79,81
CONCLUSIONES
El abordaje de pacientes con formas moderadas y graves de
enfermedad por SARS-CoV-2, implica el reconocimiento del aspecto
sistémico de la dolenÂcia, el de su carácter a menudo
incapacitante y su amplia distribución en la comunidad.
En la actualidad, la Rehabilitación Respiratoria
constituye la única intervención que ha demostra do un impacto positivo sobre la disnea y fatiga de los
pacientes, como así también en su calidad de vida y en una
mejoría de la esfera psicológica. A pesar de estos beneficios, la
indicación y/o su imÂplementación se encuentran todavía
fuertemente subestimadas.
Sea cual fuere el nivel de complejidad
médica donde se la inicie, se sugiere que la estrategia sea implementada
de manera temprana y de forma integrada y continua durante los cambios de cada
nivel de atención, y en lo posible con la participaÂción de un
equipo multidisciplinario integrado por kinesiólogos, médicos,
nutricionistas y psicólogos.
La evaluación y el entrenamiento deben
estar centrados en las necesidades y posibilidades del paciente. Esto implica
el reconocimiento previo del ámbito donde continuará la
intervención, es decir, presencial o no presencial; el empleo de técnicas
seguras y sencillas que involucren el uso de objetos cotidianos; el
análisis de las condiciones clínicas del paciente que inicia la
rehabilitación y la factibilidad de la táctica propuesta en
razón de sus conocimientos y los de su entorno. Finalmente, el equipo de
salud debe sostener el respeto de los principios éticos de privacidad,
confidencialidad y el de ser informado sobre las expectativas y los resultados
de la intervención propuesta.
En conclusión, este grupo de trabajo
considera que el rol primero del equipo de rehabilitadores, es el de
constituirse en el puente que promueva la accesibilidad de los pacientes
afectados por SARS-CoV-2, a la única herramienta válida para
minimizar sus secuelas y mejorar su calidad de vida: la Rehabilitación
Respiratoria.
Conflicto de intereses
Los autores no presentan conflictos de
intereses
BIBLIOGRAFÍA
1. Li Q, Guan X, Wu P, et al. Early Transmission Dynamics in Wuhan, China, of Novel
Coronavirus-Infected Pneumonia. N Engl J Med. 2020;382:1199-207.
2. WHO
Director.General opening remarks at the media briefing on COVID-19: 11 March
2020. Published March 11 2020. Disponible en:
https://www.who.int/director-general/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19---11-march-2020
3. John Hopkins
Coronavirus Resource Center. Disponible
en: https://coronavirus.jhu.edu/
4. Las 10 principales causas de
defunción. Disponible en:
https://www.who.int/es/news-room/fact-sheets/detail/the-top-10-causes-of-death
5. Estadísticas-mortalidad. Disponible
en: https://www.argenÂtina.gob.ar/salud/instituto-nacional-del-cancer/estadisticas/
mortalidad
6. Ministerio de Salud de la Nación.
Boletín Integrado de Vigilancia N540 SE 10/2021. Disponible en:
https://bancos.salud.gob.ar/recurso/boletin-integrado-de-vigilancia-n540-
se10-2021
7. Schönfeld D,
Arias S, Bossio JC, Fernández H, GoÂzal D, Pérez-Chada D.
Clinical presentation and outÂcomes of the first patients with COVID-19 in
ArgenÂtina: Results of 207079 cases from a national database. Disponible en:
https://journals.plos.org/plosone/article/authors?id=10.1371/journal.pone.0246793
8. Abate SM, Ahmed
Ali S, Mantfardo B, Basu B. Rate of InÂtensive Care Unit admission and outcomes
among patients with coronavirus: A systematic review and Meta-analysis. PLoSOne 2020;15(7).
https://doi.org/10.1371/journal.pone.0235653
9. Osuchowski MF,
Winkler MS, Skirecki T et al. The COVÂID-19 puzzle: deciphering pathophysiology
and phenotypes of a new disease entity. Lancet Respir Med 2021;9:622-42. https://doi.org/10.1016/S2213-2600(21)00218-6.
10. Hou YJ, Okuda K,
Edwards CE, et al. SARS-CoV-2 reÂverse genetics reveals a variable infection
gradient in the respiratory tract. Cell 2020;182:429-46.e14.
https://doi.org/10.1016/j.cell.2020.05.042
11. Tang X, Du RH,
Wang R, et al. Comparison of hospiÂtalized patients with ARDS caused by
COVID-19 and H1N1. Chest 2020;158:195â205.
https://doi.org/10.1016/j.chest.2020.03.032
12. Ellinghaus D,
Degenhardt F, Bujanda L, et al. Genome wide association study of severe
Covid-19 with respiraÂtory failure. N Engl J Med 2020;383:1522â34.
https://doi.org/10.1056/NEJMoa2020283
13. Yu M, Liu Y, Xu
D, Zhang R, Lan L, Xu H. Prediction of the development of pulmonary fibrosis
using serial thin-section CT and clinical features in patients dis charged
after treatment for COVID-19 pneumonia. Korean J Radiol 2020;21:746â55.
https://doi.org/10.3348/kjr.2020.0215
14. Wilson MS, Wynn
TA. Pulmonary fibrosis: pathogenesis, etiology and regulation. MucosalImmunol 2009;2:103-21. https://doi.org/10.1038/mi.2008.85
15. Akoumianaki E, Dousse N, Lyazidi A, et
al. Can proporÂtional ventilation modes
facilitate exercise in critically ill patients? A physiological cross-over
study: Pressure support versus proportional ventilation during lower limb
exercise in ventilated critically ill patients. Ann Intensive Care 2017;7:64.
https://doi.org/10.1186/s13613-017-0289-y
16. Nydahl P,
Sricharoenchai T, Chandra S, et al: Safety of patient mobilization and
rehabilitation in the intensive care unit. Systematicreviewwith meta-analysis.
Ann Am Thorac Soc 2017;14:766-77.
https://doi.org/10.1513/AnnalsATS.201611-843SR
17. Devlin JW, Skrobik Y, Gélinas C,
et al. Clinical practice guidelines for pain
management, agitation/sedation, delirium, immobility and sleep disturbances in
adult patients in the ICU. PADIS Method Innovations Paper. Crit Care Med
2018;46:1457-63. https://doi.org/10.1097/CCM.0000000000003298
18. Mart MF, Brummel
NE, Ely EW. The ABCDEF Bundle for the Respiratory Therapist. Respir Care. 2019;64:1561-73.
https://doi.org/10.4187/respcare.07235
19. Stiller K,
Phillips A. Safety aspects of mobilising acutely ill inpatients. Physiother
Theory Pract 2003;19:239-57. https://doi.org/10.1080/09593980390246751
20. Jones PW, Bestall
JC. Modified Medical Research CounÂcil scale. Thorax 1999;54:581-6.
https://doi.org/10.1136/thx.54.7.581
21. Medical Research
Council of the UK, Aids to the investiÂgation of Peripheral Nerve Injuries,
Memorandum No.45. London, Pendragon House
1976: 6-7.
22. Ely E, Truman B,
Shintani A, et al. Monitoring SeÂdation Status Over Time in ICU Patients:
Reliability and Validity of the Richmond Agitation-Sedation Scale (RASS). JAMA 2003;289:2983-91.
https://doi.org/10.1001/jama.289.22.2983
23. Latorre Marco, M. Solís
Muñoz, T. Falero Ruiz, et. al. ValidaÂtion
of the Scale of Behavior Indicators of Pain (ESCID) in critically ill,
non-communicative patients under mechanical ventilation: results of the ESCID
scale. Enferm Intensiva 2011;22:3-12.
24. Ely EW, Inouye SK,
Bernard GR, et al. Delirium in MeÂchanically Ventilated Patients. Validaty and
Reliability of the Confusion Assessment Method for the Intensive Care Unit
(CAM-ICU). JAMA 2001;286:2703-10. https://doi.org/10.1001/jama.286.21.2703
25. Morris PE, Goad
A, Thompson C, et al. Early intensive care unit mobility therapy in the
treatment of acute respiraÂtory failure. Crit Care Med 2008;36:2238-43.
https://doi.org/10.1097/CCM.0b013e318180b90e
26. Moss M,
Nordon-Craft A, Malone D, et al. A randomized trial of an intensive physical
therapy program for patients with acute respiratory failure. Am J Respir Crit
Care Med 2016;193:1101-10. https://doi.org/10.1164/rccm.201505-1039OC
27. Ortiz Calderón M, Páez
Pineda O. Prevención y Manejo del desacondicionamiento físico en
el paciente hospiÂtalizado por Covid-19. Ed: Universidad Pedagógica y
Tecnológica de Colombia. Versión electrónica. Colombia.
Julio 2020.
28. Fuke R, Hifumi T, Kondo Y, et al. Early rehabilitation to preÂvent post intensive care
syndrome in patients with critical illness: A systematic review and
meta-analysis. BMJ Open 2018;8:1-10.
https://doi.org/10.1136/bmjopen-2017-019998
29. Klok FA, Boon
GJAM, Barco S, et al. The Post-COVID-19 Functional Status scale: atool to
measure functional status over time after COVID-19. Eur Respir J
2020;56:2001494. https://doi.org/10.1183/13993003.01494-2020
30. Barker-Davies R,
OâSullivan O, Senaratne K, et al. The Stanford Hall consensus statement for
post-COVID-19 rehabilitation. Br J Sports
Med. 2020:54:949-59. https://doi.org/10.1136/bjsports-2020-102596
31. Hong Mei Z, Yu
Xiao X, Chen W. Recommendations for reÂspiratory rehabilitation in adults with
coronavirus disease 2019. Chin Med J (Engl) 2020;133:1595-602.
https://doi.org/10.1097/CM9.0000000000000848
32. Wang T, Chau B,
Lui M, et al. Physical Medicine and RehaÂbilitation and Pulmonary
Rehabilitation for Covid-19. Am J Phys Med Rehabil. 2020;99:769-74.
https://doi.org/10.1097/PHM.0000000000001505
33. Stiller K,
Phillips A. Safety aspects of mobilising acutely ill inpatients. Physiother
Theory Pract 2003;19:239-57. https://doi.org/10.1080/09593980390246751
34. Díez
Burón F, Marcos Vidal JM, Baticón PM. Concordancia entre la escala verbal numérica y la
escala visual analógica en el seguimiento del dolor agudo postoperatorio.
Rev Esp Anestesiol Reanim 2011;5:279-82.
https://doi.org/10.1016/ S0034-9356(11)70062-7
35.
Núñez-Cortés R, Rivera-Lillo G, Arias- Campoverde M. Use
of sit-to-stand test to assess the physical capacity and exertional
desaturation in patients post COVID-19. Chron Respir Dis.
2021;18:1479973121999205. https://doi.org/10.1177/1479973121999205
36. Maddocks M, Nolan
CM, Man WD. Man. Simple functionÂaltests in COPD: stand up and be counted! Eur
Respir J 2017;49:1700104. https://doi.org/10.1183/13993003.00104- 2017.
37. Beauchamp MK,
Hill K, Goldstein RS, et al. Impairments in balance discriminate fallers from
non-fallers in COPD. Respir Med.
2009;103:1885-91. https://doi.org/10.1016/j.rmed.2009.06.008
38. Kon SS, Canavan JL, Nolan CM. The 4 metregait speed in COPD: responsiveness and
minimal clinically important difference. Eur Respir J. 2014;43:1298-305.
https://doi.org/10.1183/09031936.00088113
39. Mador MJ , Mogri
M , Patel A. Contractile fatigue of the quadriceps muscle predicts improvement
in exercise perÂformance after pulmonary rehabilitation. J Cardiopulm Rehabil Prev. 2014;34:54-61.
https://doi.org/10.1097/HCR.0000000000000023
40. Ehlenz H, Grosser M, Zimmerann E. La
Resistencia desde una Perspectiva Práctica del Entrenamiento. En: EntreÂnamiento
de la Fuerza. 2º ed. Ed. Martínez Roca S.A. 1990, p 103-11.
41. Boeckh-Behrens WU, Buskies W. Control del
esfuerzo según el porcentaje de la fuerza máxima. En:
Entrenamiento de la Fuerza. Editorial Paidotribo. Barcelona España
año 2005, p 64-69
42. Mahoney FI,
Barthel DW. Functional evaluation: the BarthÂel index. Md Med J. 1965;14:61-65.
https://doi.org/10.1037/t02366-000
43. Katz S, Ford A,
Moskowitz R, Jackson B, Jaffe M. StudÂies of illness on the aged. The index of
ADL: a stanÂdardized measure of biological and psychological funcÂtion. JAMA 1963;185:914-9.
https://doi.org/10.1001/jama.1963.03060120024016
44. Rodríguez Núñez I,
Torres Castro R, Vera R. Consenso de Rehabilitación Respiratoria en
pacientes con CoÂvid-19. Sociedad Chilena de Kinesiología Respiratoria
(SOCHIKIR). Chile. Agosto 2020. https://doi.org./10.13140/RG.2.2.16594.17607/1
45. Saadia Otero MA. El Entrenamiento
Físico en la RehaÂbilitación Respiratoria, un Programa Diferente.
Editorial Académica Española. 2017 p 16-19.
46. Vega ML, Sirotti C, Montiel G, et al.
Recomendaciones para el manejo invasivo y no invasivo de la insuficiencia respiÂratoria
hipoxémica por COVID-19. Número especial de la Revista Educativa
de ALAT. Asociación Latinoamericana de Tórax, ALAT. Mayo 2020
47. Bowers R, Fox E. Procesos de
recuperación. En: Fisiología del Deporte. 3o ed. México.
Editorial Médica Panamericana, 1998 p 54-69.
48. Zintl F. Conceptos fundamentales de la
teoría del entreÂnamiento. En: Entrenamiento de la Resistencia â FunÂdamentos,
métodos y dirección del entrenamiento. 2o ed. Barcelona,
España Editorial Martínez Roca, S.A. 1991 p 110-113
49. Peña G, Heredia Elvar JR, Moral S,
Mata F y Marzo Edir Da Silva G. Evidencias sobre los Efectos del Entrenamiento
Inestable para la Salud y el Rendimiento. PubliCE Standard. 2012
50. Willardson JM.
Core Stability Training: applications to sports conditioning programs. J Strength Cond Res 2007;21:979-85.
https://doi.org/10.1519/00124278-200708000-00054
51. Fajardo J. ÂŋQué es la
musculación y dónde ubicarla? Nuevas Tendencias en Fuerza y
Musculación, 1 ed. Autor Editor Julio Tous Fajardo, 1999, p 37-5
52. Societat Catalana de Medicina Familiar i
Comunitària (CAMFiC). Manifestaciones Persistentes de la Covid-19.
Guía de Práctica Clínica. Edición 2020.
53. Guía Clínica para la
atención del paciente Long COVID/COVID
Persistente, 1-5-2021. Documento colaborativo enÂtre colectivos de pacientes y
sociedades científicas. Versión 1.0. Fecha: 1-5-2021.
54 Patient-Led Research
Collaborative. Report: What Does COVID-19 Recovery Actually Look Like? An
Analysis of the Prolonged COVID-19 Symptoms Survey by Patient-Led R Research
Team. Disponible en: https://patientresearchcoÂvid19.com/research/report-1/.
55. Greenhalgh, T, Knight M,
AâCourt M, Buxton M, Husain L. Management of post-acute COVID-19 in primary
care. BMJ 2020;370:m3026. https://doi.org/10.1136/bmj.m3026.
56. Fernández-de-Las-Peñas C,
Palacios-Ceña D, Gómez- Mayordomo V, Cuadrado ML, Florencio LL. Defining post-COVID symptoms (post-acute COVID, long COVID, persistent
post-COVID): An integrative classification. Int J Environ Res Public Health.
2021;18:2621. https://doi.org/10.3390/ijerph18052621.
57. National Institute for Health
and Care Excellence, PractiÂtioners of RC of G, Scotland HI. COVID-19 rapid
guideline: managing the long-term effects of COVID-NICE Guide (Internet) 2020;
18 December 2020: 1-35. Disponible en:
https//www.nice.org.uk/guidance/ng188/resources/covid19-rapid-guidance-managing-the-longterm-effects-of-covid19-pdf66142028400325.
58. Rajan S, Khunti K, Alwan N et
al. In the way for the panÂdemic preparing for long COVID (Internet) HEALTH SYSÂTEMS
AND POLICY ANALYSIS POLICY 2020. Cited 2021 Mar 12. Disponible
en:https://apps.who.int/iris/bitstream/ handle/10665/339629/Policy-brief-39-1997-8073-eng.pdf.
59. Maltezou H, Pavli A, Tssakris
A. Post-COVID Syndrome: An Insight on Its Pathogenesis. Vaccines 2021;9:497.
https://doi.org/10.3390/vaccines9050497.
60. Lopez-Leon S, Wegman-Ostrosky
T, Perelman C, et al. More than 50 Long-term effects of COVID-19: a systematic
review and meta-analysis. medRxivpreprintdoi:
https://doi.org/10.1101/2021.01.27.21250617.
61. Davis HE, Assafi GS,
McCorkelli L, et al. Characterizing Long COVID in an International Cohort: 7
Months of Symptoms and Their Impact. 2021:101019
https://doi.org/10.1101/2020.12.24.20248802
62. Sociedad Española de Médicos Generales
y de Familia (SEMG). Colectivo de pacientes Long COVID (ACTS). Encuesta de
síntomas y discapacidad producida por los misÂmos, en los afectados por
COVID persistente. Disponible en:
https://www.semg.es/images/2020/Noticias/20201111_ReÂsultados_Encuesta_COVID_Persistente.pdf.
63. Documento intersociedades. Desafío pospandemia
COVID. Recomendaciones para la rehabilitación pos COVID19. Ministerio de Salud y Bienestar Social, Argentina.
64. Sudre C, Murray B, Varsasky
t, et al Attributes and predicÂtors of Long-COVID: analysis of COVID cases and
their symptoms 2 collected by the Covid Symptoms Study App.
https://doi.org/10.1101/2020.10.19.20214494.
65. Greenhalgh T, Javid B, Knight
M, et al. What is the efficacy and safety of rapid exercise tests for
exertional desaturaÂtion in covid-19? Oxford COVID-19 Evidence Service. 2020
https://www.cebm.net/covid-19/what-is-the-efficacy-and-safety-of-rapid-exercise-tests-for-exertional-desaturation-in-covid-19/
66. Spruit MA, Holland AE, Singh
SJ, Tonia T, Wilson KC, Troosters T. COVID-19: interim guidance on
rehabilitation in the hospital and post-hospital phase from a European
Respiratory Society- and American Thoracic Society-coordinatÂed international
task force. Eur Respir J 2020;56:2002197.
https://doi.org/10.1183/13993003.02197-2020].
67. Brennan D, Tindall L,
Theodoros D, et al. A blueprint for telerehabilitation guidelines.
International journal of telerehabilitation 2010;2:31-4.
https://doi.org/10.5195/ ijt.2010.6063
68. Vitacca M, Lazzeri M,
Guffanti E et al. An Italian conÂsensus on COVID-19 patients recovering from
acute respiratory faillure : results of a Delphy process. Monaldi Arch Dis
2020;90:1444:385-93. https://doi.org/10.4081/ monaldi.2020.1444
69. Agency for Clinical
Evaluation. NSW Governement. DeÂlivering pulmonary rehabilitation via
Telehealth during COVID-19. Virtual PuRe. April
2020. Disponible en: www.aci.health.nsw.gov.au.
70. Almonacid C, Plaza V. Guía SEPAR para la
teleconsulta de pacientes respiratorios. Disponible
en:https://www.separ.es/node/1974.
71. Vaidya T, Chambellan A, De
Bisschop C. Sit-to-Stand Test on COPD: A literature review. Resp Med
2017;128:70-7. https://doi.org/10.1016/j.rmed.2017.05.003
72. Quintana JM, Padierna A,
Esteban C, ArosteguiI, Bilbao A, Ruiz I. Evaluation of the psychometric
characteristics of the Spanish version of the Hospital Anxiety and Depression
Scale. Acta Psychiatr Scand 2003;107:216â21. https://doi.org/10.1034/j.1600-04472003.00062.x
73. Terol Cantero MC, Cabrera Perona V,
Martín-Aragón M. Revisión de estudio de la Escala de
Ansiedad y Depresión Hospitalaria (HAD). Anales de Psicología 2015;31:494-503.
http://dx.doi.org/10.6018/analesps.31.2.172701.
74. ATS Committee on Proficiency
Standards for CliniÂcal Pulmonary Function Laboratory. ATS statement:
guidelines for six minute walk test. Am J Respir Crit Care Med.
2002;166:111-17. https://doi.org/10.1164/ ajrccm.166.1.at1102
75. Puente-Maestu LP, PalangeP, Casaburi R et al. Use of exerÂcise testing in the evaluation of interventional efficacy :
an official ERS statement. Eur Resp J
2016;47:429-60. http://dx.doi.org/10.1183/13993003.00745-2015.
76. Alonso J, Prieto L, Anto JM. La versión
española del SF-36 HealthSurvey (Cuestionario de Salud SF-36): un instruÂmento
para la medida de los resultados clínicos. Med Clin (Barc). 1995;104:771-6
77. Jones PW, Quirk FH,
Baveystock CM. The St Georgeâs reÂspiratory questionnaire. Respir Med 1991;85:25-31. https://doi.org/10.1016/S0954-6111(06)80166-6
78. Curci C, Pisano F, Bonacci E, Camozzi DM, Ceravolo C,
BerÂgonzi R, et al. Early rehabilitation in
post-acute COVID-19 patients: data from an Italian COVID-19 Rehabilitation Unit
and proposal of a treatment protocol. Eur J Phys Rehabil Med 2020;56:633-41.
http://dx.doi.org/10.23736/S1973-9087.20.06339-X.
79. Liverpool Heart and Chest
Hospital. NHS Foundation Trust. COVID-19 Patient Rehabilitation Guide. https://www.lhch.nhs.uk/media/7300/covid19-rehabilitation-guide.pdf.
80. Ainsworth B, Haskell W,
Herrmann S et al. 2011 Compendium of Physical Activities: a second update of
codes and MET values. http://dx.doi.org/10.1249/MSS.0b013e31821ece12.
81. Capparelli I, Saadia Otero M,
Steimberg J, et al. RehabiliÂtación respiratoria
en pacientes con enfermedad pulmonar intersticial difusa, experiencia de un
hospital especializado de Argentina. Rev Am Med Resp 2019;19:291-7.
82. Dowman L, Hill CJ, May A, Holland A.
Rehabilitación pulmonar para la enfermedad pulmonarintersticial.
Disponible
en:https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD006322.pub4/full/es.