Autor Palmero Domingo1,2, Lagrutta Laura1,2, Aidar Omar1,2, Bartoletti Bruno1, Cruz VĂctor1, Gamberale Ana1, GarcĂa Ana1 , González Montaner Pablo1,2, Inwentarz Sandra2, Vescovo Marisa1,2
1Hospital de Infecciosas Dr. F. J. Muñiz, Ciudad AutĂłnoma de Buenos Aires, Argentina 2Instituto de TisioneumonologĂa Prof. Dr. RE. Vaccarezza, Ciudad AutĂłnoma de Buenos Aires, Argentina
Correspondencia : Domingo Palmero E-mail: djalmero@intramed.net
RESUMEN
La
emergencia de cepas resistentes de Mycobacterium
tuberculosis a múltiples drogas, las dificultades de su
diagnóstico y tratamiento constituyen un desafío a la salud
pública mundial. Para afrontar esta situación, se emplean nuevas
drogas antituberculosis, como bedaquilina,
pretomanid y delamanid,
así como drogas repropuestas, como fluoroquinoÂlonas, linezolid y clofazimina. Con base en la evidencia brindada por estudios
multicénÂtricos, se han descubierto
fármacos asociados a un mejor pronóstico de la tuberculosis drogorresistente y, recientemente, se ha propuesto una
nueva clasificación, así como nuevos esquemas totalmente orales.
En esta revisión, describimos los esquemas de tratamiento actuales y los
aspectos farmacológicos prácticos necesarios a la hora de la
prescripción de los nuevos regímenes de tratamiento de la
tuberculosis drogorresistente.
Palabras
clave:
Tuberculosis, Drogorresistencia, TB-MDR,
Farmacología
ABSTRACT
The emergence of resistant strains of Mycobacterium tuberculosis to multiple drugs and the difficulties of their diagnosis and treatment constitute a challenge to global public health. To face this challenge,
new anti-tuberculosis drugs, such
as bedaquiline, pretomanid,
and delamanid, as well as replacement drugs, such as fluoroquinolones, linezolid and clofazimine, are used. Based on
the evidence provided by multicenter
studies, drugs associated with a better prognosis of drug-resistant
tuberculosis have been discovered and, recently, a new classification has been proposed, as well as new totally oral regimens. In this review, we
describe current treatment regimens and practiÂcal pharmacological aspects required when prescribing
new drug-resistant tuberculosis treatment
regimens.
Key words:
Tuberculosis, Drug-resistance; MDR-TB, Pharmacology
Recibido: 09/12/2021
Aceptado: 12/02/2022
INTRODUCCIÓN
La
amenaza global de la tuberculosis drogorresisÂtente
(TB-DR) ha promovido la investigación de nuevos esquemas
terapéuticos, nuevos fármacos y fármacos repropuestos1 (no
comercializados originalmente para TB, como fluoroquinolonas,
linezolid y clofazimina)
junto con las drogas traÂdicionalmente llamadas de segunda línea con el
objetivo de mejorar la eficacia del tratamiento de estas formas de la
enfermedad.
El
objetivo de esta revisión es analizar brevemenÂte los esquemas actuales
de tratamiento según norÂmas internacionales y describir las dosis en
adultos y niños, mecanismos de acción, reacciones adversas y uso
en insuficiencia renal, hepática, embarazo y meningitis tuberculosa de
los fármacos disponibles para tratar la TB drogorresistente.
Una revisión amplia de la TB-DR puede encontrarse en2.
Existen
diferentes categorías de TB-DR, que deÂfinimos a continuación3-5. TB monorresistente es la provocada por cepas de Mycobacterium tuberculosis (Mtb) resistente a una sola droga, son las de mayor
preocupación la monorresistencia a isoniacida (rH) y a rifampicina (rR); TB multidrogorresistente (TB-MDR) es aquella en que se observa
resistencia como mínimo a isoniacida (H) y rifampicina (R); la TB preextensamente
resistente (TB pre-XDR) agrega a la MDR la resistencia a por lo menos una de
las fluoroquinolonas antituberculosis
(levofloxacina o moxifloxacina);
por último, la TB extensamente resistente (TB-XDR) adiciona a la pre-XDR
la resisÂtencia como mínimo a bedaquilina o linezolid (grupo A de la Organización Mundial de la
Salud, OMS).
En
2018, OMS publica una nueva clasificación de las drogas a utilizar en
TB-DR, actualizada en 20206 (Tabla
1) y basada en el metaanálisis de datos de
pacientes individuales con TB-MDR publicado por Ahmad y cols.7
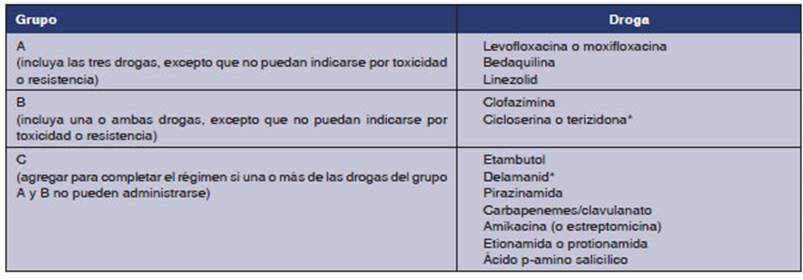
Esquemas de tratamiento
de la TB resistente a isoniacida, rifampicina
y multidrogorresistente
El
tratamiento recomendado por las guías interÂnacionales de la TB-rH es un esquema de 6 meses con cuatro drogas, sin fase
inicial: levofloxacina, piÂrazinamida,
rifampicina y etambutol. La
duración del tratamiento está determinada por la necesidad de
completar 6 meses de levofloxacina6,
8.
La
TB-rR es una categoría que surgió a
partir del advenimiento del método molecular rápido de
diagnóstico denominado Xpert Mtb RIF, que detecta en el Mtb,
con una especificidad cercana al 100%, la presencia de las cinco mutaciones
más frecuentes del gen RpoB que
explican la resistencia a R.9 Cómo
aproximadamente un 80% de las cepas rR presentan
resistencia adicional a H10 y,
además, se ha perdido una droga central en el tratamiento de la TB, se
recomienda tratar la TB-RR como MDR6,
8.
La
TB-MDR, de acuerdo a las nuevas recomenÂdaciones puede tratarse con un esquema
100% oral que incluya las tres drogas del grupo A de OMS (bedaquilina,
linezolid, fluoroquinolona),
junto con una o dos del grupo B (cicloserina o clofazimina). La bedaquilina se
administra los primeros 6 meses (véase Tabla 2) y las otras tres o
cuatro drogas durante todo el tratamiento, que dura en total 18 meses (puede
acortarse en formas mínimas). Las drogas del grupo C quedarían
como reemplazo de las de los grupos A y B en caso de no poder utilizarlas por
reacciones adversas o resistencia6,
8.
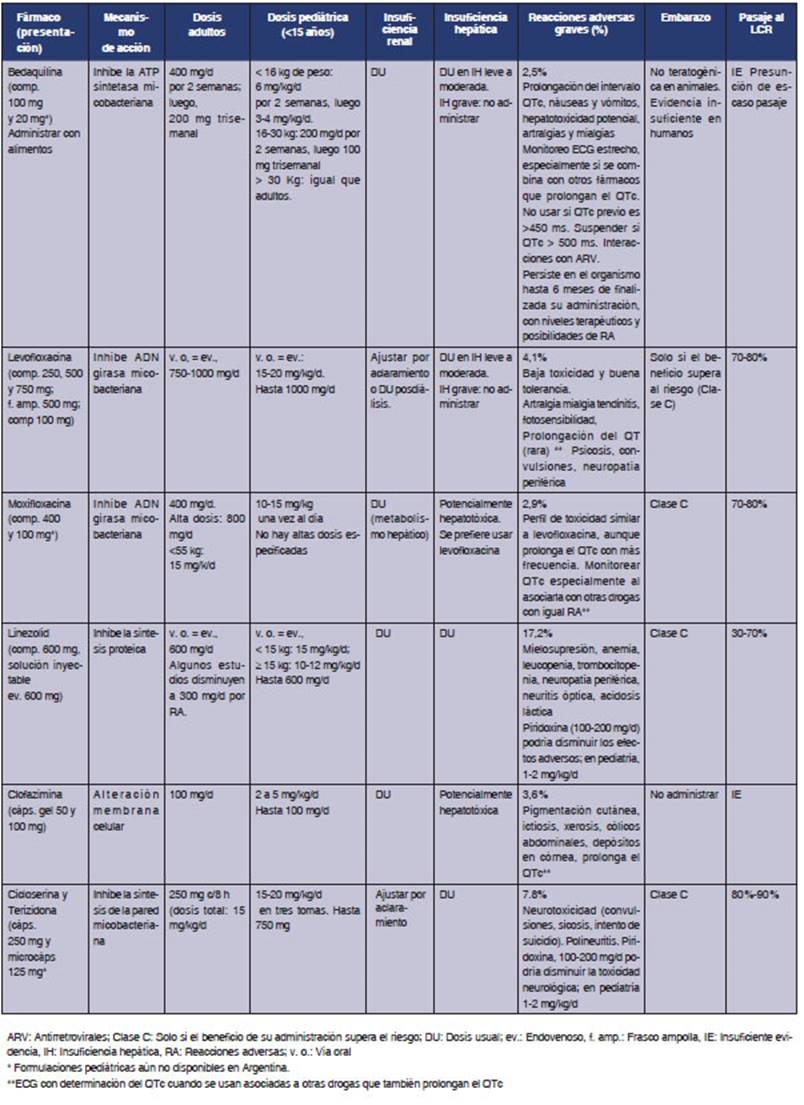
Drogas
alternativas a isoniacida y rifampicina
a utilizar en el tratamiento de la TB-drogorresistente
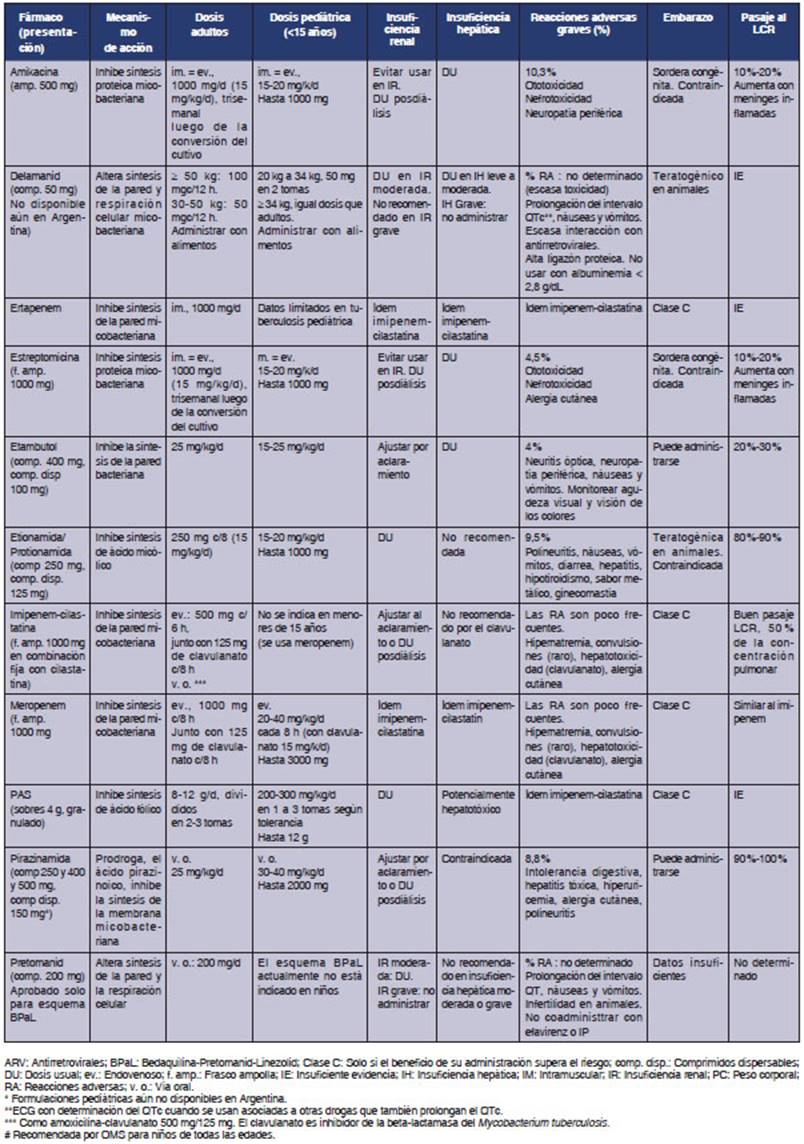
En las Tablas 2 y 3, describimos cada fármaco, su mecanismo
de acción, dosificación en adultos y niños, reacciones
adversas más frecuentes, su uso en insuficiencia renal y
hepática, embarazo y el pasaje al LCR, elemento fundamental en el
tratamiento de la meningits TB.
Tratamiento
de la TB-XDR11-13
Como vimos en su definición, implica la resistencia como
mínimo a H, R, una fluoroquinolona (levo o moxifloxacina) y bedaquilina o linezolid. A partir de esa base mínima de la
definición (que ya crea una situación complicada, pero deja
opciones teraÂpéuticas) la resistencia puede extenderse a prácÂticamente
todos los fármacos anti-TB. Además, el antibiograma en pacientes multitratados no correÂlaciona tan bien con la
clínica como en la TB-MDR y es más frecuente encontrar discordancias
entre los métodos fenotípicos y genotípicos. Por lo tanto,
es importante realizar un detallado interrogatorio a los pacientes sobre los
tratamientos previos y la respuesta bacteriológica y clínica.
Resumiendo, el diseño de un esquema para TB-XDR es artesanal y no pueden
brindarse guías como en las otras formas de TB-DR. Se indican esquemas
con las drogas a las que pueda persistir sensibilidad en el antibiograma
más aquellas que no fueron utilizaÂdas previamente, tratando de reunir
un número mínimo de fármacos posiblemente eficaces (3 o
4). En un intento por mejorar el pronóstico de estos pacientes, se ha
utilizado la asociación bedaquiÂlina-delamanid,
así como bedaquilina durante un año de
tratamiento. Nuevos esquemas como el BPaL (bedaquilina, pretomanid y linezolid) aportarán evidencia sobre la eficacia del
nuevo fármaco pretomanid en estas
circunstancias14.
El pronóstico de estos pacientes es peor que otras formas de TB-DR.
CONCLUSIONES
En esta breve reseña de los aspectos farmacológicos
prácticos de las drogas para el tratamiento de la TB-DR en adultos y
pediatría, exponemos fármaÂcos (como bedaquilina,
delamanid y pretomanid) que
fueron investigados específicamente como drogas antituberculosis,
hecho que no ocurría desde el descubrimiento de la rifampicina,
medio siglo atrás. Es un hecho auspicioso, junto con la evidencia que
demuestra la actividad de drogas que permiten un tratamiento 100% oral en
adultos y niños. Existe disponibilidad de esquemas basados en la
evidencia publicada para el tratamiento de la TB monorresistente
y multirresistente. LamenÂtablemente, la TB-XDR, que
es la situación de resistencia micobacteriana
más grave, continúa siendo un problema complejo tanto en sus
aspectos terapéuticos como pronósticos.
Conflicto de intereses
Los autores declaran no tener conflictos de intereses en
relación con esta publicación.
BIBLIOGRAFÍA
1. Rossato Silva D, Dalcolmo
M, Tiberi S, et al. New and repurposed
drugs to treat multidrug- and extensively drug-resistant tuberculosis. J Bras
Pneumol. 2018; 44: 153-60.
https://doi.org/10.1590/S1806-37562017000000436
2. Palmero DJ, Lagrutta L, Inwentarz SJ, Vescovo M, Aidar OJ, González Montaner PJ. Tratamiento de la
tuberculosis drogorresistente en adultos y
niños. Revisión narrativa. Medicina (Buenos Aires). 2021. E-pub:
https://www.meÂdicinabuenosaires.com/adelantos/
3. Organización Mundial de la Salud (OMS). Definiciones y
marco de trabajo para la notificación de Tuberculosis-revisión
2013 (actualizado en diciembre de 2014). WHO/ HTM/TB/2013.2. ISBN 978 92 4
350534 3.
4. World Health
Organization (WHO). Meeting report
of the WHO expert consultation on the definition of extensively drug-resistant
tuberculosis, 27-29 October 2020. Geneva: World Health Organization;
2021. CC BY-NC-SA 3.0 IGO. En:
https://www.who.int/publications/i/item/meeting-report-of-the-who-expert-consultation-on-the-definition-of-extensively-drug-resistant-tuberculosis
5. Roelens M, Migliori
GB, Rozanova L, et al. Evidence-based
Definition for Extensively Drug-resistant Tuberculosis.
Am J Respir Crit Care Med. 2021; 204): 713-22.
https://doi.org/10.1164/rccm.202009-3527OC.
6. WHO. Consolidated guidelines
on tuberculosis. ModÂule 4: treatment
- drug-resistant tuberculosis treatÂment.
Geneva: World Health Organization; 2020. CC BY-NC-SA 3.0 IGO. En:
https://www.who.int/publications/i/item/9789240007048
7. Ahmad N, Ahuja SD, Akkerman OW, et al. Collaborative
Group for the Meta-Analysis of Individual Patient Data in MDR-TB treatment–2017.
Treatment correlates of successful outcomes in pulmonary multidrug-resistant
tuberculosis: an individual patient
data meta-analysis. Lancet.
2018; 392: 821-34. https://doi.org/10.1016/S0140-6736(18)31644-1
8. Nahid P, Mase SR, Migliori
GB, et al. Treatment of Drug-
Resistant Tuberculosis. An Official ATS/CDC/ERS/IDSA Clinical
Practice Guideline. Am J Respir Crit Care
Med. 2019; 200: e93-e142.
https://doi.org/10.1164/rccm.201909-1874ST.
9. WHO. WHO consolidated guidelines on tuberculosis.
Module 3: diagnosis – rapid diagnostics
for tuberculosis detection.
2020. CC BY-NC-SA 3.0 IGO. En:
https://www.who.int/publications/i/item/9789240029415185
10.
WHO. Global tuberculosis report 2021. Geneva: World Health Organization;
2021. CC BY-NC-SA 3.0 IGO. En: https://www.who.int/publications/i/item/9789240037021
11.
Hewison C, Bastard M, Khachatryan N, et al. Is 6 months of bedaquiline enough? Results from the compassionÂate
use of bedaquiline in Armenia
and Georgia. Int J Tub Lung Dis. 2018;22:766-72.
https://doi.org/10.5588/ijtld.17.0840
12.
Conradie F, Diacon AH, Ngubane N, et al. Nix-TB Trial Team. Treatment of Highly Drug-Resistant Pulmonary Tuberculosis. N Engl J Med. 2020; 382: 893-902.
https://doi.org/10.1056/NEJMoa1901814
13.
Pecora F, Dal Canto G, Veronese P, Esposito S. Treatment
of Multidrug-Resistant and Extensively
Drug-Resistant Tuberculosis in Children:
The Role of Bedaquiline and
Delamanid. Microorganisms.
2021; 9: 1074. https://doi.org/10.3390/microorganisms9051074
14.
Conradie F, Everitt D, Olugbosi M, et al. High rate of successful outcomes treating highly resistant TB in the ZeNix study of pretomanid, bedaquiline and alternative doses and durations
of linezolid. Abstract
OALB01LB02. 11th IAS Conference on
HIV Science Abstract Supplement JIAS 2021;24(S4):e25755-Page
70 En: https://onlinelibrarywiley.com/doi/epdf/10.1002/jia2.25755; consultado
octubre 2021.
15.
Sentinel project.
Management of Drug-Resistant TuberÂculosis in Children: A Field Guide. Boston,
USA: The Sentinel Project for Pediatric Drug-Resistant
Tuberculosis; November 2018, Fourth
edition. En:
http://sentinel-project.org/2019/04/10/sentinel-field-guide/; consultado
octubre 2021.
16.
Dheda K, Gumbo T, Maartens G, et al. The epidemiology, pathogenesis, transmission, diagnosis, and management
of multidrug-resistant, extensively
drug-resistant, and incurÂable tuberculosis. Lancet Respir Med.
2017; S2213-2600: 30079-6. v https://doi.org/10.1016/S2213-2600(17)30079-6
17.
WHO. Companion Handbook to the WHO Guidelines for the Programmatic
Management of Drug-Resistant TuberÂculosis. Geneva: World Health Organization;
2014. WHO/ HTM/TB/2014.11. En:
https://apps.who.int/iris/bitstream/handle/10665/130918/9789241548809_eng.pdf;
consultado octubre 2021.
18.
Lange C, Dheda K, Chesov D, Mandalakas AM, Udwadia Z, Horsburgh CR Jr.
Management of drug-resistant tuberÂculosis. Lancet. 2019; 394: 953-66. https://doi.org/10.1016/S0140-6736(19)31882-3.
19.
Huynh J, Marais BJ. Multidrug-resistant tuberculosis infection
and disease in children: a review of new and reÂpurposed drugs. Ther Adv
Infect Dis. 2019; 6: 1-16.
https://doi.org/10.1177/2049936119864737.
20.
WHO. Rapid communication on
updated guidance on the management
of tuberculosis in children and adolescents.
Geneva: World Health Organization; 2021. Licence: CC
BY-NC-SA 3.0 IGO. En: https://www.who.int/publications/i/item/9789240033450
21.
Seddon JA, Wilkinson R, van
Crevel R, et al. Knowledge
gaps and research priorities
in tuberculous meningitis. Wellcome
Open Res. 2019; 4: 188. https://doi.org/10.12688/wellcomeopenres.15573.1
22.
Wilkinson RJ, Rohlwink U, Misra UK, et al. Tuberculous
Meningitis International Research Consortium:
TubercuÂlous meningitis. Nat
Rev Neurol. 2017;
13: 581-98. https://doi.org/10.1038/nrneurol.2017.120.
23.
Palmero D, González Montaner P, Cufré
M, García A, VescoÂvo M, Poggi
S. First series of patients
with XDR and pre- XDR TB treated
with regimens that included meropenen-clavulanate
in Argentina. Arch Bronconeumol. 2015; 51: e49-52. https://doi.org/10.1016/j.arbres.2015.03.012
24.
Tiberi S, D’Ambrosio L, De
Lorenzo S, et al. Ertapenem in the
treatment of multidrug-resistant
tuberculosis: first clinical
experience. Eur Respir J. 2016; 47: 333-6.
https://doi.org/10.1183/13993003.01278-2015