Autor : Samolski Daniel1
1 OrganizaciĂłn de Servicios Directos Empresarios (OSDE), NeumonologĂa, Buenos Aires, Argentina
Correspondencia :Daniel Samolski - E-mail: dsamolski@gmail.com
Resumen
La neumonía por COVID-19 genera tanto daños
inmediatos por efecto viral como alejados por desregulación
inmunológica inflamaÂtoria. La corticoterapia
sistémica ha demostrado ser beneficiosa en la primer
parte del proceso, pero aún se desconoce con certeza su utilidad
en el daño post agudo. El número de pacientes afectados hace
imperativo encontrar terapéuticas que reduzcan las potenciales secuelas
pulmonares. Se incluyeron en esta serie de casos 18 pacientes internados en
instituciones médicas privadas polivalentes de la Ciudad de Buenos
Aires: 15 de sexo masculino y 3 femenino y edad 58,4 ± 13,6 años.
Antecedentes comórbidos más frecuentes:
HTA (4 pacientes), obesidad (6 pacientes) y tabaquismo (4 pacientes). Cinco
pacientes no presentaban ningún antecedente médico. Todos los
incluidos presentaron disnea, desaturación de
oxígeno y alteraciones tomográficas
persistentes o en progresión, posteriores a los 14 días de su
infección. Todos recibieron dexametasona
acorde a las normativas vigentes. Posteriormente, dada la mala evoluÂción,
fueron tratados con corticoesteroides orales y/o
endovenosos aplicando el tratamiento utilizado para neumonía organizada
(OP) secundaria. En 6 de los pacientes se realizó biopsia transbronquial describiéndose patron
OP en 3 de ellos. Cuatro semanas después de iniciado dicho tratamiento
todos los pacientes presentaron mejoría clínica expresada por
menor disnea, ningún paciente mantuvo el requerimiento de oxígeno
y todas las tomografías de tórax mostraron clara
disminución de la afectación parenquimatosa pulmonar. Los
corticoides sistémicos administrados en el periodo post agudo de la
COVID-19 tienen un efecto beneficioso clínico y radiológico.
Palabras clave: Neumonía por COVID 19,
Neumonía organizada secundaria, Corticoterapia
sistémica
Recibido: 30/06/2021
Aceptado: 13/09/2021
Abreviaturas
COVID-19 Infección por coronavirus SARS COV2
NYHA New York Health Association
O2 oxígeno
OP neumonía organizada
TAC tomografía axial computada
ARM asistencia respiratoria mecánica
FBC fibrobroncoscopia
BAL lavado broncoalveolar
BTB biopsia transbronquial
DAD daño alveolar difuso
NIC neumonía intersticial celular
mg/kg miligramos por kilogramo de peso corporal
Introducción
Desde el principio de la pandemia de COVID-19, mucho se ha
discutido sobre la utilidad de los corticoÂesteroides
como terapéutica farmacológica. Desde un inicio donde se
asumió incluso un potencial efecto perjudicial1,
posteriormente se demostró su utilidad en aquellos pacientes con
neumonía aguda severa requiriente de
oxigenoterapia o algún tipo de soporte ventilatorio2.
Pacientes que superan esta fase aguda de la enfermedad pueden presentar alteraciones
clinico-radiologicas3-5 en el periodo post-agudo, no
conociéndose aún con certeza su evolución a largo plazo.
Es pertinente contar con tratamientos probados para acelerar su
recuperación y reducir las potenciales secuelas6.
Los corticosteroides conÂtrarrestarían el
proceso inflamatorio desencadenado por la infección viral y perpetuado
por un sistema inmunológico “desregulado”7.
Este reporte de casos intentó dar una respuesta al menos inicial a esta
hipótesis, describiendo la evolución clínica y radiológica
de los pacientes que recibieron dicho tratamiento
Materiales
y métodos
Se tomaron en consideración para este reporte 18 pacientes
con neumonía grave8 por COVID-19 que, transcurridos
los primeros 14 días desde el inicio sintomático, persistieron
con significativas alteraciones clínicas (disnea CF III-IV según
escala NYHA, no explicada por otra causa), oximétricas
(desaturación de oxígeno (O2) respirando aire
ambiente, no presente previo al COVID-19) y/o tomográficas
(infiltraÂdos parenquimatosos bilaterales sugestivos de neumonía
organizada (OP) o aparición tardía de nuevos infiltrados no
explicados por infección de otra etiología). Los pacientes fueron
internados y tratados en 3 instituciones médicas privadas polivalentes
de la Ciudad Autónoma de Buenos Aires.
Todos los casos recibieron durante el periodo agudo el tratamiento
con dexametasona acorde a lo descripto en el estudio
Recovery2,
indicándose en algunos de ellos otras medidas terapéuticas
según lo que estuviese avalado al momento de dicha internación
(plasma de convaleciente, suero equino hipeÂrinmune, hidroxicloroquina, fármacos antirretrovirales)
Se realizaron Tomografías (TAC) de tórax al ingreso
a internación, ante cambios clínicos que exÂpresasen deterioro de
su situación respiratoria, al momento de iniciar la corticoterapia
y 4 semanas posteriores al inicio de esta. Se utilizaron corticoesteroides
endovenosos en pulsos (metilprednisolona 500 mg por
día, 3 dosis) en pacientes con asistencia respiratoria mecánica
(ARM) o con respiración espontanea con elevado requerimiento de O2
mediante cánula de alto flujo o mascara reservorio. En
pacientes con requerimiento de O2 por cánula nasal
convencional menor a 5 litros/minuto se indicaÂron corticoesteroides
orales (meprednisona 0,5 a 0,75 mg/kg/día).
Este mismo esquema continuó al endovenoso en los pacientes que
requirieron las dosis en pulsos. El tratamiento se extendió por 3 a 6
meses a semejanza de otras neumonías organizadas9,
con descenso progresivo según la respuesta clíÂnica, oximétrico y radiológica. En aquellos
pacientes donde existió sospecha de infecciones agregadas, y donde
clínicamente fue posible y seguro, se realizó broncoscopia
(FBC) con lavado broncoalveolar (BAL) y biopsias transbronquiales (BTB) tanto para descartar la misma como
para intentar filiar las características anatomo-patológicas
del proceso inflamatorio evidenciado en las imágenes.
Consideración
ética
Este manuscrito es una serie de casos clínicos y sobre los
cuales se adoptaron conductas meramente descriptivas e interpretativas de sus
resultados, intentando alcanzar conclusiones validas en relación con los
mismos. No se produjo en el contexto de un ensayo de investigación con
grupo control ni trataÂmientos aleatorizados. Se firmó el consentimiento
informado al ingreso del paciente a la hospitalización y el
correspondiente a la broncoscopia cuando fuera
realizada. Se respetaron los lineamientos de la Ley de Protección de
Datos Personales N° 25.236, particularmente en sus artículos 1°, 5°
inciso D, 8° y 11° inciso D.
Resultados
De los 18 pacientes incluidos, 15 eran de sexo masculino y 3
femenino, con una media de edad de 58,4 ± 13.6 años. Cinco pacientes no
tenían antecedentes patológicos conocidos. Los otros 13 contaban
con antecedentes médicos clínicos y oncológicos (Tabla
1). Todos los pacientes recibieron el tratamiento con dexametasona
6 mg/día EV o VO por 10 días acorde al estudio Recovery. El tiempo promedio desde el inicio de
síntomas hasta el inicio del tratamiento corticoideo
“no dexametasona” fue de 28,1 ± 10 días. Dada
la criticidad del cuadro clínico 7 pacientes recibieron inicialmente el
tratamiento endovenoso con metilprednisolona (5
pacientes con cánula nasal de alto flujo o mascara reservorio y 2 con
ARM). En aquellos que utilizaron corticoterapia oral
se administró meprednisona 50 ± 12
mg/día.
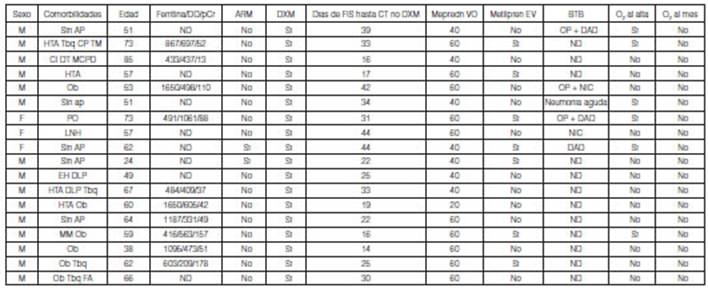
M: masculino. F: femenino. Sin AP: sin
antecedentes patológicos. HTA: hipertensión arterial. Tbq: Tabaquismo. CP: cáncer de próstata. TM.
tumor de maxilar inferior. CI: cardiopatía isquémica. DBT:
diabetes. MCPD: marcapasos definitivo. Ob: obesidad.
PO: penfigoide ocular. LNH: linfoma no Hodgkin. EH: estetatosis
hepática. DLP: dislipemia. MM: mieloma
múltiple. FA: fibrilación auricular. Ferritina ng/ml. DD: dímero D ng/ml.
pCR: proÂteína C reactiva mg/L. FIS: fecha de
inicio de síntomas. CT no DXM: corticoterapia
no desametasona. Mepredn
VO: meprednisona oral dosis inicial. Metilpren EV: pulsos de metilprednisolona
endovenosa: BTB: biopsia transbronquial. OP:
neumonía organizada. DAD: daño alveolar difuso. NIC:
neumonía intersticial celular. ND: no disponible/no realizado. O2:
oxígeno.
En 6 pacientes se realizó FBC con BAL y BTB. En ninguno de
ellos se aislaron gérmenes. En 3 de ellos el informe anatomopatológico
demostró patrón de OP asociada en 2 de ellos a daño
alveolar difuso (DAD) y 1 asociado a inflamación linfocitaria o
neumonía intersticial celular (NIC). En 1 paciente se observaron cambios
de DAD aislado, en otra afectación inflamatoria neutrofílica
de aspecto agudo y en el restante se informó NIC
Seis de los 18 pacientes requirieron al alta hospitalaria
provisión de O2 domiciliaria por disnea o desaturación. Al mes del alta ninguno de ellos
mantuvo la indicación de O2.
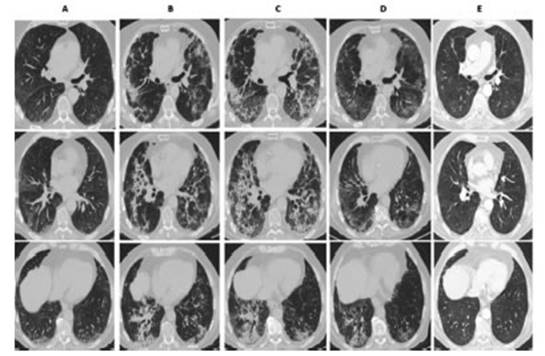
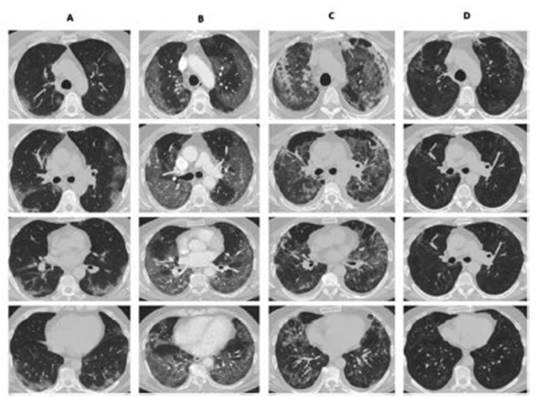
En la totalidad de los pacientes, la TAC de tórax realizada
4 semanas posteriores al alta evidencio clara disminución del compromiso
parenquimatoso, siendo el hallazgo más frecuente la persistencia de
afectación en vidrio esmerilado asociado a engrosamientos septales (Figuras 1 y 2). Solo en 1 paciente se
observaron bronquiectasias por tracción y en otro una imagen compatible
con un neumatocele.
Discusión
Al conocerse la infección por SARS-CoV-2, se asumió
que el inicio clínico era expresión de la infección viral
y el periodo post agudo era consecuencia de una desregulación del
sistema inmunológico, más conocida como “tormenta de citoquinas”7. La corticoterapia
en fase aguda infecciosa demostró su utilidad en el estudio Recovery2
donde se describió una mejoría en la supervivencia
con el uso de dexametasona en aquellos pacientes con
requerimiento de algún tipo de asistencia respiratoria. Otros autores
reportaron similares beneficios utilizando dosis mayores de metilprednisolona10-12. Superado el proceso
infeccioso agudo, y a semejanza de otros agentes etiológicos más
conocidos13,
la COVID-19 puede evolucionar hacia un cuadro clínico compatible con
neumonía organizada secundaria14,
15. Ello queda demostrado en las características tomográficas observadas durante la evolución
de la infección16.
En los informes anatomo-patológicos de
necropsias y en escasos reportes de biopsias “in vivo” se confirmó dicho
patrón de afectación, asociado a otros también observados
como el daño alveolar difuso y la neumonía organiÂzada fibrinoide
aguda (AFOP)14, 17.
Se desconoce a la fecha la natural evolución de las
consecuencias clínicas y radiológicas post infección aguda
por COVID-19. Pero el volumen de pacientes que esta pandemia aqueja hace
imperativo enconÂtrar algún tratamiento que acelere la
recuperación y reduzca al mínimo las anomalías
respiratorias potencialmente secuelares. Según
diversos reportes3, 4, 18,
39% de los pacientes continuaron sintomáticos al mes del alta
hospitalaria, hasta 63% de los pacientes presentaron alteraciones espirométricas a 3 meses de la infección y
30% al año, y 25% de los pacientes mantuvieron alteraciones
radiológicas al año de la infección.
Myall y
colaboradores18 describieron en su trabajo una
conducta similar a la descripta en este reporte, solo que iniciaron el
tratamiento corticoideo 6 semanas luego del alta en
pacientes con hallazgos clínicos o radiológicos sugestivos de
lesión pulmonar persistente, principalmente OP. En su caso indicaron
solo 3 semanas de tratamiento con corticoides orales y sus resultados mostraron
una mejoría sintomática, radiológica y espirométrica.
La guía francesa19 para el manejo de las secuelas
respiratorias post COVID también apoyó esta conducta,
considerando pasibles de tratamiento aquellos pacientes que persistieron
sintomáticos o con alteraciones radiológicas o espirométricas hasta 1 año luego de la
infección. En esta normativa, el tratamiento se asemeja más al
tratamiento convencional de una neumonía organizada, iniciando con prednisona 0,5 mg/kg por un mes y luego reduciendo 10 mg
cada mes.
Es parte de estudios futuros definir si la corticoterapia
debe ser iniciada en el periodo post-agudo inmediato o en forma diferida ante
la falta de mejoría clínica o radiológica. Deberá
también evaluarse si existe un grupo de pacientes donde el tratamiento corticoideo indicado en el periodo agudo deba ser
continuado por un periodo mayor a los 10 días “protocolares” al
reconocer marcadores radiológicos o clínicos que sugieran la
posterior “mala” evolución acá descripta. Por último,
sería adecuado definir qué dosis y que duración
debería tener el tratamiento corticoesteroideo
teniendo en cuenta que el desencadenante del proceso inflamatorio ya fue resuelto
(infección viral aguda) `y los efectos adversos relacionados con su uso
prolongado.
Este trabajo retrospectivo sobre una serie de casos tiene claras
limitaciones: la falta de un grupo control y también la falta de
aleatorización en el tratamiento indicado. La decisión sobre cual
utilizar fue definido por el propio médico tratante analizando
clínicamente cada caso en forma individual. Aun así, los
resultados favorables descriptos en los pacientes permite sugerir que el tratamiento
con cortiÂcoesteroides sistémicos indicados
luego del periodo agudo, tendría un efecto beneficioso tanto
clínico como radiográfico en pacientes con evolución
tórpida de la neumonía grave por COVID-19 siempre que se haya
debidamente descartado la presencia de tromboembolia pulmonar o
sobreinfección bacteriana o micótica u
otras causas de disnea y/o infiltrados pulmonares (insuficiencia cardiaca,
toxicidad pulmonar farmacológica, agudización de
patologías pulmonares de base) que puedan justificar el cuadro
clínico más allá de la propia evolución no
favorable de su COVID-19. Es menester de estudios prospectivos debidamente
diseñados establecer con certeza el beneficio aquí esbozado,
definiendo claros criterios de inclusión, formas de tratamiento, dosis y
tiempo del mismo.
Conclusiones
La corticoterapia sistémica
utilizada luego del periodo agudo tendría un potencial efecto
beneficioso en pacientes con neumonía grave por SARS COV 2 que mantienen
luego de los 14 días del inicio sintomático, manifestaciones
clínicas o radiológicas que sugieran daño generado por la
respuesta inmune al virus.
Conflictos de interés: El autor declara no tener
ningún conflicto de interés.
Agradecimiento:
A los servicios de Clínica Médica de IADT y
Sanatorio Finochietto por su partiÂcipación y
apoyo permanente en el seguimiento médico de los pacientes.
A la Dra. Teresa Castiglioni,
patóloga del Laboratorio Dr. Elsner, por su
colaboración permanente con mi tarea médica. Y por último
mi recuerdo a todos los médicos y pacientes que juntos afrontamos esta
pandemia.
Bibliografía
1. Centers for Disease
Control and Prevention. Interim
Clinical Guidance for Management of Patients with Confirmed 2019 Novel
Coronavirus (2019-nCoV) Infection. Updated March 7, 2020.
2. Horby P, WS Lim
WS, Emberson J, et al. Dexamethasone
in Hospitalized Patients with Covid-19. The RECOVERY CollaboraÂtive Group. N Engl J Med 2021; 384: 693-704.
3. Xiaojun W, Xiaofan
L, Yilu Z, et al. 3 month,
6 month, 9 month and 12 month respiratory outcomes in patients following COVID-19 related hospitalization: a prospective study. Lancet Respir
Med 2021. May 5:S2213-2600(21)00174-0
4. Lerum TV, Aalokken
TM, Bronstad E, et al. Dyspnoea,
lung function and CT findings 3 months after hospital admission for COVID-19. Eur Respir J 2021; 57(4): 2003448.
5. Sibila O, Albacar N, Perea L, et al. Lung function sequelae
in COVID-19 patients 3 months
after hospital discharge. Arch Bronconeumol 2021; 57(S2):
45-63.
6. Gentile F, Aimo
A, Forfori, F et al. COVID-19 and risk
of pulmonary fibrosis: the importance of planning ahead. Eur J Prev
Cardiol 2020; 27(13): 1442-6.
7. Deblina Datta
S, Talwar A, Lee JT. A Proposed
framework and timeline of the Spectrum of disease due to SARS COV 2 infection. Illness Beyond Acute infection
and Public health implications. JAMA 2020; 324(22): 2251-2.
8. World Health
Organization (2020) Clinical
Management of COVID-19: interim guidance;
27 May 2020. WHO
9. King T. Cryptogenic organizing pneumonia. Retrieved May 13, 2021, from www.uptodate.com/contents/COP
10. Salton F, Confalonieri
P, Meduri U, et al. Prolonged
low doce methylprednisone
in patients with severe COVID-19 pneumonia. Open Forum Infect Dis.
2020; 7910:ofaa421.
https://doi.org/10.1093/ofid/oaa421. eCollection 2020
Oct.
11. Edalatifard M, Akhtari
M, Salehi, M et al. Intravenous
methylprednisolone pulse as a treatment
for hospitalized seÂvere COVID-19 patients: results from a randomized controlled clinical trial. Eur Respir J 2020;56:2002808
https://doi. org/10.1183/13993003.02808-202
12. Papamanoli A, Yoo
J, Grewal P, et al. High dose
methylprednisolone in nonintubated
patients with severe COVID-19 pneuÂmonia. Eur Respir J 2020; 56(6):
2002808.
13. Cordier JF. Cryptogenic
organising pneumonia. Eur Respir J 2006; 28: 422-46.
14. Edupunganti S, Kumar
A, Konopka K. Organizing pneumonia as a manifestation of
coronavirus disease 2019. Pathol
Int 2021; 7193: 210-2.
15. Kory P, Kanne
JP. SARS CoV2 organising pneumonia:
Has there been
a widespread failure to identify and treat this prevalent condition in COVID-19? BMJ Open Resp
Res 2020; 7(1): e000724
16. Parra Gordo ML, Buitrago Weiland G,
Grau Garcia M, et al. Aspectos radiológicos de
la neumonía COVID-19: evolución y complicaciones
torácicas. Radiología 20212; 63: 74-88.
17. Copin MC, Parmentier
E, Duburcq T et al. Time to consider
histologic pattern of lung injury to treat critically ill patients with
COVID-19 infection. Intensive
Care Med 2020; 46: 1124-6.
18. Myall KJ, Mukherjee
B, Castanheira AM, et al. Persistent
Post COVID-19 Inflammatory Interstitial
Lung Disease: An obÂservational Study of corticosteroid treatment. Ann Am Thorac Soc 2021; 18(5): 799-806.
19. Andrejak C, Cottin
V, Crestani B et al. Guide
de prise en charge des sequelles respiratoires post infection a SARS COV 2. Proposition
de prise en charge elaborees par la Societe de Pneumologie de Langue Francaise. Versio du 10 novembre 2020. Revue des Maladies Respiratoires 2021; 38: 114-21.