Autor : Juan Manuel Ossés
Coordinador de trasplante Pulmonar - División Trasplante Intratoråcico Hospital Universitario Fundación Favaloro - Av. Belgrano 1782, 1° piso (C1093AAS)
Correspondencia : E-mail: jmosses@ffavaloro.org
¿Cuál es la magnitud del problema clínico?
En el pasado, la trombosis venosa profunda de miembros superiores (TVPMS) fue considerada una entidad rara y benigna. La TVPMS se ha convertido en más frecuente desde 1970 debido al incremento en el uso de catéteres venosos centrales (CVC) y de dispositivos transvenosos, como marcapasos y cardiodesfibriladores. La TVPMS representa el 4% de todos los casos de trombosis venosa profunda (TVP) y el 18% de las TVP en pacientes hospitalizados1.
Datos publicados en las últimas décadas sugieren que la TVPMS se asocia a una significativa prevalencia de embolia de pulmón2, la cual varía ampliamente en al literatura de un 2 a un 35% vs 29% de TVP en miembros inferiores (TVPMI)1.
A 3 meses, la mortalidad por todas las causas en pacientes con TVPMS es 7% comparada con 11% en aquellos con TVPMI4.
Por otra parte, la morbilidad de la TVPMS no es menor e incluye pérdida de los accesos vasculares, síndrome de vena cava superior, tromboflebitis séptica y síndrome post trombótico3, 4, 7.
Las venas más frecuentemente involucradas son la subclavia y la axilar, menos frecuentemente son afectadas las venas braquiales, yugular interna y venas centrales (tronco braquiocefálico y vena cava superior).
De acuerdo a la etiología, la TVPMS ha sido clasificada en primaria y secundaria. La TVPMS primaria se observa en el 20% de los casos e incluye las formas idiopáticas, la relacionada a esfuerzos (Síndrome de Paget-Schroetter) y síndrome del desfiladero torácico. Las causas secundarias se observan en el 80% de los casos, e incluye el cáncer, los CVC, dispositivos transvenosos y trombofilias4.
Factores de riesgo
Los factores de riesgo más comunes para el desarrollo de TVPMS son el cáncer, los CVC y la trombofilia5. El cáncer es un factor de riesgo más significativo para TVPMS que para TVPMI. Sin embargo, en pacientes con cáncer, la formación espontánea de TVPMS es infrecuente en ausencia de CVC, terapia radiante o compresión venosa por el tumor.
La presencia de CVC es el predictor independiente más importante para TVPMS6. Aproximadamente un 55% de las TVPMS ocurren en pacientes quienes tienen CVC o han tenido en un plazo de 30 días previos al diagnóstico de la trombosis. El tipo de catéter influye en la frecuencia de TVPMS. Los catéteres centrales tienen un riesgo a 3 meses de TVPMS de 3%, comparado con 9.3% de catéteres insertados periféricamente. Por otra parte, la duración del catéter, el tipo de solución administrada, número de lúmenes y la infección relacionada al catéter influyen en el riesgo de TVPMS. Pacientes con cáncer y CVC tiene mayor riesgo que aquellos con CVC y sin cáncer8.
La incidencia de TVPMS asociada al uso de dispositivos transvenosos, tales como marcapasos o cardiodesfibriladores, es de 13.9%. El riesgo se incrementa en individuos con pobre función cardiaca (fracción de eyección ventricular izquierda menor a 40%) y con insuficiencia cardiaca congestiva.
Los estados trombofílicos son otro factor de riesgo mayor para el desarrollo de RVPMS. El riesgo se incrementa cinco a seis veces en pacientes con deficiencia de proteína C, proteína S o anti-trombina III o heterozigotas para factor V Leiden y protrombina G20210A. La prevalencia de defectos heredados de la coagulación en pacientes con TVPMS no relacionada a CVC oscila según reportes entre 10 a 62%.
¿Por qué la TVPMS es menos frecuente que la TVPMI?
El sistema venoso de miembros superiores tiene menos propensión a la TVP por varias razones, en primer lugar al alto flujo sanguíneo a través del mismo, y a la presencia de pocas válvulas que sirven como asiento en la formación de trombos. Además, los miembros superiores tienen mayor movilidad que los inferiores, inclusive en pacientes postrados, con menor posibilidad de estasis.
Finalmente, las venas de las extremidades superiores presentan mayor actividad fibrinolítica y niveles más elevados del activador del plasminógeno4.
Manifestaciones clínicas
Hasta un 66% de los pacientes con TVPMS suelen estar asintomáticos, especialmente los que se asocian a CVC. La manifestación clínica más prevalente es el edema, el cual suele acompañarse de dolor en el 40% de los casos y en tan solo un 6% suele observarse eritema en la región afectada1.
Los síntomas en la TVPMS asociada a CVC son menos frecuentes debido a que los coágulos suelen ser menos oclusivos y de desarrollo más lento. Las manifestaciones de la TVPMS asociada a CVC pueden ser sutiles, incluyendo la dificultad en extraer sangre a través del catéter, incremento en la presión de diálisis y edema transitorio del miembro afectado luego de la diálisis8, 9.
Otros síntomas y signos observados con menor frecuencia son el edema de cuello (compromiso de venas intratorácicas), dolor torácico, tos, dolor mandibular, cefaleas, parestesias en miembros superiores y circulación colateral. Complicaciones más graves son el síndrome de vena cava superior (SVC), gangrena venosa, síncope y embolia de pulmón.
Evaluación diagnóstica
Tanto la sensibilidad como la especificidad del diagnóstico clínico es baja, los estudios objetivos suelen confirmar la TVP en solamente un 50% de los casos con síntomas y signos de TVPMS2.
La venografía es el test contra el cual otros estudios por imágenes son evaluados2,11. El hallazgo más característico es la falta de relleno de la vena involucrada. Sin embargo, la técnica no está exenta de riesgos, en este sentido la misma al utilizar contraste iodado puede ser potencialmente nefrotóxica o desencadenar reacciones alérgicas. Entre un 6 y 13 % de pacientes con sospecha clínica de TVPMS la venografía no puede ser utilizada por insuficiencia renal, embarazo, antecedentes alérgicos o inaccesibilidad de las venas del miembro involucrado. Por estas razones, la venografía solamente debe ser utilizada cuando otras modalidades no han podido establecer o excluir el diagnóstico de TVPMS.
La ecografía es frecuentemente utilizada en el diagnóstico de TVPMS. La misma tiene la ventaja de ser no invasiva, estar disponible en la mayoría de las instituciones, pudiendo ser realizada al lado de la cama del paciente. Múltiples modalidades, tales como la compresión y el doppler color (Figura 1) suelen ser utilizadas6, 12. La sensibilidad de la ecografía para TVPMS oscila entre 82 y 97% y la especificidad entre 82 y 96%.
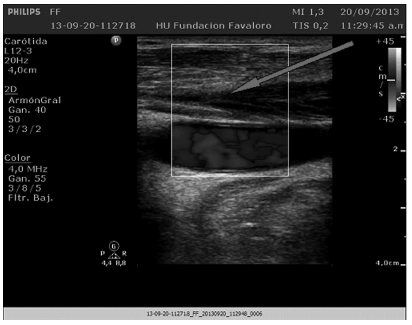
La ecografía no es adecuada frente a la sospecha clínica de trombosis de venas centrales (vena cava, tronco braquiocefálico).
La venografía con tomografía computada (Figura 2) tiene la ventaja de poder evaluar directamente las venas centrales, como así también diagnosticar otras causas de obstrucción venosa, tales como la compresión externa por tumores o adenopatías13.
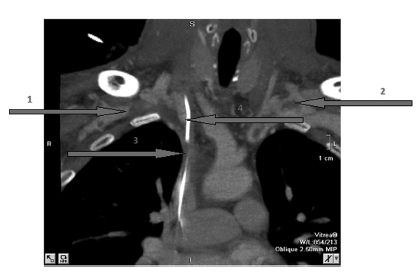
Diversos estudios han puesto en evidencia una buena correlación entre la resonancia magnética nuclear (RMN) y la venografía con contraste. La RMN tiene una sensibilidad del 90% y una especificidad del 100%14. La RMN puede ser realizada sin contraste, haciéndola disponible para pacientes con insuficiencia renal o antecedentes severos de alergia. Al igual que la tomografía, puede evaluar las estructuras adyacentes y por lo tanto descartar otras causas de alteración en el retorno venoso. Por último la RMN puede distinguir entre trombos agudos y crónicos6.
¿Cuáles son las principales complicaciones de la TVPMS?
Aproximadamente un 9% de pacientes con TVPMS desarrollan embolia de pulmón (EP)10. La hipertensión pulmonar crónica tromboembólica (HPCT) cuya prevalencia oscila entre un 2-4% luego de un evento embólico agudo ha sido descripta después de la TVPMS.
El síndrome post trombótico, causado por hipertensión venosa secundaria a la obstrucción
del flujo de sangre y a la injuria valvular, varía desde edema leve hasta formas severas caracterizadas por dolor, ulceración, impotencia funcional del miembro afectado y predisposición a las infecciones bacterianas15. La prevalencia del síndrome post trombótico ha sido difícil de precisar debido a diferentes criterios utilizados en la definición del mismo y por el incremento en la presentación a través del tiempo. La prevalencia reportada del síndrome post trombótico después de una adecuada anticoagulación es de 21% a 6 meses, 25% al año y 27% a los 2 años. Los factores de riesgo para el desarrollo de síndrome post trombótico son la obstrucción de múltiples vasos, retardo en el inicio del tratamiento, falta de resolución del coágulo y la elevación persistente de los niveles del dímero d y factor VII a pesar del tratamiento.
La asociación entre infección del CVC y la formación de coágulos ha sido bien establecida, aunque la precisa relación causal entre estos dos eventos no es clara. El riesgo relativo se trombosis en presencia de infección del CVC se incrementa 17 veces, comparados con aquellos sin infección.
Otras complicaciones reportadas son el SVC, la tromboflebitis séptica, la plexopatía braquial y la pérdida de accesos vasculares.
La mortalidad a tres meses por todas las causas en pacientes con TVPMS es de 7%, sin embargo la prevalencia de EP fatal a 3 meses es solamente de 0.2%16. La mortalidad por EP está relacionada a una inadecuada anticoagulación y a la presencia de severas comorbilidades. Finalmente, la localización del coágulo (subclavia-axilar o yugular interna) no influye en la mortalidad.
Tratamiento y profilaxis
El tratamiento preferido para la TVPMS es la anticoagulación. Las recomendaciones son similares a las de TVPMI. El tratamiento inicial puede ser con heparinas de bajo peso molecular (HBPM), heparina no fraccionada o fondaparinux17. La anticoagulación debe ser mantenida con antagonistas de vitamina K, o HBPM por al menos tres meses, pudiendo ser utilizados además inhibidores sintéticos de trombina o factor Xa. Se aconseja la utilización de HBPM en pacientes con cáncer, debido al menor riesgo de retrombosis o sangrado observado, en relación a los antagonistas de vitamina K.
Si la TVP está asociada a CVC, es aconsejable una anticoagulación efectiva durante un período de 3 a 5 días previo a la remoción del catéter. La decisión de remover o mantener el catéter no afecta la duración de la anticoagulación.
La duración del tratamiento puede estar condicionado por la carga trombótica, persistencia del factor de riesgo para TVP y presencia de comorbilidades.
Comparada con la anticoagulación, la trombolisis ha demostrado en diversos estudios una mejor repermeabilización de la vena afectada, aunque no fueron encontradas diferencias en la incidencia de retrombosis o desarrollo de síndrome post trombótico18. Sin embargo, la trombolisis presentó una significativa mayor incidencia de sangrado. En la actualidad la trombolisis sistémica o dirigida por catéter está indicada en pacientes muy sintomáticos y con bajo riesgo de sangrado.
Los filtros en vena cava superior han sido utilizados con éxito en pacientes con contraindicaciones o complicaciones para la anticoagulación, y casos de progresión de la trombosis a pesar de un correcto tratamiento anticoagulante19.
Las intervenciones endovasculares (angioplastia o stent) son opciones terapéuticas válidas para pacientes en los cuales la anticoagulación o trombolisis fallaron en la recanalización de la vena, continuando los mismos muy sintomáticos.
La descompresión quirúrgica es utilizada en el manejo de la trombosis venosa relacionada a esfuerzos (Síndrome de Pager-Schroetter), una rara condición típicamente observada en hombres jóvenes, con sobre desarrollo del escaleno anterior. Durante un esfuerzo intenso el escaleno anterior puede comprimir a la vena subclavia contra la primera costilla, generando estasis e injuria endotelial y favoreciendo el desarrollo de TVP. El procedimiento quirúrgico suele requerir de la resección de la primera costilla, el tendón del subclavio y la inserción del escaleno anterior.
Numerosos estudios han demostrado que el uso de CVC predispone al desarrollo de TVPMS. Esto ha generado un notable interés sobre el uso de profilaxis anticoagulante en este grupo de pacientes. No existen en la actualidad recomendaciones formales para el uso de profilaxis en pacientes con CVC. Sin embargo, han sido identificados algunos factores que incrementan notablemente el riesgo de TVPMS asociada al uso de CVC: 1. cáncer y quimioterapia, 2. radioterapia torácica, 3. inserción del catéter en el miembro superior izquierdo, 4- presencia de metástasis y 5. colocación de catéter en presencia de SVC20. En estas circunstancias la profilaxis anticoagulante podría resultar beneficiosa para estos pacientes.
Conflictos de interés: El autor declara no tener conflictos de interés.
1. Mustafá S, Stein P, Patel K, et al. Upper extremity deep venous thrombosis. Chest 2003; 123: 1953-6.
2. Prandoni P, Polistena P, Bernardi E, et al. Upper extremity deep vein trombosis. Risk factors, diagnosis and complications. Arch Intern Méd 1997; 157: 57-62.
3. Joffe H, Goldhaber S. Upper-extremity deep vein thrombosis. Circulation 2002; 106: 1874-80.
4. Hingorani A, Ascher E, Marks N, et al. Morbidity and mortality associated with brachial vein thrombosis. Ann Vasc Surg 2006; 20: 297-300.
5. Martinelli I, Battaglioli T, Bucciarelli P, et al. Risk factors and recurrence rate of primary deep vein thrombosis of the upper extremities. Circulation 2004; 110: 566-70.
6. Baarslag H, Koopman M, Reekers J, et al. Diagnosis and management of deep vein thrombosis of the upper extremity: a review. Eur Radiol 2004; 14: 1263-74.
7. Arnhjort T, Persson L, Rosfors S, et al. Primary deep thrombosis in the upper limb. A retrospective study with emphasis on pathogenesis and late sequelae. Eur J Intern Med 2007; 18: 304-8.
8. Verso M, Agnelli G, Kamphuisen P, et al. Risk factors for upper limb deep vein thrombosis associated with the use central vein catheter in cancer patients. Intern Emerg Med 2008; 3: 117-22.
9. Kucher N. Deep-vein trombosis of the upper extremities. N Engl J Med 2011; 364: 861-9.
10. Muñoz FJ, Mismetti P, Poggio R, et al. Clinical outcome of patients with upper extremity deep vein thrombosis: results from the RIETE Registry. Chest 2008; 133: 143-8.
11. Baarslag H, van Beek E, Koopman M, et al. Prospective study of color duplex ultrasonography compared with contrast venography in patients suspected of having deep thrombosis of the upper extremities. Ann Intern Med 2002; 136: 865-72.
12. Katz D, Hon M. Current imaging. Tech Vasc Interv Radiol 2004; 7: 55-62
13. Sabharwal R, Boshell D, Vladica P. Multidetector spiral CT venography in the diagnosis of upper extremity deep venous thrombosis. Australas Radiol 2007; 51 (Suppl): B253-6.
14. Baarslag HJ, Van Beek EJ, Reekers JA. Magnetic resonance venography in consecutive patients with suspected deep vein thrombosis of the upper extremity: initial experience. Acta radiol 2004; 45: 38-43.
15. Elman E, Kahn S. The post-thrombotic syndrome after upper extremity deep venous thrombosis in adults: a systematic review. Thromb Res 2006; 117: 609-14.
16. Monreal M, Muñoz F, Rosa V, et al. Upper extremity DVT in oncological patients: analysis of risk factors. Data from the RIETE registry. Exp Oncol 2006; 28: 245-7.
17. Kearon C, Kahn S, Agnelli G, et al. Antithrombotic therapy for venous thromboembolic disease: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th edition). Chest 2008; 133 (Suppl 6): 454S-545S.
18. Sabeti S, Schillinger M, Mlekusch W, et al. Treatment of subclavian-axillary vein thrombosis: long term outcome of anticoagulation versus systemic thrombolysis. Thromb Res 2002; 108: 279-85.
19. Spence L, Gironta M, Malde H, et al. Acute upper extremity deep venous thrombosis: safety and effectiveness of superior vena cava filters. Radiology 1999; 210: 53-8.
20. Verso M, Agnelli G, Bertoglio S, et al. Enoxaparin for the prevention of veonus thromboembolism associated with central vein catheter: a double-blind, placebo-controlled, randomized study in cancer patients. J Clin Oncol 2005; 23: 4057-62.