Autor Schiavone Miguel1, Blanco MagalĂ2-31, Ernst Glenda2, Salvado Alejandro2, Manuale Osvaldo1, Nosetto Daniela1 y Borsini Eduardo2-3
1Unidad de Hipertensión Arterial, 2 Centro de Medicina Respiratoria, 3 Unidad de Sueño y Ventilación. Hospital Británico de la Ciudad de Buenos Aires. Argentina
Correspondencia : Dr. Miguel Schiavone: mjschiavone@gmail.com; Dr. Eduardo Borsini: borsinieduardo@yahoo.com.ar
Resumen
Introducción: La hipertensión arterial y las apneas obstructivas del sueño constituyen patologías de alta prevalencia frecuentemente relacionadas. Comprender los perfiles hemodinámicos permitiría orientar el tratamiento basado en los cambios producidos por la combinación de ambas patologías.
Materiales y métodos: Se realizó un estudio prospectivo; piloto y exploratorio, con el objetivo de caracterizar los patrones hemodinámicos de los pacientes derivados al Centro de Hipertensión Arterial que se encontraban sin tratamiento farmacológico al momento de la consulta. El patrón hemodinámico y el contenido fluido torácico fueron evaluados mediante cardiografía por impedancia. Además, se registraron los valores de presión arterial tanto de consultorio como de monitoreo ambulatorio de 24 horas y la sospecha de apneas del sueño fue evaluada objetivamente mediante poligrafía respiratoria domiciliaria.
Resultados: Se incluyeron 58 pacientes. El diagnóstico de apneas del sueño fue confirmado en 84.5% de los casos (46.5% moderada a severa) y el de hipertensión arterial en el 65.2%. Los hallazgos de este estudio mostraron una disminución progresiva de la proporción de patrón normodinámico y contenido fluido torácico normal, en relación al incremento de la severidad del trastorno respiratorio del sueño (p 0.5). Más aún, la presión de consultorio, sistólica y diastólica, mostraron un incremento progresivo en relación al incremento en la severidad de la apnea del sueño (p 0.05 y 0.01).
Conclusión: El trastorno respiratorio del sueño moderado- severo se relacionó con incremento de las cifras tensionales en reposo y una tendencia que no alcanzo significación estadística en el hallazgo de patrones hemodinámicos alterados.
Palabras clave: Hipertensión arterial; Apneas del Sueño; Patrones Hemodinámicos.
Introducción
La hipertensión arterial (HTA) afecta al 33.5% de la población adulta1. Se ha demostrado que esta enfermedad se asocia con enfermedades cardiovasculares tales como insuficiencia cardíaca, infarto agudo de miocardio, insuficiencia renal y accidente cerebrovascular después de años de exposición2.
En ocasiones, es posible detectar la causa subyacente que contribuye al aumento de la presión arterial (PA). Una de ellas es el síndrome de apneas e hipopneas obstructivas del sueño (SAHOS). Se ha descripto que el SAHOS afecta aproximadamente al 30% de la población general adulta3, aunque existe una elevada tasa de subdiagnostico4. De esta manera, el SAHOS representa un dilema sanitario emergente por su elevada prevalencia y por la morbi-mortalidad que origina, atribuible a accidentes de tránsito y al desarrollo de complicaciones cardiovasculares2-5.
El mayor grado de evidencia de riesgo cardiovascular y SAHOS lo posee la asociación con HTA. También se han asociado los trastornos respiratorios del sueño con la cardiopatía isquémica, arritmias cardíacas e hipertensión pulmonar. Más aún, la relación causa-efecto se ha fortalecido por la identificación de posibles vías patogénicas, así como por la documentación de los efectos del tratamiento sobre el sistema cardiovascular2-8.
Ha sido previamente demostrado que el SAHOS sería un factor de riesgo independiente para el desarrollo de HTA. Worsnop y cols. observaron una significativa asociación entre la HTA y un índice de apnea hipopnea (IAH) > 5/hora mediante polisomnografía y monitorio ambulatorio de presión arterial de 24 horas (MAPA)5. Más aún; Pedrosa y cols. demostraron que el 64% de los pacientes con diagnóstico de HTA secundaria presentaban trastornos respiratorios del sueño6.
Los pacientes con HTA presentan alteración de factores hemodinámicos tales como vasoconstricción periférica, índice cardíaco o un incremento en el volumen intravascular incluso en ocasiones asociada al aumento en los niveles de aldosterona plasmática6-9. A pesar de esta evidencia, no se conocen con detalle las características hemodinámicas de los pacientes con HTA y SAHOS. Los resultados de los estudios de cardiografía por impedancia (CGI) permiten conocer el patrón hemodinámico de los pacientes10-12. Esta técnica podría resultar de utilidad para comprender los determinantes del aumento de la PA y guiar el tratamiento antihipertensivo inicial o adecuar el enfoque farmacológico.
El objetivo principal de este trabajo es caracterizar los distintos patrones hemodinámicos hallados en los pacientes con diagnóstico de HTA y SAHOS, derivados al Centro de Hipertensión Arterial del Servicio de Cardiología en un hospital universitario de comunidad.
Materiales y Métodos
Diseño: estudio prospectivo, piloto y exploratorio en pacientes con diagnóstico presuntivo de HTA y SAHOS que se encontraban sin tratamiento al momento de la consulta. Los datos del presente estudio representan el análisis preliminar de un estudio mayor aún en curso y ha sido aprobado por el comité de revisión institucional de acuerdo a las normas de Helsinki; Aprobación CRIHB N°: #639.
Población estudiada: entre marzo 2016 y marzo 2017 se incluyeron pacientes entre 18 y 65 años, con diagnóstico presuntivo de HTA derivados para diagnóstico y estratificación.
Los pacientes con sospecha de SAHOS fueron definidos por un puntaje mayor a 10 puntos en la escala de somnolencia diurna subjetiva de Epworth13 (ESS), cuestionario de Berlín de alto riesgo y/o más de 5 puntos en cualquier combinación de la escala de STOP-BANG14-16 y considerados elegibles para el protocolo (cualquiera de las tres opciones).
Se excluyeron del estudio los pacientes con tratamiento del SAHOS con CPAP o dispositivos de avance mandibular, y/o tratamiento de la HTA con fármacos. Asimismo excluimos pacientes con obesidad mórbida (IMC mayor a 40 kg/m2) y patologías tales como: enfermedad pulmonar obstructiva crónica, enfermedad neuromuscular e insuficiencia cardíaca aguda o crónica.
Evaluación clínica inicial: al inicio del estudio se realizó una anamnesis del paciente (antecedentes y factores de riesgo), datos antropométricos (IMC, circunferencia de cuello, perímetro de cintura), toma de presión arterial de consultorio, análisis bioquímicos de sangre, electrocardiograma, ecocardiograma doppler color, MAPA y CGI. Luego de la realización de los cuestionarios de Berlín, STOP-BANG y Epworth, a aquellos con riesgo elevado de SAHOS, se les realizó un registro de poligrafía respiratoria (PR) nocturna.
Evaluación de la presión arterial: la medición de la PA se realizó según guías nacionales17. La misma fue registrada con un tensiómetro automático (OMRON 7220). Previo reposo de 5 minutos se procedió a realizar 3 registros separados por 2 minutos y se consideró el promedio de ellas. Monitoreo ambulatorio de Presión Arterial: Se realizó un MAPA de 24 horas con equipo Spacelabs Ultralite (modelo 90217, SpaceLabs, Redmond, WA). Las tomas de PA fueron programadas cada 15 minutos durante el día (8:00 am a 11:00 pm) y cada 30 minutos durante la noche (11:00 pm a 8:00 am). Se definió PA diurna y nocturna controlada cuando las cifras sistólica y diastólica fueron menor o igual a 135/85 mmHg y 120/80 mmHg respectivamente17. El MAPA y el registro de PR se realizaron en noches sucesivas. La lectura e
interpretación de MAPA estuvo a cargo de cardiólogos especialistas en HTA. Se definieron patrones de predominio en la PA (sistólico/diastólico o sisto-diastólico) y en el horario (diurno/nocturno o ambos).
Medición no invasiva de patrones hemodinámicos: La medición de los patrones hemodinámicos se realizó de forma no invasiva a través de CGI. Basado en la determinación de las variaciones de la impedancia eléctrica del tórax, inducidas por cambios en el flujo aórtico durante el ciclo cardíaco, se establecen las variables hemodinámicas. Las mediciones se tomaron con el torso desnudo, en decúbito dorsal luego de 30 minutos de reposo en horario de la mañana antes de las 09:00 horas. Mediante una ecuación de transferencia (ecuación de Kubicek) se calculó el volumen sistólico. A partir de este parámetro y junto con la frecuencia cardíaca y la PA se determinó el gasto cardíaco, las resistencias periféricas y el contenido fluido (TFC)18.
Poligrafía respiratoria: Se utilizaron polígrafos Apnea Link Plus™ (ResMed. Australia) que cuentan con cinco canales y tres señales básicas, oximetría de pulso, flujo por cánula nasal y esfuerzo torácico, (dispositivos de nivel III de la American Academy of Sleep Medicine)19. La lectura se realizó a distancia (Unidad de Sueño y Ventilación) mediante análisis manual secuencial por neumonólogos con experiencia en medicina del sueño. Solo se aceptaron como válidos aquellos registros con un tiempo total de registro en el análisis manual > 240 minutos (> 4 horas). Se definió apnea como reducción del flujo aéreo de > 80% del basal ≥ 10 segundos (s) y las hipopneas se consideraron como una reducción del flujo aéreo de 50% ≥ 10s asociadas a desaturaciones ≥ 3%20. El índice de apnea/hipopnea (IAH) se calculó como el número de apneas/hipopneas por hora de evaluación válida del tiempo total de registro (TTR). Los pacientes se clasificaron como; normales (IAH < 5/h), leves (IAH ≥ 5 y < de 15), moderados (IAH ≥ 15 y < de 30) y severos (IAH ≥ 30).
Análisis estadístico: Los resultados se presentaron como porcentajes en las variables categóricas o media y desvío estándar en las numéricas. Las variables con distribución normal se expresaron como medias y desvío estándar, y las variables sin distribución normal se muestran como medias y percentilos (25-75%). Para comparar diferencias se utilizaron el test de Fisher, Mann Withney o χ2. Para el análisis estadístico se utilizó Graph Pad Prism-6™ software.
Resultados
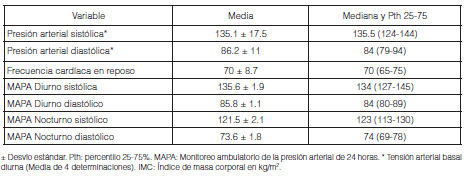
Población: Se incluyeron en el análisis 58 pacientes cuyas características demográficas se observan en la Tabla 1. Los hallazgos según los componentes presentes del cuestionario STOP-BANG se muestran en la Tabla 2 y las mediciones basales de PA de consultorio y de MAPA en la Tabla 3. El diagnóstico de HTA fue confirmando por MAPA en el 65.2% de los pacientes, de los cuales un 13% resultaron HTA nocturna aislada.
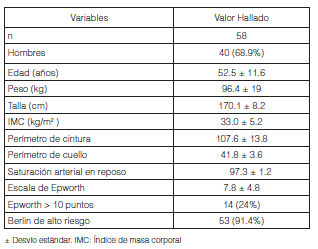
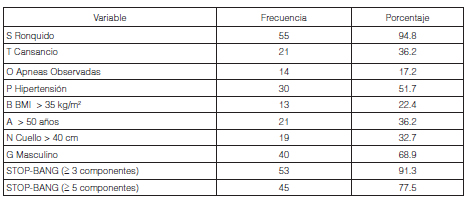
El diagnóstico de SAHOS fue confirmado en el 84.5%, de los cuales el 46.5% correspondieron a formas moderadas a severas categorizadas según el IAH. Los motivos principales para la realización de la PR fueron ronquido (94.0%), edad > 50 años (68.3%), cansancio diurno (34.5%), más de 5 puntos en la escala STOP-BANG (n = 45; 77.5%) y finalmente más de 10 puntos de Epworth (n = 14; 24%).
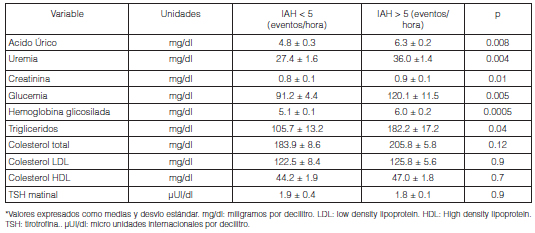
Se encontró un incremento significativo en valores de laboratorio en los pacientes con SAHOS respecto de los pacientes con IAH < 5 eventos/hora en la glucemia (mg/dl): 120.1 ± 11.5 vs 91.2 ± 4.4; p < 0.01 (Tabla 4).
Alteración del patrón hemodinámico en relación con la severidad del SAHOS: Se observó una disminución progresiva que no alcanzó diferencia estadísticamente significativa en la proporción de pacientes con patrón hemodinámico normal (patrón normodinámico) en función del incremento de la severidad del SAHOS (Figura 1A).
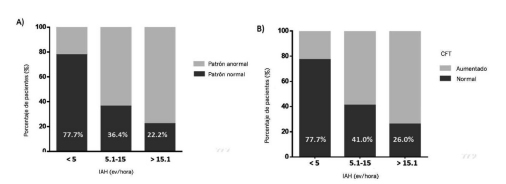
Incremento del Contenido Fluido Torácico en relación con la severidad del SAHOS: Se halló un progresivo incremento del TFC en función del incremento de la severidad del SAHOS (Figura 1B). De igual manera que en el punto anterior, estos no alcanzaron diferencias estadísticamente significativas.
Aumento de la presión arterial de consultorio en relación con la severidad del SAHOS: Tanto en los valores de presión arterial sistólica (PAS) como en la presión arterial diastólica (PAD) se observó un incremento progresivo en relación al incremento en la severidad del trastorno respiratorio del sueño por IAH (normal: 130.4 ± 3.2 mmHg y 85.1 ± 2.8 mmHg; leve: 134.2 ± 3.2 mmHg y 85.4 ± 2.3 mmHg y moderado a severo: 135.5 ± 4.1 mmHg y 87.3 ± 2.3 mmHg; p < 0.05 y p < 0.01 respectivamente) (Figura 2 A y B)
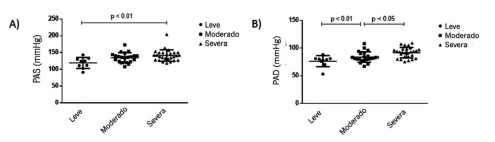
Aumento de la presión arterial por MAPA en relación con la severidad del SAHOS: si bien no hubo diferencia estadísticamente significativa, observamos que el doble de pacientes con HTA nocturna aislada padecían apneas del sueño de grado moderado a severo en comparación a los pacientes HTA diurna aislada (Figura 3).
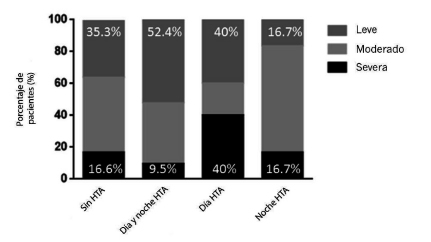
Discusión
La CGI constituye un método rápido y no invasivo para medir el perfil hemodinámico de pacientes hipertensos, permitiendo inferir el mecanismo fisiopatológico prevalente y en forma consecuente elegir la terapéutica antihipertensiva. Sin embargo, existe escasa información sobre el patrón hemodinámico presente en distintos fenotipos de hipertensos y menos aún sobre su relación con SAHOS.
Los hallazgos de este estudio, realizado en pacientes con sospecha de HTA sin tratamiento establecido, mostraron una tendencia que sugiere una relación de incremento proporcional entre la severidad del SAHOS y patrón hemodinámico anormal sin alcanzar significación estadística.
Nuestros resultados son relevantes a causa de que el 46.5% de los pacientes con HTA de reciente diagnóstico que son derivados a un centro especializado presentan SAHOS moderado a severo y son candidatos a tratamiento con CPAP.
Los resultados de la PAS y PAD de consultorio revelaron un incremento proporcional a la severidad del SAHOS; sin embargo los valores promedio de la PA en consultorio resultaron dentro de valores considerados como normotensión. Estos resultados son acordes a la evidencia existente donde demuestra que los pacientes con SAHOS suelen presentar HTA oculta5, 6, 21.
Para confirmar los valores de PA se utilizó el MAPA que demostró que un 65.2% de los pacientes eran hipertensos, de los cuales 13% fueron HTA nocturnos aislados. Sin embargo, un porcentaje mayor de pacientes con HTA diurna en el MAPA presentó SAHOS moderado a severo, colaborando a alertar sobre patrones de presentación circadianos diferentes al nocturno en esta población.
Pratt-Ubunama ha demostrado la asociación entre SAHOS e hiperaldosteronismo, produciendo una mayor cantidad de líquido intravascular debido a la reabsorción de sodio y excreción de potasio relacionada a la aldosterona9. Por su parte, en relación con estos resultados se ha descripto una respuesta favorable de los pacientes con SAHOS a los antialdosterónicos22.
Patrones hemodinámicos en hipertensos con apneas del sueño
De acuerdo a los datos disponibles, estudios en pacientes hipertensos mal controlados muestran un desplazamiento caudal-rostral de fluidos como vía patogénica con un rol significativo en la fisiopatología del SAHOS23. La interacción entre el desplazamiento de líquidos en los pacientes con HTA y SAHOS aún no se comprenden completamente23, 24 y nuestros datos basados en CGI muestran que el TFC se relaciona al IAH contribuyendo a comprender que se incrementa en forma proporcional en relación a la gravedad del SAHOS. Comprender los perfiles hemodinámicos permitiría orientar el tratamiento de la HTA basado en los cambios hemodinámicos producidos por la combinación de la HTA y SAHOS25.
Nuestro estudio adolece de múltiples limitaciones. La subestimación del IAH cuando se utiliza la PR puede ocurrir en el orden de entre el 10 al 15 % en comparación con la PSG convencional26, 27. Esto representa una limitación de la PR que es inherente a la ausencia de señales neurofisiológicas. Los índices utilizados (IAH) difieren con los de la PSG (IAH o RDI) ya que el IAH resulta del cociente entre los eventos de flujo y el tiempo total de registro.
Este pequeño estudio fue conducido en una muestra de pacientes adultos ambulatorios derivados a un servicio de cardiología para evaluación especializada debido a diagnóstico sospechado de HTA. Por ello, la prevalencia de SAHOS es superior a la de la población general, aunque coincidentes a lo reportado previamente en nuestro medio usando PR en un centro especializado28. Además, los pacientes fueron seleccionados por cifras elevadas de PA de consultorio y riesgo aumentado de padecer apneas del sueño; hecho que puede explicar la elevada prevalencia de ambas entidades y sesgar los resultados cuando los grupos son comparados. Finalmente, la escasa potencia estadística derivada de una muestra pequeña requiere confirmación mediante estudios de mayor número de pacientes.
Conclusiones
El trastorno respiratorio del sueño moderado-severo se relacionó con incremento de las cifras tensionales en reposo y una tendencia que no alcanzo significación estadística en el hallazgo de patrones hemodinámicos alterados.
Sin embargo, nuevos estudios aumentando el tamaño de la muestra son necesarios para confirmar nuestros hallazgos.
Conflictos de intereses: Los autores declaran no tener conflictos de intereses en el tema relacionado con este manuscrito.
1. Marín M, Fábregues G, Rodriguez P, y cols. Registro Nacional de Hipertensión Arterial. Conocimiento, tratamiento y control de la hipertensión arterial. Estudio RENATA. Rev Argent Cardiol. 2012; 80: 121-9.
2. Omura M, Yamaguchi K, Kakuta , Nishikawa T. Prospective study on the prevalence of secondary hipertensión among hypertensive patients visiting a general outpatient clinic in Japan.Hypertens Res. 2004; 27: 193-202.
3. Tufik S, Santos-Silva R, Taddei JA, Bittencourt LR. Obstructive sleep apnea syndrome in the Sao Paulo Epidemiologic Sleep Study. Sleep Med. 2010. 11(5): 441-6.
4. Peppard PE, Young T, Palta M, Skatrud J. Prospective study of the association between sleep-disordered breathing and hypertension. N Engl J Med. 2000; 342: 1378-84.
5. Williams AJ, Houston D, Finberg S, et al. Sleep apnea syndrome and essencial hypertension. Am J Cardiol. 1985; 103: 1019- 22.
6. Pedrosa RP, Drager LF, Gonzaga CC, Sousa MG, de Paula LK, Amaro AC, et al. Obstructive sleep apnea: the most common secondary cause of hypertension associated with resistant hypertension. Hypertension. 2011; 58(5): 811-7.
7. Ke X, Guo W, Peng H, et al. Association of aldosterone excess and apnea-hypopnea index in patients with resistant hypertension. Sci Rep. 2017; 22; 7: 45241.
8. De Souza F, Muxfeldt ES, Margallo V, Cortez AF, Cavalcanti AH, Salles GF. Effects of continuous positive airway pressure treatment on aldosterone excretion in patients with obstructive sleep apnoea and resistant hypertension: a randomized controlled trial. J Hypertens. 2017; 35(4): 837-44.
9. Pratt-Ubunama MN, Nishizaka MK, Boedefeld RL, Cofield SS, Harding SM, Calhoun DA. Plasma aldosterone is related to severity of obstructive sleep apnea in subjects with resistant hypertension. Chest. 2007; 131: 453-9.
10. Smith R, Levy P. Ferrario, C, for the Consideration of Noninvasive Hemodynamic Monitoring to Target Reduction of Blood Pressure Levels Study Group: Value of Noninvasive Hemodynamics to Achieve Blood Pressure Control in Hypertensive Subjects. Hypertension. 2006; 47: 771-7.
11. Treister N, Wagner K, Jansen PR. Reproducibility of impedance cardiography parameters in outpatients with clinically stable coronary artery disease. Am J Hypertens. 2005; 18(2): 44S-50S.
12. Taler SJ, Textor SC, Augustine JE. Resistant hypertension: comparing hemodynamic management to specialist care. Hypertension. 2002; 39(5): 982-8.
13. Chiner E, Arriero JM, Signes-Costa J, Marco J, Fuentes I. Validation of the Spanish version of the Epworth Sleepiness Scale in patients with a sleep apnea síndrome. Arch Bronconeumol. 1999; 35: 422-7.
14. Borsini E, Ernst G, Salvado A, et al. Utility of the STOP-BANG components to identify sleep apnea using home respiratory polygraphy. Sleep Breath. 2015; 19(4): 1327-33.
15. Chung F, Yegneswaran B, Liao P, et al. Validation of the Berlin questionnaire and American Society of Anesthesiologists checklist as screening tools for obstructive sleep apnea in surgical patients. Anesthesiology. 2008; 108(5): 822-30.
16. Chung F, Yegneswaran B, Liao P, et al. STOP questionnaire: a tool to screen patients for obstructive sleep apnea. Anesthesiology. 2008; 108(5): 812-21.
17. Consenso de Hipertensión Arterial. Consejo Argentino de Hipertensión Arterial “Dr. Eduardo Braun Menéndez”. Sociedad Argentina de Cardiología. Rev Argent Cardiol. 2013; 81: 1-72.
18. Ferrario CM, Basile J, Bestermann W, et al. The role of noninvasive hemodynamic monitoring in the evaluation and treatment of hypertension. Ther Adv Cardiovasc Dis. 2007; 1(2): 113-8.
19. Clinical Guidelines for the Use of Unattended Portable Monitors in the Diagnosis of Obstructive Sleep Apnea in Adult Patients. Portable Monitoring Task Force of the American Academy of Sleep Medicine Journal of Clinical Sleep Medicine. 2007; 3(7): 737-47.
20. Berry RB, Budhiraja R, Gottlieb DJ, et al. Rules for scoring respiratory events in sleep: update of the 2007 AASM Manual for the Scoring of Sleep and Associated Events. Deliberations of the Sleep Apnea Definitions Task Force of the American Academy of Sleep Medicine. J Clin Sleep Med. 2012; 8(5): 597-619.
21. Kario K. Obstructive sleep apnea syndrome and hypertension: ambulatory blood pressure. Hypertension Research. 2009; 32: 428-432.
22. Gaddam K, Pimenta E, Thomas SJ, et al. Spironolactone reduces severity of obstructive sleep apnea in patients with resistant hypertension: a preliminary report. J Hum Hypertens. 2010; 24: 532-7.
23. Friedman O, Bradley TD, Chan CT, Parkes R, Logan AG. Relationship between overnight rostral fluid shift and obstructive sleep apnea in drug-resistant hypertension. Hypertension. 2010; 56: 1077-1082.
24. Dempsey JA, Veasey SC, Morgan BJ, O’Donnell CP. Pathophysiology of sleep apnea. Physiol Rev. 2010; 90: 47–112.
25. Van De Water JM, Miller TW, Vogel RL, Mount BE, Dalton ML. Impedance cardiography: the next vital sign technology? Chest. 2003; 123(6): 2028-33.
26. Skomro RP, Gjevre J, Reid J, et al. Outcomes of home based diagnosis and treatment of obstructive sleep apnea. Chest. 2010; 138: 257-63.
27. Kuna ST, Gurubhagavatula I, Maislin G, et al. Non inferiority of functional outcome in ambulatory management of obstructive sleep apnea. American Journal of Respiratory and Critical Care Medicine. 2011; 183: 1238-44.
28. Borsini E, Blanco M, Bosio M, Schrappe M, Ernst G, Nosetto D, et al. Prevalence of sleep apnea and cardiovascular risk factors in patients with hypertension in a day hospital model. Clin Exp Hypertens. 2017; 5: 1-7.