Autor : Imperiale BelĂŠn1, 2, Di Giulio Beatriz3, Moyano Roberto D.1, 2, Santangelo Ma de la Paz1, 2, TĂĄrtara Silvina4, Alonso Viviana4, Sanjurjo Myriam4, GarcĂa Graciela4, Castellaro Patricia4, Romano Ma Isabel1, 2, Morcillo Nora4
1 Instituto de BiotecnologĂa, Instituto Nacional de TecnologĂa Agropecuaria (INTA/CICV), Buenos Aires 2 Consejo Nacional de Investigaciones CientĂficas y TĂŠcnicas (CONICET), CABA 3 Hospital Petrona V. de Cordero, San Fernando, Buenos Aires 4Hospital Dr. Antonio A. CetrĂĄngolo, Vicente LĂłpez, Buenos Aires, Argentina
Correspondencia : Nora Morcillo nora_morcillo@yahoo.com.ar
Resumen
Introducción: El término micobacterias no tuberculosas (MNT) incluye distintas especies
ambientales capaces de enfermar humanosy/o animales incluso mediante una probable
transmisión zoonótica
Objetivos. Determinar: la importancia clínica de varias especies del género Mycobacterium y la diversidad genética del Complejo M. avium (MAC), la sensibilidad bacteriana in vitro yel éxito del tratamiento especifico.
Materiales y Métodos: Recolección de datos clínicos, epidemiológicos y aislamientos
en el periodo 2009-2016; identificación molecular de los aislamientos; determinación
de la sensibilidad bacteriana in vitro y de la diversidad genética del MAC; evaluación
del tratamiento.
Resultados: Fueron diagnosticados 225 casos de micobacteriosis, con prevalencia
estable ≈ 6% por año, y 22 especies recuperadas: 4 de rápido desarrollo aisladas de 66
pacientes y 18 de lento desarrollo. MAC fue aislado en 95 casos, 40 M. avium hominissuis,
51 M. intracellulare, 3 M. chimaera, 1 M. colombiense. Se observó mayor probabilidad
de enfermar por M. intracellulare en pacientes tratados previamente por tuberculosis (TB).
Los pacientes HIV+ tuvieron riesgo incrementado de enfermedad causada por M. avium
hominissuis. Los aminoglucósidos, fluoroquinolonas y macrólidos fueron las drogas más
activas frente a la mayoría de las MNT. Aproximadamente la mitad de los casos curaron.
Conclusiones: M. intracellulare, M. aviumhominissuis con una gran variabilidad genética, y M. abscessus fueron los patógenos más frecuentemente hallados. Un hallazgo
importante fue el de casos de enfermedad mixta TB+MNT. Estos pacientes requirieron
una terapia con agregado de drogas de segunda línea al esquema terapéutico para TB
habiendo curado la mayoría de ellos.
Palabras clave: Micobacterias no tuberculosas; Diversidad e importancia clinica
Clinical Relevance, Diversity and Genetic Variability of Different Species within the Genus Mycobacterium
Abstract
Introduction: The term non-tuberculous mycobacteria (NTM) includes different ambient species capable of sickening humans and/or animals, even by means of a potential
zoonotic transmission.
Objectives: To determine: The clinical importance of several species within the genus Mycobacterium and the genetic diversity of the M. avium complex (MAC), the in vitro bacterial sensitivity and the success of the specific treatment.
Materials and Methods: Collection of clinical and epidemiologic data and information
about isolates of the 2009-2016 period; molecular identification of the isolates; determination of the in vitro bacterial sensitivity and genetic diversity of the MAC; treatment
evaluation.
Results: 225 mycobacteriosis cases were diagnosed, with a stable prevalence of ≈6%
per year and 22 recovered species: 4 rapidly growing species isolated from 66 patients
and 18 slowly growing species. The MAC was isolated in 95 cases, M. avium hominissuis - 40 cases, M. intracellulare - 51 cases, M. chimaera - 3 cases and M. colombiense - 1
case. We observed a greater probability of getting sick from M. intracellulare in patients
previously treated for tuberculosis (TB). HIV-positive patients had a greater risk of falling ill from M. avium hominissuis. Aminoglycosides, fluoroquinolones and macrolides
were the most active drugs against most NTM. Approximately half of the cases healed.
Conclusions: M. intracellulare, M. aviumhominissuis with great genetic variability and M. abscessus were the most commonly found pathogens. The cases of TB+NTM mixed
disease were an important finding. For treating these patients, it was necessary to add
second line drugs to the therapeutic regimen for TB; and most of them healed.
Key words: Non-tuberculous mycobacteria; Diversity and clinical importance
Introducción
El término “micobacterias no tuberculosas” (MNT) incluye varias especies capaces de producir
un amplio espectro patogénico y ejercer un posible
papel zoonótico entre los animales y el hombre.
Algunas especies son estrictamente patogénicas
mientras que otras pueden causar infecciones oportunistas como ocurre con los miembros del
Complejo Mycobacterium avium (MAC). Sin embargo, la enfermedad causada por las MNT o
micobacteriosis se ha incrementado durante lasúltimas décadas acompañando el aumento en las
causas de inmunodepresión como la infección por
HIV, las enfermedades malignas y autoinmunes
cuyos tratamientos generan las condiciones para que una infección por MNT pueda evolucionar a
enfermedad en los individuos que las padecen1,2.
Las micobacterias de rápido desarrollo (MRD)
fueron definidas como aquellas especies que requieren menos de 7 días para producir colonias
fácilmente observables a simple vistaen los medios
de cultivo sólidos3. Este grupo comprende aproximadamente 56 especies ambientales algunas de
ellas que pueden ser aisladas de seres humanos o
animales. M. fortuitum, M. abscessus, M. chelonae, M. smegmatis, M. immunogenum, M. peregrinum, M. houstonense,M. neworleansense (M. mageritense, M. septicum, M. mucogenicum (previamente
organismos M. chelonae-like), M. wolinskyi y M.
goodii fueron aisladas de pacientes4-6. M. porcinum,
M. farcinogenes y M. senegalense, son considerados
patógenos de importancia veterinaria aunque M.
porcinum fue responsable de un brote en humanos
relacionado con el suministro de agua potable7. M.
abscessus fue subdividido hace pocos años en tres
genomoespecies y más recientemente por Tortoli
y col. en subespeciesdel Complejo M.abscessus: M.abscessus subespecie abscessus, M.abscessussubespecie masiliense y M. abscessus subespecie bolletii8-10. Por razones de simplicidad semántica,
algunas de las especies mencionadas son frecuen-tementeagrupadas e informadas como grupos o
complejos: M. abscessus, que incluye las especies
citadas, y M. fortuitum-chelonae que incluye las
especiesM. chelonae, M. senegalense,M. smegmatis y M. fortuitum7, 10, 11.
Por otro lado, se denominan “micobacterias de
lento desarrollo (MLD) a las especies que requieren
más de sietedíaspara evidenciar un crecimiento
visible en medios sólidos de cultivo2,3. El MAC incluye: M. avium subespecie selvaticum, M. avium
subespecie hominissuis, M. avium subespecie
avium, M. avium subespecie paratuberculosis, M.
intracellulare y las especies recientemente incorporadas M. chimaera y M. colombiense12-14. M. avium
subespecie hominissuis y M. intracellulare son los
patógenos humanos másfrecuentes e importantes,
mientras que M. paratuberculosis (MAP) es un
patógenos bovino de gran importanciaque causa
la Paratuberculosis o enfermedad de Johne en los
animales. Esta misma micobacteria ha sido postulada como agente patogénico de la enfermedad de
Chron en humanos12,13.
Estudios de reciente difusión sobre la secuenciación completa de un total de 120 genomas de cepas consideradas como especies individuales,demostraron que, en algunos casos,
se trataría de especies identificadas previamente
o bienque estarían en una relación filogenética
muy cercana a éstas. Así, han sido incorporados M. nonchromogenicum y M. kumamotonense al
complejo M. terrae; M. chimaera y M. colombiense al MAC; M. ulcerans y M. pseudozhottsii al complejo M. marinum14,15.
A diferencia de lo que ocurre con el diagnóstico
microbiológico de la tuberculosis (TB) y dado el
hábitat natural de las MNT que incluye el suelo y
el agua, el diagnóstico microbiológico de micobacteriosis debe cumplir ciertos requisitos ya establecidos por la Sociedad Americana del Tórax (ATS) que
definen si se trata de una eventual colonización o
si la micobacteria aislada es la verdadera causante
de la enfermedad15.
Los objetivos de este estudio fueron: estimar la
frecuencia e importancia clínicade las MNT como
agentes causantes de enfermedad; determinar la
proporción de casos causados por MLD y MRD;
explorar la aparición de más de una micobacteria
aislada en forma simultanea o no en el mismo
huésped; observar las diferencias en la sensibilidad
de las distintas especies de MNT a los antibióticos;
evaluar el éxito del tratamiento específico; analizar
la diversidad genética del MAC,principal causante
de micobacteriosis, en el periodo comprendido
entre enero 2009 a diciembre 2016.
Material y Método
Durante el periodo de estudio fue recolectada la
siguiente información epidemiológica, demográfica
y clínica de los pacientes: edad, género, partido
de residencia; localización de la enfermedad de
acuerdo con las imágenes obtenidas; infección con
el HIV; co-morbilidades que conducen a un estado
de inmunodepresión; tratamientos previos para TB
o micobacteriosis; número de materiales clínicos
analizados con resultados bacteriológicos.
Se recolectaron tanto especímenes clínicos respiratorios, esputos, lavados bronquial y broncoalveolar y aspirados traqueales, como extrapulmonares,
fluidos pleural, cefalorraquídeo y abdominal,
materia fecal, orina, tejidos, sangre y medula ósea.
Todos los materiales, a excepción de la sangre
y la médula ósea que fueron incubados en el sistema Myco-F-Lytic BACTEC 9050 (BD Argentina),
fueron procesados para la observación microscó-pica directa por la coloración de Ziehl-Neelsen y
cultivados en medios sólidos (Löwenstein-Jensen
y Stonebrink) y en el sistema automatizado BAC-TEC MGIT 960TM 16,17.
La sensibilidad antimicrobiana fue determinada in vitro por medio de un micrométodo colorimétrico
(resazurin micro assay, REMA), que emplea resazurina como colorante vital y que indica tanto el
crecimiento bacteriano como la ausencia de éste18.
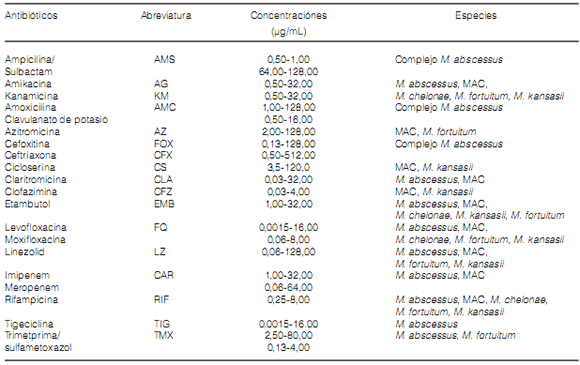
Las drogas incluidas en el antibiograma pueden
verse en la Tabla 1.
La identificación de las distintas especies halladas fue realizada por medio del sistema GenoType
CMTM 19. Cuando los resultados de la identificación
fueron inconclusos, se procedió a secuenciar el gen
del ARNr 16S para identificar correctamente los
aislamientos20, 21.
La diferenciación de los miembros del MAC fue
realizada por medio de la reacción en cadena de
la polimerasa de las secuencia de inserción 1311
(PCR IS1311) (21). La PCR IS901 fue usada para
diferenciar específicamentelas subespecies M. avium subesp. avium (MAA) de M. avium subesp.
Hominissuis22.
La diversidad genética del MAC fue explorada
por medio delestudio del polimorfismo presente en
8 loci con estructura de VNTR-MIRU, mediante la
técnicapreviamente descripta por Thibault et al. 2007 (23).La diversidad alélica (D) de cada locus
y el poder discriminatorio global del esquema
completo de MIRU-VNTR (HGDI) fueron determinadosutilizando el software online editado por
la Universidad del País Vasco23-25 http://insilico.ehu.es/mini_tools/discriminatory_power/ a través de la siguiente fórmula:
Donde N es el número total de aislamientos de
cada tipo de esquema; s es el número total de
distintos subtipos discriminados por el método
de tipificación, y xjes el número de aislamientos
pertenecientes al subtipo xth.
Los patrones hallados fueron comparados con
los registrados en la base de datos internacional
(http://mac-inmv.tours.inra.fr/) de MIRU-VNTR
para MAC y asignados a un determinado número
de patrón, INMV22, 26, 27.
Resultados
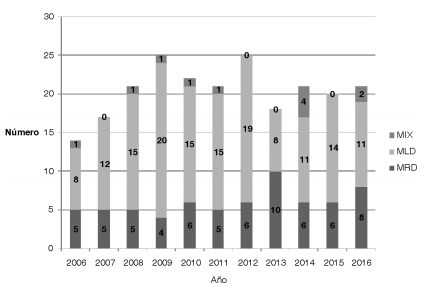
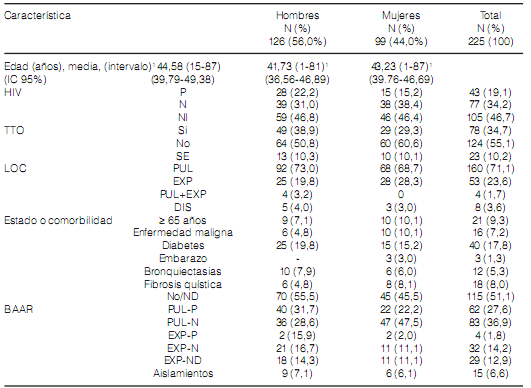
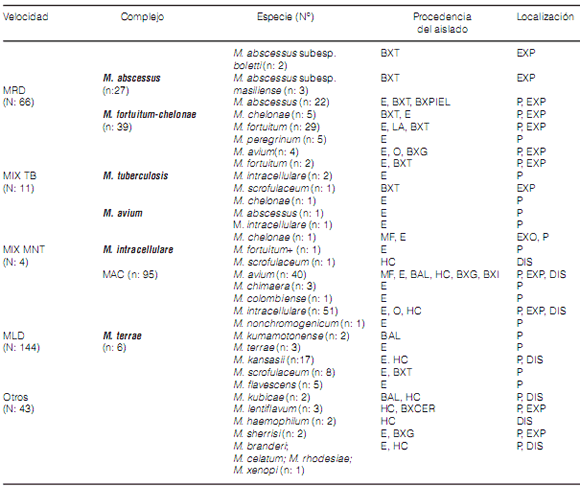
Durante el periodo del estudio el Laboratorio de Micobacterias del Hospital Dr. Antonio A. Cetrángolo, en su carácter de referente provincial, diagnosticó 4.236 casos de enfermedad micobacteriana de los cuales 3.965 (93,9%) fueron confirmados como casos de TB: un caso causado por el bacilo BCG, tres como M. bovis y el resto M. tuberculosis. En 271 (6.8%) casos fue aislada un MNT como posible agente causal de la enfermedad. En total fueron excluidos del estudio 46 (16.9%) casos: en 31 fue aislada una MNTpor única vez (10 aislamientos pertenecían al complejo M. gordonae) que fue desestimada como el agente causal de la enfermedad27. En 6 casos no fue posible obtener la identificación apropiada del aislado y en 9 no la información de los pacientes no estaba completa. De los 225 casos restantes, 66 (29,3%) resultaron con MRD, y 159 (70,7%) con MLD. En 15 (6,7%) casos fueron aisladas dos especies de micobacterias diferentes durante el mismo el episodio de la enfermedad. La Figura 1 y la Tabla 2 muestran respectivamente la frecuencia de aparición de casos con micobacteriosis causadas por MLD y MRD durante los años del estudio, y la diferenciación en especies y complejos de los aislamientos hallados. En la Tabla 3 se consignan las características de los pacientes incluidos en el estudio. El 71,1% de los casos tuvo localización pulmonar y de estos el 38,8% presentaba bacilos al examen directo (BAAR +); 8 pacientes (3,6%), de los cuales 6 tenían coinfección con el HIV, presentaron enfermedad diseminada con bacilos aislados de hemocultivos seriados. En78 (34,7%) pacientes se demostró antecedentes de TB tratada previamente. En 151 (67,1%) casos se presentaban individualmente o en forma simultanea: a) la infección por HIV (43 pacientes); b) una condición física particular (edad avanzada, embarazo); c) alguna co-morbilidad diagnosticada (110 casos, por ejemplo diabetes, bronquiectasias con y sin fibrosis quística, una enfermedad maligna).
Independientemente del sexo del paciente se
observó una mayor probabilidad de desarrollar
micobacteriosis por M. intracellulare en pacientes
con tratamiento previo (odds ratio: 2,71487, IC
95%: 1,087-6,798; X2: 4,398, p: 0.0324) mientras
que los pacientes con infección por el HIV tuvieron más riesgo de desarrollar enfermedad por M.
avium subesp. hominissuis (odds ratio: 7,111, IC
95%: 1,542-33,17; X2: 7,930, p: 0.0125).
En total fueron recuperadas 22 especies diferentes, de las cuales 4 eran MRD, que fueron aisladas
de 66 (29,3%) pacientes: 27 (40,9%) casoscon el
complejo M. abscessus, de los cuales 3 aislamientos
pertenecían a la subespecie M. masiliense y 2 a M. bolletii; y 39 (59,1%) casos con el complejo M. fortuitum-chelonae: 31 M. fortuitum (47,0%), 4 M.
chelonae y 4 M. peregrinum.
Las MLD incluyeron las 18 especies restantes.
MAC fue aislado en 95 (42,2%) casos, 40 debidos
a M. avium subesp. hominissuis, y 51 a M. intracellulare, 3 casos conM. Chimaera y 1 con M.
colombiense.
En la Tabla 2 se muestra el número y la frecuencia de aparición del total de especies identificadas, los casos atribuidos a una infección mixta
y la localización de la enfermedad que produjo los
aislamientos de las distintas especies.
De un total de 27 M. abscessus, 11 (40,7%) provenían de enfermedad pulmonar, mientras que los
16 restantes fueron obtenidos de lesiones cutáneas
y/o heridas provocadas por procedimientos quirúrgicos o cosméticos.
Las cepas de M. avium subesp. hominissuis tuvieron localización pulmonar, extrapulmonar
y diseminada mientras que M. intracellulare no
causó enfermedad diseminada entre los casos
estudiados como si se comprobó, en cambio, en
casos con M. kansasii. Las especies M. flavescens, M. kubicae, M. lentiflavum, M. haemophilum, M. sherrisi, M. branderi, M. celatum, M. rhodesiae y M. xenopi fueron capaces de producir enfermedad
pulmonar, extrapulmonar y diseminada según la
procedencia de las muestras desde donde fueron
aisladas las bacterias y los datos clínicos de los
pacientes.
En un total de 15 casos se hallaron infecciones
mixtas:en 11 pacientes se aisló M. tuberculosis asociado a otras especies. En 4 casos HIV+ el segundo
germen hallado fue M. avium subesp. hominissuis;
en 2 casos HIV+ lo fue M. intracellulare, mientras
que en pacientes HIV negativos las asociaciones
fueron: en1caso con M abscessus, en 2 con M.
fortuitum, en 1 con M. chelonaey1 con M. kubicae.
Este último fue un paciente añoso internado en
una institución para mayores.
En otros 4 casos los hallazgos microbiológicos
se produjeron en general durante el tratamiento
para el primer germen aislado. Estos 4 casos fueron
los siguientes:
a) paciente añoso: en el año 2010 se aisló M. fortuitum y en el año 2011, antes de finalizar el
tratamiento correspondiente, se aisló M. intracellulare
b) paciente HIV+: se aisló M. avium subesp. hominissuis y durante el tratamiento especifico y
en el mismo año, M. intracellulare
c) paciente HIV+: se aislaron simultáneamente M.
chelonae y M. avium subesp. hominissuis en el
mismo episodio de enfermedad
d) paciente HIV+: aislamiento en el año 2008 desde esputo de M. intracellulare. En el año 2009
y durante el tratamiento por la micobacteriosis
se aisló desde hemocultivo, M. scrofulaceum
En estos últimos 15 casos las infecciones mixtas
se asociaron con los antecedentes de tratamiento
previo y/o actual en el grupo masculino (odds ratio:
1,5933 (95% IC: 0,6096-3,8217).
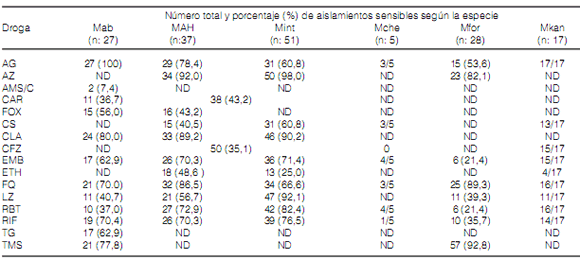
La Tabla 4 consigna el número y porcentaje
de aislamientos de cada especie, sensibles a cada
una de las drogas detalladas en la Tabla 1. EMB y RIF fueron las únicas drogas de primera línea
empleadas en el tratamiento de la TB que fueron
incluidas en los antibiogramas de MNT. La RIF
fue probada en 165 (75,7%) aislados en total de los
cuales 109 (66,0%) resultaron sensibles a la droga.
El EMB mostró una actividad inhibitoria global del
84,8% (140/165 aislados) ejercida especialmente
sobre M. kansasii y algunas cepas del MAC y M.
chelonae. M. abscesus, MAC y M. kansasii fueron
mayormente susceptibles a CLA; M. fortuitum y
MAC a la AZ. La CFZ mostró actividad en poco
más de un tercio de las cepas del MAC mientras
que M. kansasii se mostró muy sensible a este
antibiótico. Las FQ (levofloxacina y moxifloxacina)
ensayadas inhibieron más del 70% de las especies.
De los antibióticos beta-lactámicos, AMS, AMC y
FOX, sólo éste último fue activo frente al complejo M. abscessus. Dos tercios de estas cepas fueron
inhibidas por AG, FOX, CLA, FQ, RIF y TMS
mientras que un porcentaje menor (alrededor del
60%) también lo fue por EMB y TG. La mayoría
de las cepas del MAC fue inhibida por AG, AZ,
CLA, EMB, FQ, RIF y RBT. La actividad del LZ
fue mayor sobre los aislados de M. intracellulare que sobre los de M. avium.
El 80% de los MAH (n: 32) fue correctamente
genotipificado, exhibiendo una gran diversidad
genética. Por la técnica MIRU-VNTR fueron
hallados 5 patrones conocidos y otros 6 patrones
recientemente publicados por nuestro grupo y no
reportados previamente en la literatura28. Los loci X3 y 292 mostraron el mayor índice de discriminación (D) entre los aislamientos de MAH (0.7424
y 0.6515), obteniéndose un altoHGDI (0,9697).
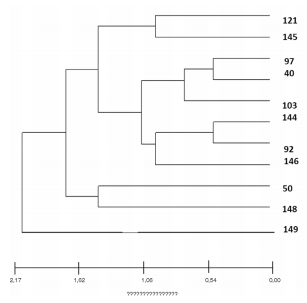
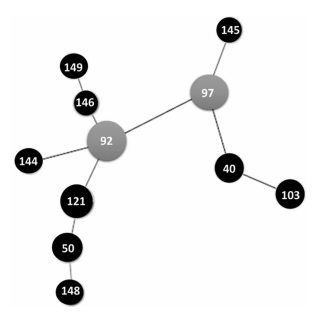
En las Figuras 2 y 3 pueden observarse los
patrones (INMV) genéticos de MAH encontrados
y la relación filogenética existente entre los mismos. Las relaciones entre los diversos patrones
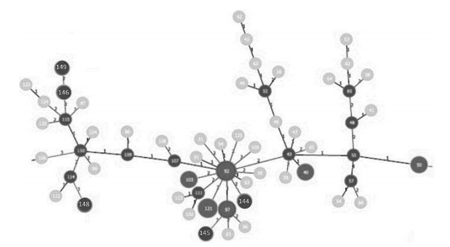
INMV son mostradas en un dendrograma de la Figura 2. Las Figuras 3 y 4 muestran las relaciones clonales entre los distintos patrones, representadas por el Minimum Spanning Tree (MST)
construido a partir del algoritmo de goeBURST.
Se asume generalmente que la distancia genética
entre dos patrones de INMVes proporcional a la
diferencia del número de repeticiones de cada locus. Estas relaciones fueron establecidas utilizando el Software Phyloviz 2 (http://goeburst.phyloviz.net)26.
Con respecto al éxito del tratamiento específico,
fueron evaluados un total de 109 (63,7%) de los 171
(76,0%) pacientes que lo comenzaron en el periodo 2009-2014. En 71 (65,1%) casos la cohorte consignaba “tratamiento terminado o curado” (TT/C).
El abandono de la terapia y los fallecimientos
ascendieron a 12,8%, con 8 y 6 pacientes respectivamente, se produjeron 6 (5,5%) recaídas y 16 casos
(14,7%) figuraban en continuación del tratamiento
al momento de la evaluación. De los 62 (36,3%)
pacientes restantes no se obtuvo información.
De los 54 (24,0%) pacientes que iniciaron tratamiento en los años 2015 y 2016 fue posible evaluar
el éxito en 41 (76,0%), de los cuales 3 (7,3%) murieron, 4 (9,8%) fueron registrados como TT/C y 34
(83,0%) continuaban en tratamiento a la fecha del
relevamiento. De los 11 casos con infección mixta,
7 fueron notificados comoTT/C. El éxito global
del tratamiento fue estimado en 50,0 % según la
relación entre elnúmero de casos evaluados en el
período 2009-2015 (n: 150) y los TT/C (n: 75).
Conclusiones
Las MNT son organismos ubicuos, naturalmentede
vida libre, consideradas agentes infecciosos oportunistas especialmente en huéspedes con alteraciones de la inmunidad celular en los que producen
una enfermedad semejante a la TB, denominada
genéricamente micobacteriosis28.
La incidencia de MNT fue de alrededor del 6,0%
de todos los casos inicialmente considerados como
TB con una tendencia más o menos estable durante
el periodo considerado.Estos resultados comparados con los publicados previamente, muestran una
tendencia estable en el tiempo de la aparición de
MB en nuestro medio20.
En este estudio los pacientes presentaron
mayoritariamente lesiones con localización respiratoria si bien la enfermedad pudo ser también
extrapulmonar, mixta o diseminada; más de un
tercio habían recibido tratamiento previo para TB
y casi la mitad presentaba co-morbilidades como
patología de base concordando este dato con lo
publicado previamente29-31. Sin embargo, la TB
previa fue el factor de riesgo más importante para
las micobacteriosis causadas especialmente por M. intracellulare que junto con M. avium subesp. hominissuis fueron los patógenos más frecuentemente hallados.
En total fueron recuperadas 22 especies de MNT
diferentes con predominio de las MLD.
Las MRD y, particularmente, los miembros del
complejo M. abscessus, son considerados patógenos oportunistas emergentes que pueden causar
infecciones pulmonares crónicas y afecciones en
la piel, tejidos blandos, huesos y articulaciones.
Existen numerosas publicaciones donde estas
MRD están involucradas en infecciones asociadas
a heridas traumáticas, cirugías y procedimientos
diversos: acupuntura, liposucción, mesoterapia,
implantación de prótesis mamarias29-31.
En este estudio el número de casos con localización pulmonar de la enfermedad causada por
el complejo M. abscessus, aislado de tejidos y esputos, fue similar al de los casos no respiratorios. M. nonchromogenicum y M. peregrinum fueron
también encontrados aunque con baja frecuencia
y localización exclusivamente pulmonar.
Entre las MRD, las especies de los complejos M. abscessus y M. fortuitum-M. chelonae fueron
las más frecuentemente aisladas, estas últimas
preponderantemente de afecciones pleuro-pulmonares.
Dentro del MAC los patógenos más frecuentemente hallados fueron M. intracellulare y M.
avium subesp. hominissuis aunque también fueron aislados M. chimaera y M. colombiense. Los miembros del MAC junto a M. kubicae y M. haemophilum fueron causantes de enfermedad diseminada. M. avium subesp. hominissuis presentó gran
variabilidad genética, hecho que sugiere diversidad
de fuentes de infección. Además, la TB previa fue
el factor de riesgo más importante especialmente
para la enfermedad por M. intracellulare.
Otras especies de MLD como M. kumamotonense y M. rhodesiae fueron también halladas aunque en
baja proporción.
Algunas MNT, como los miembros del MAC,
pueden infectar no solamente aves sino también
a mamíferos como el cerdo. Recientemente ha
sido publicado un estudio efectuado en Bélgica
donde más del 98% de los aislamientos de cerdos
correspondieron a M. avium subesp. hominissuis hallazgo podría sugerir una transmisión zoonótica
de estas micobacterias25. Este último punto hace
pensar en la necesidad de planificar estudios de
tipo genético y epidemiológico que permitieran
corroborar o bien descartar la potencial zoonosis
en las micobacteriosis y, asimismo, evaluar una
posible transmisión directa entre huéspedes.
Si bien los resultados de los antibiogramas
efectuados sobre las MNT tienen un carácter
informativo y deben ser tomados con precaución
por parte de los médicos tratantes, los resultados
de este estudio mostraron concordancia con lo
publicado previamente por varios autores31-33. En
general los aminoglucósidos, las fluoroquinolonas
y los macrólidos fueron las drogas ensayadas más
activas frente a la mayor variedad de MNT, si
bien ninguna especie se mostró homogéneamente
sensible a ellas. Las demás drogas mostraron una
relación especie dependiente más manifiesta. En
este sentido la identificación del germen a nivel de
especie es importante como predictor de la sensibilidad a los fármacos y una guía para el médico en
la implementación de una terapia adecuada. Recientemente ha sido publicada una revisión sobre
nuevos antimicrobianos con actividad frente a las
MNT en varios estadios de desarrollo32. En este
estudio, la evaluación de las cohortes demostró que
alrededor de la mitad de los casos con micobacteriosis curaron si bien se registró una importante
pérdida de la información y las cohortes resultaron
muy incompletas.
Un hecho remarcable fue el hallazgo simultáneo
de M. tuberculosis causando enfermedad conjuntamente con una MNT. La recuperación simultánea
de M. tuberculosis junto a una MNT fue interpretado como una causa conjunta de enfermedad. Los
casos fueron tratados con esquemas normatizados
para TB empleando en la fase inicial isoniacida,
rifampicina, etambutol y pirazinamida, drogas a
las cuales los M. tuberculosis aislados eran originalmente sensibles. El tratamiento convencional
continuó hasta que la detección de las MNT y/o la
falla del tratamiento (mantenimiento de baciloscopías y cultivos positivos) llevaron a personalizar los
esquemas terapéuticos agregando al convencional
aminoglucósidos, fluoroquinolonas y alguna otra
droga de acuerdo con la especie de MNT identificada (Tártara comunicación personal), los esquemas
recomendados y los resultados de sensibilidad in
vitro obtenidos para el aislamiento33. La mayoría
de estos casos se curaron.
Con respecto a la variabilidad de los aislamientos de M. avium subesp. hominissuis obtenidos,
la técnica molecular utilizada permitió demostrar
la existencia de una alta diversidad genética entre
los aislamientos. Además, los patrones de INMV
obtenidos en este estudio pudieron ser comparados
y analizados con los reportados por otros autores
en la base de datos internacional (MAC-INMV)24.
La elaboración del MST permitió establecer relaciones clonales entre los distintos aislamientos. El
INMV 92 resultó ser clon originario tanto cuando
el MST incluyo sólo a los aislamientos del estudio,
como a los reportados mundialmente en la base
de datos. Hecho que confirma su rol como clon a
partir del cual derivan otros aislamientos de M.
avium subesp. hominissuis.
Agradecimientos. A Marcelo Mazza, Guillermo Alonso, Bibiana Zingoni y Claudia Palavecino por su excelente trabajo técnico.
Conflicto de interés: Los autores del trabajo declaran no tener conflictos de intereses relacionados con esta
publicación.
BRI, MPS y MIR son investigadores de CONICET; DM
es becario postdoctoral de CONICET.
1. Nunes-Costa D, Alarico S, Pretti Dalcolmo M, Correia-Neves M, Empadinhas N. The looming tide of nontuberculous mycobacterial infections in Portugal and Brazil. Tuberculosis 2016; 96: 107-119.
2. Stahl, DA, Urbance JW. The division between fast- and slow-growing species corresponds to natural relation-ships among the mycobacteria. J Bacteriol 1990; 172: 116-124.
3. Tortoli E. Microbiological features and clinical relevance of new species of the genus Mycobacterium. ClinMicrobiolRev 2014; 27: 727e52. En: http://dx.doi.org/10.1128/CMR.00035-14.
4. Brown-Elliot BA, Griffith De, Wallace RJ. New described emerging human species of nontuberculous mycobacteria. Infect Dis Clin N Am 2002; 16:187-220.
5. Shinnick TM, Good RC. Mycobacterial taxonomy. Eur J Clin Microbiol Infect Dis 1994; 13: 884-901.
6. Tsang AY, Barr VL, McClatchy JK, Goldberg M, Drupa I, Brennan PJ. Antigenic relationships of the Mycobacterium fortuitum- M. chelonae complex. Int J Syst Bacteriol 1984. 34: 35-44.
7. Brown-Elliott BA, Wallace RJ Jr ., Tichindelean Cet al. Five-Year Outbreak of Community and Hospital-Acquired Mycobacterium porcinum Infections Related to Public Water Supplies. J Clin Microbiol 2011; 49: 4231-4238.
8. Sassi M, Drancourt M. Genome analysis reveals three genomospecies in Mycobacterium abscessus. BMC Genomics 2014; 15:359 En: http://www.biomedcentral.com/1471-2164/15/359.
9. Tortoli E, Kohl TA, Brown-Elliott BA et al.Emended description of Mycobacterium abscessus, Mycobacterium abscessus subsp. abscessus and Mycobacterium abscessus subsp. bolletii and designation of Mycobacterium abscessus subsp. massiliense comb. Nov. International Journal of Systematic and Evolutionary Microbiology. 2016; 66: 4471–4479.
10. Tan JL, Ngeow YF , Choo SW. Support from Phylogenomic Networks and Subspecies Signatures for Separation of Mycobacterium massiliense from Mycobacterium bolletii. J Clin Microbiol 2015; 53: 3042-3046.
11. Brown-Elliott B A, Wallace RJ. Clinical and Taxonomic Status of Pathogenic Nonpigmented or Late-Pigmenting Rapidly Growing Mycobacteria. Clinical Microbiology Reviews2002; 15: 716–746.
12. Narnaware SD, Periasamy S, Tripathi BN. Studies on pathology, cytokine gene expression and molecular typing of Mycobacterium avium subsp. paratuberculosis of naturally occurring Johne’s disease in bullocks. Res Vet Sci. 2016; 106:74-80.
13. Kan P, Pilli AS, Rampal R et al. Prevalence and Association of Mycobacterium avium subspecies paratuberculosis with disease course in patients with ulcero-constrictive Ileocolonic disease.PLoS One. 2016; 11(3): e0152063.doi: 10.1371/journal.pone.0152063.
14. Griffith DE, Aksamit T, Brown-Elliot BA, Cattanzaro A, Daley C, Gordon F. An official ATS/IDSA statement diagnosis, treatment and prevention of nontuberculous mycobacterial disease. Am J Respir Crit Care Med 2007; 175: 367-416.
15. American Thoracic Society. Diagnosis and treatment of disease caused by nontuberculous mycobacteria. Am J Respir Crit Care Med 1997; 156:S1–S25.
16. Tortoli E. The impact of whole genome sequencing on the taxonomy of mycobacteria. European Society of Mycobacteria, 37th Annual Congress, 3rd to 6th July 2016, Catania, Sicily, Italia. Scientific Program and Abstracts Book, pp: 29.
17. Becton Dickinson. BBL MGIT Products for the Detection of Mycobacteria. Becton Dickinson Cockeysville, Maryland, USA. Insert 88-0950, 1996.
18. Jacomo V, Musso D, Gevaudan MJ. Isolation of blood-borne Mycobacterium avium by using the nonradiactive BACTEC 9000 MB system and comparison with a solid-culture system. J ClinMicrobiol. 1998; 3703-3706.
19. Martin A, Paasch F, Docx S, et al. Multicentre laboratory validation of the colorimetric redox indicator (CRI) assay for the rapid detection of extensively drug-resistant (XDR) Mycobacterium tuberculosis. J Antimicrob Chemother 2011; 66: 827-833.
20. Richter E, Rüsch-Gerdes S, Hillemann D. Evaluation of the GenoType Mycobacterium Assay for Identification of Mycobacterial Species from Cultures. J Clin Microbiol. 2006; 44: 1769-1775.
21. Imperiale B, Zumárraga M, Gioffré A, Di Giulio B, Cataldi A, Morcillo N. Disease caused by non-tuberculous mycobacteria: diagnostic procedures and treatment evaluation in the North of Buenos Aires Province..Rev Argent Microbiol2012; 44:3-9.
22. Travería G, Zumárraga M, Etchechoury I et al. First identification of Mycobacterium avium paratuberculosis sheep strain in Argentina. Brazilian J Microbiology 2013; 44: 897-899.
23. Thibault VC, Grayon M, Boschiroli ML et al. New variablenumber tandem-repeat markers for typing Mycobacterium avium subsp. paratuberculosis and M. avium strains: comparison with IS900 and IS1245 restriction fragment length polymorphism typing.J Clin Microbiol 2007; 45: 2404-2410.
24. Imperiale B, Moyano RD, Di Giulio AB et al. Genetic diversity of Mycobacterium avium complex strains isolated in Argentina by MIRU-VNTR. Epidemiology and Infection, Cambridge University Press 2017, pp: 1-10 doi: 10.1017/S0950268817000139.
25. Vluggen C, Soetaert K, Duytschaever L et al. Genotyping and strain distribution of Mycobacterium avium subspecies hominissuis isolated from humans and pigs in Belgium, 2011-2013. Euro Surveill. 2016; 21: 30111. doi: 10.2807/1560-7917.ES.2016.21.3.30111.
26. Hunter P. Reproducibility and indices of discriminatory power of microbial typing methods. J Clin Microbiol 1990; 28: 1903-1905.
27. Hunter PR, Gaston MA. Numerical index of the discriminatory ability of typing systems: an application of Simpson’s index of diversity. J ClinMicrobiol1988; 26:2465- 2466.
28. Francisco AP, Vaz C, Monteiro PT, Melo-Cristino J, Ramírez M, Carric JA. PHYLOViZ: phylogenetic inference and data visualization for sequence based typing methods. BMC Bioinformatics 2012, 13:87.DOI: 10.1186/1471-2105-13-87.
29. Wassilew N, Hoffmann H, Andrejak C, Lange C. Pulmonary Disease Caused by Non-Tuberculous Mycobacteria. Respiration 2016;91:386–402. DOI: 10.1159/000445906.
30. Rivera-Olivero IA, Guevara A, Escalona A et al. Infecciones en tejido blando debidas a micobacterias no tuberculosas posterior a mesoterapia. ¿Cuál es el precio de la belleza? Enferm Infecc Microbiol Clin. 2006; 24: 302-306.
31. Da Mata O, Hernández-Pérez R, Corrales H, Cardoso-Leao S, de Waard J. Seguimiento de un brote de infección en tejido blando causado por Mycobacterium abscessus posterior a la mesoterapia en Venezuela. Enferm Infecc Microbiol Clin 2010; 28:596-601.
32. I. Porvaznik, I. Solovicˇ J, Mokry J. Non-Tuberculous Mycobacteria: Classification, Diagnostics, and Therapy. Advs Exp. Medicine, Biology. Neuroscience and Respiration 2016. DOI 10.1007/5584_2016_45.
33. Soni I, De Groote MA, Dasgupta A, Chopra S. Challenges facing the drug discovery pipeline for non-tuberculous mycobacteria. J Medical Microbiol2016; 65: 1–8.
34. Brown-Elliott BA, Nash KA, Wallace RJ Jr. Antimicrobial Susceptibility Testing, Drug Resistance Mechanisms, and Therapy of Infections with Nontuberculous Mycobacteria. Clinical Microbiology Reviews. CMR J Association for Microbiology 2012; 25: 545-582.