Autor : Bethy Camargo#, Fernando DiTullio, MartĂn Bosio, Reynaldo Smith, Eduardo Borsini, Romina Canzonieri, Alexis Muryan, Alejandro Iotti, Alejandro Salvado, Ernst Glenda
Hospital Británico de Buenos Aires # Becaria del programa de entrenamiento en la técnica de esputo inducido del Hospital Británico
Correspondencia : Dra Glenda Ernst e-mail: gernst@hbritanico.com.ar Domicilio postal: Hospital Británico de Buenos Aires Perdriel 74, 1° Piso. CP 1280AEB Tel.: (5411) 43096400 ext 2808
Resumen
El tabaquismo es la principal causa de la EPOC, sin embargo, factores como la edad de
diagnóstico, la historia previa de asma, exacerbaciones, predisposición genética y otros
influirían en el desarrollo de la enfermedad. Esto estaría relacionado con los fenotipos de
pacientes con EPOC, los cuales tendrían diferentes respuestas a los corticoides inhalados
(CI). Recientemente, ha sido propuesto que los eosinófilos serían potenciales biomarcadores predictores de buena respuesta a los CI. Con la hipótesis de que la presencia
de eosinófilos en esputo podría constituir una estrategia para diferenciar fenotipos de
pacientes con EPOC, evaluamos los perfiles celulares infamatorios en muestras de esputo
inducido en pacientes con EPOC no exacerbados.
Para esto, se reclutaron 20 pacientes con EPOC moderado a severo que concurren al
gimnasio de rehabilitación respiratoria, los cuales fueron agrupados en eosinofílicos (n: 8,
cuando presentaron más de 3% de eosinófilos en la muestra de esputo inducido) o no
eosinofílicos (n: 9). Se descartaron 3 muestras por contaminación con células epiteliales.
Si bien no se observaron diferencias significativas en los test de función pulmonar o
de marcha de 6 minutos, los pacientes con eosinoflia presentaron ligeramente mayor
reversibilidad luego del broncodilatador. Además, tuvieron mayor eosinofilia periférica,
mayores valores de FeNO y mejor calidad de vida (medida por cuestionarios) que los
pacientes no eosinofílicos. El esputo inducido es una técnica no invasiva, económica,
que representaría una herramienta útil para conocer los diferentes fenotipos inflamatorios
en pacientes con EPOC.
Palabras clave: Esputo inducido; EPOC; Eosinófilos; Fenotipos; Corticoides inhalados
Abstract
Heterogeneity of Infammatory Phenotypes In Copd Patients: Role of Differential Cell Counting in Sputum
Smoking is the major cause of COPD; however factors such as age, previous history
of asthma, exacerbations, and genetic predisposition could infuence the development
of the disease. This could be related with the phenotypes of COPD patients, who would
have different responses to inhaled corticosteroids (ICs). Recently, it has been suggested
that eosinophils are potential biomarkers that contribute to predict good response to
ICs. To test the hypothesis that the presence of eosinophils in sputum could be useful to
characterize different phenotypes of COPD patients, we assessed the infammatory cell
profles in induced sputum samples from not exacerbated COPD patients.
20 patients with moderate to severe COPD, attending a pulmonary rehabilitation gym, were
grouped into eosinophilic (8 patients who presented more than 3% eosinophils in the
induced sputum sample) or neutrophilic (9 patients who had more than 60% neutrophils).
Only 3 patients were excluded due to contamination of the sputum with epithelial cells. Although there were no-signifcant differences in the pulmonary function tests or the
6-minute walk, the patients with eosinophilia showed higher responsiveness to bronchodilator therapy. Besides this group presented an increase of peripheral eosinophils,
higher FeNO and better quality of life (measured by questionnaires) compared with the
neutrophilic patients.
Induced sputum is an economic non-invasive technique and would be a useful tool to
know different infammatory phenotypes in COPD patients.
Key words: Induced sputum; COPD; Eosinophils; Phenotypes; Inhaled corticosteroids
Introducción
La enfermedad pulmonar obstructiva crónica
(EPOC) tiene alta morbi-mortalidad, por lo que
constituye un verdadero desafío para médicos e
investigadores. La Organización Mundial de la
Salud ha revelado que en el año 2030 la EPOC
sería la tercera causa de muerte en el mundo1. La
calidad de vida de estos pacientes se ve gravemente
afectada, especialmente en estadios avanzados2,
esto se asocia con una elevada carga económica
para el sistema sanitario. La Unión Europea ha
dado a conocer que los costos directos totales de
las enfermedades respiratorias serían aproximadamente del 6% del presupuesto total de salud y
que la EPOC representaría el 56%3. En España,
el costo directo total de la EPOC estimado durante
el año 2012 fue de 4.169,81 millones de euros4.
El principal factor de riesgo relacionado con
el desarrollo de esta enfermedad es el cigarrillo5,
sin embargo, se ha descripto que existirían otros
factores que influyen en su evolución. Dentro de
estos, se encuentran la edad, historia previa de
asma bronquial, predisposición genética e infecciones respiratorias6-9. En adición a esto, factores
del medio ambiente u ocupacionales, tales como la
exposición a biomasa o a inhalación de determinadas sustancias, podrían incrementar el riesgo de
padecer EPOC10, 11.
La EPOC se caracteriza por limitación persistente del flujo aéreo, que progresa asociado a la
inflamación de la vía aérea generada por la exposición a noxas o gases. La severidad de la enfermedad
en cada paciente está dada por las exacerbaciones
y comorbilidades12. La inflamación crónica puede
causar remodelación de la vía aérea e incluso destrucción del parénquima pulmonar que altere su
funcionalidad13. Las exacerbaciones usualmente
requieren visitas no programadas que en ocasiones incluyen internación del paciente ya sea por el empeoramiento de los síntomas respiratorios,
infecciones o eventos cardiovasculares, etc. En
estos pacientes, las exacerbaciones conducen a un
empeoramiento de la calidad de vida, un incremento de la severidad de la enfermedad, acompañado
de una reducción de la expectativa de vida14.
En virtud de heterogeneidad de la presentación
clínica de la EPOC, se ha propuesto la estratificación de los pacientes de acuerdo a marcadores
clínicos y biológicos. Estos incluirían la potencial
respuesta farmacológica a los corticoides inhalados
y la presencia de eosinofilia en las vías respiratorias. Algunos autores sugieren que los niveles de
eosinofilia periférica podrían ser utilizados como
biomarcadores que contribuyan a determinar su
respuesta15.
Se ha demostrado previamente que más del 30%
de los pacientes con EPOC presentarían eosinofilia
periférica16. Más aún, se ha descripto un incremento de la eosinofilia durante las exacerbaciones en
pacientes con EPOC moderado o leve, lo que mostró valores en esputo mayores al 3% y en sangre
periférica mayores al 2%17. De esta manera, la eosi-
nofilia podría constituir un bio-marcador predictor
de las exacerbaciones, así como la identificación
de potenciales respondedores al tratamiento con
corticoides inhalados18, 19. Si bien los eosinófilos en
esputo parecerían ser mejores predictores que los
eosinófilos periféricos, la técnica de esputo inducido no es una práctica habitual ya que requiere
personal altamente entrenado, infraestructura
especial y procesamiento inmediato. Además, se ha
propuesto como bio-marcador subrogante de la inflamación eosinofílica durante las exacerbaciones
en EPOC, la determinación de la fracción de óxido
nítrico en aire exhalado (FeNO)20, 21. Se ha sugerido
que los valores de corte de FeNO para pacientes
con asma serían mayor de 50 ppb, síndrome de
overlap Asma-EPOC entre 25 y 50 ppb y para los
pacientes con EPOC menor de 25 ppb22. A partir de estos valores, según la Sociedad Americana
de Tórax (ATS-2011), los pacientes con EPOC y
FeNO menor de 25 ppb no tendrían una fuerte
recomendación para recibir corticoides inhalados,
mientras que los pacientes con FeNO entre 25 y 50
deberían ser manejados a criterio del neumonólogo
y finalmente los pacientes con FeNO mayor a 50
tendrían indicación de corticoides inhalados23, 24.
Dado que la medición del FeNO no es una
práctica habitual en la mayoría de los centros de
salud por falta de disponibilidad, por su elevado
costo y su cuestionada especificidad; nosotros
hipotetizamos que la presencia de eosinófilos en
esputo podría constituir la mejor estrategia para
diferenciar los fenotipos de pacientes con EPOC.
El objetivo es evaluar el rol del recuento celular
diferencial en el esputo inducido para evaluar la
presencia de diferentes fenotipos de pacientes con
EPOC estables.
Materiales y métodos
Diseño: Estudio prospectivo en pacientes con
EPOC moderado a severo GOLD D (definido por
espirometría y exacerbaciones) que concurren al
gimnasio de Rehabilitación Respiratoria del Hospital Británico de Buenos Aires.
Pacientes: Todos los pacientes firmaron un
consentimiento informado que contó con la evaluación y el aval del comité de revisión institucional
del Hospital Británico. A los pacientes reclutados,
se les realizó una prueba de esputo inducido para
evaluar el perfil celular inflamatorio. Solo se incluyeron pacientes que no hubieran exacerbado
en las cuatros semanas. Se incluyeron pacientes
mayores de 40 años del servicio de Neumonología
del Hospital Británico, que firmaron el consentimiento informado y que tuvieron diagnóstico de
EPOC conforme los criterios de las últimas guías
GOLD 2015, que fueron ex tabaquistas o tabaquistas de al menos 10 paquetes/año, que tuvieron
una relación FEV1/FVC ≤ 0.7 y FEV1 menor del
70%. Se excluyeron pacientes que presentaron
síntomas de exacerbación de EPOC o eventos
cardiovasculares en las 4 semanas previas a la
incorporación al estudio y pacientes con enfermedad pulmonar intersticial difusa, enfermedades
neoplásicas, vasculitis, con compromiso pulmonar,
enfermedades renales crónicas, cirrosis hepáticas,
enfermedades sistémicas no controladas (diabetes,
hiper/ hipotiroidismo, enfermedad cardiovascular activa), bronquiectasias con infección aguda en las últimas 4 semanas o fibrosis quística y pacientes
con diagnóstico de neumonía.
Cuando el paciente fue incluido en el estudio,
realizó el cuestionario (CAT), la determinación
del FeNO, espirometría (con la suspensión del
tratamiento inhalatorio 24 hs previas al estudio)
y finalmente se indujo el esputo. Se solicitó una
muestra de sangre para hemograma y determinación de la proteína alfa-uno antripsina que
se realizó en la misma semana del resto de las
determinaciones.
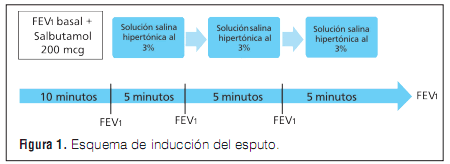
Inducción del esputo: Se procedió de acuerdo
al protocolo previamente establecido25. Brevemente, se obtuvieron los plugs de moco, obtenidos con
una pinza a partir de muestras frescas, se resuspendieron en DTT al 0.1% durante 20 minutos en
agitación, se realizó una citocentrifugación a 300
RPM durante 5 minutos, las muestras se fijaron
y se realizó una coloración de May Grundwald-Giemsa. Se realizaron hasta 3 nebulizaciones con
solución salina hipertónica durante 5 minutos,
controlando que el FEV1 no descendiera más del
20% según lo indicado en el esquema mostrado en
la Figura 1. Se utilizó solución salina hipertónica
que varió su concentración en un rango de 0.9 a
3.0%, según al valor del FEV1 de cada paciente. Las
muestras se procesaron con dithiotreitol (DTT) al
0.1% y se centrifugaron para realizar el recuento
diferencial. Se descartaron las muestras que presentaron más del 5% de células epiteliales26.
Se consideró como criterio para clasificar los
pacientes de acuerdo a la celularidad
Determinación de los niveles de FeNO: Se
midieron los niveles de óxido nítrico en aire exhalado mediante la utilización del equipo NIOX
MINO (Aerocrine).
Determinación de los niveles de la proteína
alfa-uno: Se dosaron muestras de una gota de
sangre seca en papel por nefelometría cinética con
un valor de corte correspondiente a 100 mg/dL de
1.8 mg/dL.
Test de función pulmonar: Todos los pacientes fueron sometidos a test de función pulmonar
(TFP) que incluyó espirometrías y la capacidad
de difusión de monóxido de carbono (DLCO) realizados de acuerdo a las recomendaciones de la
ATS/ERS. Para las mediciones de TFP, se utilizó un equipo de volumen constante (Platinum Elite
DL, Medical Graphics Corporation). Los valores
normales predichos fueron referidos a los de Crapo. Estos fueron realizados el mismo mes en que se
tomó la muestra de esputo inducido27,28.
Análisis de los datos: Los resultados se analizaron mediante test no paramétricos utilizando
el software Graph-Pad PRISM-5 (Graph Pad, La
Jolla, CA). Para la estadística descriptiva, se informaron las medias y el desvío estándar. Para comparar las diferencias entre dos grupos, se utilizó el test de Mann Withney y cuando se compararon
los resultados de tres o más grupos, se utilizó el
test no paramétrico de Kruskal Wallis y el test de
comparaciones múltiples de Dunn. Se consideró estadísticamente significativamente una p < 0.05.
Resultados
Población estudiada
Se reclutaron 20 pacientes, de los cuales 17 fueron
hombres; un paciente fumador activo y el resto
exfumadores (con más de un año sin fumar) con
una carga tabáquica de 53.3 ± 7.3 paquetes/año.
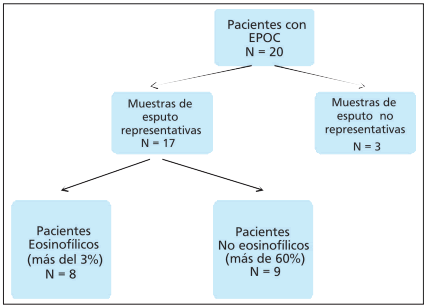
Los pacientes se agruparon de acuerdo al recuento celular diferencial en las muestras de esputo
inducido tal como se observa en la Figura 2, tres
muestras fueron excluidas por contaminación con
células epiteliales. Si bien la mayoría de los pacientes fueron nebulizados con solución salina hipertónica al 3%, en cuatro de ellos se utilizó solución
salina al 0.9% por presentar FEV1 menor de 1L.
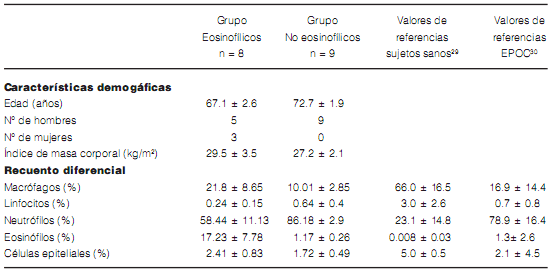
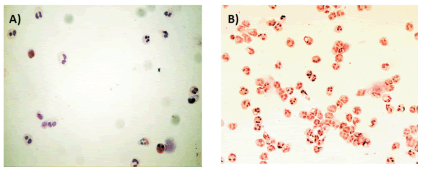
Dado que el esputo inducido constituye una técnica mínimamente invasiva, reproducible, validada y segura en pacientes con enfermedad pulmonar crónica tanto estables como exacerbados; la misma se utilizó para evaluar la heterogeneidad en los perfiles celulares inflamatorios de 17 pacientes con EPOC29, 30. Esto permitió organizar los pacientes en 2 grupos: eosinofílicos y no eosinofílicos (Tabla 1). En la Figura 3 se observan imágenes representativas de los patrones encontrados en nuestros pacientes.
Características de los diferentes fenotipos de pacientes con EPOC
El grupo de pacientes no eosinofílicos presentó
en promedio mayor carga tabáquica que los pacientes eosinofílicos; sin embargo, estas diferencias no resultaron estadísticamente significativas
(91.9 ± 22.4 vs 54.3 ± 11.7 paquetes/año; p = 0.28).
Los dosajes de α1-antitripsina mostraron que todos
los pacientes estuvieron dentro de la normalidad.
Como antecedentes de relevancia, se observó que
todos los pacientes eosinofílicos refirieron rinitis,
mientras que en los pacientes no eosinofílicos, sólo
dos de ellos (100.0% vs 22.2% respectivamente).
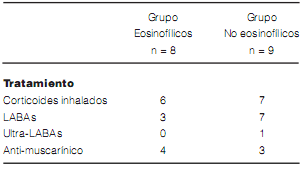
El tratamiento de mantenimiento para los pacientes incluyó corticoides inhalados (flutocasona
o budesonide), broncodilatadores de rápida acción
(SABAs y SAMAs), LABAS y broncodilatadores
de ultrarápida acción ultra-LABAs: indicaterol)
y antimuscarínicos (tiotrapio y glicopirronio).
Ambos grupos recibieron similares tratamientos
dada la severidad de su enfermedad (Tabla 2). Dos
pacientes del grupo eosinofílico, además, recibieron
tratamiento con corticoides orales (meprednisona)
y otros dos corticoides intranasales (furoato de
mometasona).
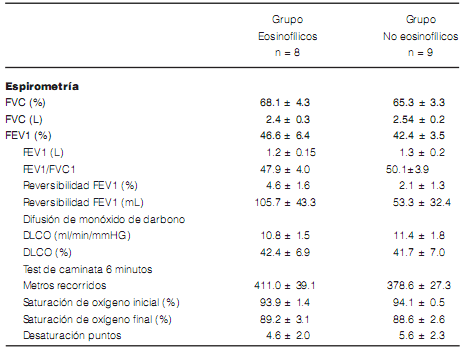
No se encontraron diferencias estadísticamente significativas en los parámetros de función pulmonar de ambos grupos de pacientes (eosinofílicos vs no eosinofílicos), aunque se observó un ligero incremento de la reversibilidad en el grupo de pacientes eosinofílicos (Tabla 3). Tampoco se observaron diferencias en la difusión (DLCO), ni en los metros recorridos en el test de marcha de 6 minutos. Sin embargo, la evaluación de los datos recogidos del test de impacto del CAT que mide el bienestar y calidad de vida desarrollado específicamente para pacientes con EPOC (COPD Assessment Test: CAT), mostró que los pacientes no eosinofílicos tienen peor calidad de vida respecto de los pacientes eosinofílicos (17.7 ± 3.8 vs 10.3 ± 0.66).
Mediadores inflamatorios: comparación de ambos
grupos
Se observó que tanto los pacientes eosinofilicos
como los no eosinofílicos presentaron más del 2%
de eosinófilos en sangre periférica. Sin embargo,
los valores fueron mayores en las muestras de
los pacientes con eosinofilia en esputo comparados con los pacientes no eosinofílicos (635.4± 111.1 eos/mm3 que equivalen a 5.8 ± 1.3% vs 435.0 ± 35.5 eos/mm3 correspondientes a 4.0 ± 0.7%). Según el test de Mann Whitney, estas diferencias no resultaron estadísticamente significativas (p = 0.07). También se observó que la
cantidad de eosinófilos en esputo se correlacionó positivamente con la cantidad de eosinófilos en
sangre (r de spearman = 0.52; p = 0.1).
Los pacientes eosinofílicos mostraron un ligero
incremento en los niveles de FeNO respecto de los
pacientes no eosinofílicos (43.5 ± 25.5 vs 21.3± 1.2 ppb; p = 0.7).
Discusión
La EPOC es una enfermedad que puede presentar
diferentes fenotipos. Esta heterogeneidad se pone
en evidencia con las diferentes respuestas a los
tratamientos farmacológicos26. Si bien numerosos
trabajos se han centrado en definir estos fenotipos,
no existe un consenso validado que los agrupe y
clasifique, sin embargo se identifican entre ellos la
bronquitis, el enfisema, los exacerbadores frecuentes, la sobreposición asma-EPOC y la EPOC con
bronquiectasias27, 28. Comprender las distintas presentaciones clínicas asociadas al perfil inflamatorio
particular de cada paciente podría contribuir a determinar estrategias personalizadas de tratamiento.
Recientemente las guías emitidas en conjunto
por la iniciativa global del manejo de la enfermedad
obstructiva crónica (Global Initiative for Chronic
Obstructive Lung Disease: GOLD) y la iniciativa
global de asma (Global Initiative for Asthma:
GINA); han definido al fenotipo de sobreposición
asma-EPOC como ACOS29, 30. Este síndrome,
caracterizado por una limitación persistente del flujo aéreo, tendría una prevalencia del 2% en la
población general y del 20% en los pacientes con
EPOC31, 32.
Conocer los criterios para el diagnóstico de ACOS
es fundamental ya que estos pacientes presentan
mayor número de exacerbaciones y en ocasiones
más severas que los pacientes con EPOC33. Los
pacientes con ACOS corresponden a un subgrupo
de pacientes con EPOC que requieren tratamiento
con corticoides inhalados asociados a broncodilatores β-2 de larga duración (LABA)34. ACOS incluye
pacientes con EPOC que poseen reversibilidad
parcial del flujo aéreo, con o sin antecedentes de
rinitis o alergias, reducida DLCO y/o eosinofilia en
el esputo o bien pacientes con asma que presenten
obstrucción parcialmente reversible de la vía aérea,
con o sin enfisema o DLCO <80%35, 36.
El nuevo algoritmo para el diagnóstico de ACOS
incluye criterios mayores y menores. Dentro de
los criterios mayores, se encuentran una reversibilidad al broncodilatador mayor a 400 ml o al
15% del VEF1, historia de asma o eosinofilia en el
esputo; y dentro de los menores se encuentra una
reversibilidad al broncodilatador de más de 200 ml
o al 12% del VEF1 en al menos dos ocaciones, IgE
elevada o historia de atopía37. Por consenso, los
pacientes deben presentar dos criterios mayores o
uno mayor y dos menores para ser diagnosticados
como ACOS.
Los pacientes con ACOS presentan mayor
morbi-mortalidad que los pacientes con asma o
EPOC solo, incluso en poblaciones jóvenes38-40. La
relevancia de su adecuado diagnóstico se basa en
el hecho de que presentan una notable estabilidad
o mejoría cuando reciben corticoides inhalados. La
eosinofilia en esputo con un valor de corte mayor a
2.5% predice la respuesta a corticoides inhalados con una sensibilidad de 82.4% y especificidad de
84.8%41. Más aún, se ha sugerido que la presencia
de eosinófilos en esputo inducido podría ser un
potencial predictor para el éxito del tratamiento42.
Si bien el tratamiento con corticoides inhalados
ha demostrado beneficios en los pacientes con
EPOC que presentan inflamación eosinofílica
disminuyendo las exacerbaciones y mejorando su
calidad de vida, en la práctica clínica habitual su
utilización de acuerdo a la severidad del paciente
puede resultar inapropiada. A pesar de que el número de pacientes reclutados hasta el momento es
bajo, se encontró mayor estabilidad y mejoría de la
calidad de vida (reflejada por el CAT) en el grupo
de pacientes eosinofilicos que se encuentran con
terapia de mantenimiento que incluye corticoides
inhalados.
Actualmente, aquellos pacientes con EPOC
con más de dos exacerbaciones por año tienen
indicación de recibir tratamiento con corticoides
inhalados, aunque la dosis a utilizar no está claramente definida. Sin embargo, debe considerarse
que la sobre-utilización de corticoides inhalados
podría tener más riesgos que beneficios a largo
plazo y generar además un innecesario incremento en los costos del sistema de salud. La necesidad de encontrar bio-marcadores que faciliten la
identificación de estos pacientes continúa siendo
un desafío. Si bien los hallazgos de este trabajo
constituyen resultados preliminares de un estudio descriptivo que intenta comprender el rol de
los eosinófilos para diferenciar los pacientes con
EPOC, nosotros hipotetizamos que la eosinofilia
en esputo podría ser una herramienta a utilizar
como criterio para la indicación de corticoides
inhalados. Cada paciente debe ser evaluado en
forma individual para optimizar su tratamiento.
Conflictos de interés: Los autores declaran que no tienen conflictos de intereses relacionados con el tema de esta publicación.
Bibliografía
1. Global Initiative for Chronic Obstructive Lung Disease. [homepage on the Internet] Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. En: http://www.goldcopd.org/uploads/users/files/GOLD_Report_2014_Jun11.pdf.
2. Rutten-van Molken MP, Oostenbrink JB, Tashkin DP et al. Does quality of life of COPD patients as measured by the generic EuroQol five-dimension questionnaire differentiate between COPD severity stages? Chest 2006; 130(4): 1117-1128.
3. European Respiratory Society/European Lung Foundation. Chronic Obstructive Pulmonary Disease. European Lung Foundation. European Lung White Book. Laussane: European Respiratory Society; 2003, pp.34-43.
4. Masa JF, Sobradillo V, Villasante C et al. Costes de la EPOC en España. Estimación a partir de un estudio epiemiológico poblacional. Arch Bronconeumol 2004; 40: 72-79.
5. Gould NS, Min E, Gauthier S, Chu HW, Martin R, Day BJ. Aging Adversely Affects the Cigarette Smoke-induced Glutathione Adaptive Response in the Lung. Am J Respir Crit Care Med 2010; 182(9): 1114-22.
6. Barrecheguren M, Esquinas C, Miravitlles M. The asthma COPD overlap syndrome (ACOS). Opportunities and challenges. Curr Opin Pulm Med 2015; 21: 74-79.
7. Soler-Cataluña JJ, Cosío B, Izquierdo JL et al. Consensus document on the overlap phenotype COPD-asthma in COPD. Arch Bronconeumol 2012; 48(9): 331-7.
8. Weiss ST. What genes tell us about the pathogenesis of asthma and chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2010; 181(11): 1170-1173.
9. Matkovic Z, Tudoric N, Miravitlles M. Impact of chronic bronchial infection in the lung and beyond. Eur Respir Mon 2013; 60: 46-57.
10. Hnizdo E, Sullivan PA, Bang KM, Wagner G. Association between chronic obstructive pulmonary disease and employment by industry and occupation in the US population: a study of data from the Third National Health and Nutrition Examination Survey. Am J Epidemiol 2002; 156(8): 738-746.
11. Torres-Duque C, Maldonado D, Pérez-Padilla R, Ezzati M, Viegi G. Biomass Fuels and Respiratory Diseases. Proc Am Thorac Soc 2008; 5(5): 577-90.
12. Global Initiative for Chronic Obstructive Lung Disease. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. 2007. En: http://www.goldcopd.org/Guidelines/guidelines-globalstrategy-for-diagnosis-management-2007.html, 2014.
13. Kersul AL, Iglesias A, Rios A et al. Molecular mechanisms of inflammation during exacerbations of chronic obstructive pulmonary disease. Arch Bronconeumol 2011; 47: 176-83.
14. Dal Negro RW, Bonadiman L, Turco P. Prevalence of different comorbidities in COPD patients by gender and GOLD stage. Multidiscip Respir Med 2015 5; 10(1): 24.
15. Lopez-Campos JL, Agustí A. Heterogeneity of chronic obstructive pulmonary disease exacerbations: a two-axes classification proposal. Lancet Respir Med 2015; S2213-2600(15)00242-8.
16. Magnussen H, Disse B, Rodriguez-Roisin R et al. Withdrawal of inhaled glucocorticoids and exacerbations of COPD. N Engl J Med 2014; 371: 1285-94.
17. Liesker JJW, Bathoorn E, Postma DS, Vonk JM, Timens W, Kerstjens HAM. Sputum inflammation predicts exacerbations after cessation of inhaled corticosteroids in COPD. Respir Med 2011; 105(12): 1853-1860.
18. Pascoe S, Locantore N, Dransfield MT, Barnes NC, Pavord ID. Blood eosinophil counts, exacerbations, and response to the addition of inhaled fluticasone furoate to vilanterol in patients with chronic obstructive pulmonary disease: a secondary analysis of data from two parallel randomised controlled trials. Lancet Respir Med 2015; 3(6): 435-442.
19. Siva R, Green RH, Brightling CE et al. Eosinophilic airway inflammation and exacerbations of COPD: a randomised controlled trial. Eur Respir J 2007; 29(5): 906-913.
20. Antus B, Barta I, Horvath I, Csiszer E. Relationship between exhaled nitric oxide and treatment response in COPD patients with exacerbations. Respirology 2010; 15(3): 472-477.
21. Soter S, Barta I, Antus B. Predicting Sputum Eosinophilia in Exacerbations of COPD Using Exhaled Nitric Oxide. Inflammation 2013; 36(5): 1178-1185.
22. Louie S, Zeki AA, Schivo M et al. The asthma-chronic obstructive pulmonary disease overlap syndrome: pharmacotherapeutic considerations. Expert Rev Clin Pharmacol 2013; 6(2): 197-219.
23. Bjermer L, Alving K, Diamant Z et al. Current evidence and future research needs for FeNO measurement in respiratory diseases. Respir Med 2014; 108(6): 830-841.
24. Dweik RA, Boggs PB, Erzurum SC et al. An official ATS clinical practice guideline: interpretation of exhaled nitric oxide levels (FENO) for clinical applications. Am J Respir Crit Care Med 2011; 184(5): 602-615.
25. Hargreave FE, Pizzichini E. Pizzichini M. Induced sputum examination. J Allergy Clin Immunol 1998; 101(4): 569-70.
26. European Respiratory Task Force Standardised methodology of sputum induction and processing. Eur Respir J 2002; 20(37): 1s-55s.
27. Miller MR, Hankinson J, Brusasco V et al. Standardisation of spirometry. Eur Respir J 2005; 26: 319-338.
28. Macintyre N, Crapo RO, Viegi G et al. Standardisation of the single-breath determination of carbon monoxide uptake in the lung. Eur Respir J 2005; 26: 720-735.
29. Veras TN, Pizzichini E, Steidle LJ et al. Cellular composition of induced sputum in healthy adults. J Bras Pneumol 2011; 37(3): 348-53.
30. Singh D, Fox SM, Tal-Singer R et al. Altered gene expression in blood and sputum in COPD frequent exacerbators in the ECLIPSE cohort. PLoS One 2014; 9(9): e107381.
31. Miravitlles M, Soler-Cataluña JJ, Calle M, Soriano JB. Treatment of COPD by clinical phenotypes: putting old evidence into clinical practice. Eur Respir J 2013 6-1; 41(6): 1252-6.
32. Blasi F, Chalmers JD, Aliberti S. COPD and Bronchiectasis: Phenotype, Endotype or Co-morbidity? COPD: Journal of Chronic Obstructive Pulmonary Disease 2014; 11(6): 603-604.
33. Allen-Ramey FC, Gupta S, DiBonaventura MD. Patient characteristics, treatment patterns, and health outcomes among COPD phenotypes. Int J Chron Obstruct Pulmon Dis 2012; 7: 779-87.
34. Miravitlles M, Soler-Cataluña JJ, Calle M et al. Spanish Guideline for COPD (GesEPOC). Update 2014. Arch Bronhoneumol 2014; 50(1): 1-16.
35. GINA. Global Strategy for Asthma Management and Prevention. Vancouver USA: Global Initiative for Asthma 2014; 1-134.
36. Gibson PG, McDonald VM. Asthma-COPD overlap 2015: now we are six. Thorax 2015; 70 (7): 683-691.
37. Pleasants RA, Ohar JA, Croft JB et al. Chronic obstructive pulmonary disease and asthma-patient characteristics and health impairment. COPD 2014; 11(3): 256-266.
38. de Marco R, Pesce G, Marcon A et al. The coexistence of asthma and chronic obstructive pulmonary disease (COPD): prevalence and risk factors in young, middle-aged and elderly people from the general population. PLoS ONE 2013; 8: e62985.
39. Gibson PG, Simpson JL. The overlap syndrome of asthma and COPD: what are its features and how important is it? Thorax 2009; 64: 728-735.
40. Akamatsu K, Matsunaga K, Sugiura H et al. Improvement of Airflow Limitation by Fluticasone Propionate/Salmeterol in Chronic Obstructive Pulmonary Disease: What is the Specific Marker? Front Pharmacol 2011; 2(36): 1-6.
41. Hardin M, Silverman EK, Barr RG et al. The clinical features of the overlap between COPD and asthma. Respir Res 2011; 12: 127.
42. Bujarski S, Parulekar AD, Sharafkhaneh A, Hanania NA. The asthma COPD overlap syndrome (ACOS). Curr Allergy Asthma Rep 2015; 15(3): 509.
43. Barrecheguren M, Esquinas C, Miravitlles M. The asthmachronic obstructive pulmonary disease overlap syndrome (ACOS): opportunities and challenges. Curr Opin Pulm Med 2015; 21(1): 74-9.
44. Yamauchi Y, Yasunaga H, Matsui H. Comparison of inhospital mortality in patients with COPD, asthma and asthma-COPD overlap exacerbations. Respirology 2015; 20(6): 940-946.
45. Kim MA, Noh CS, Chang YJ et al. Asthma and COPD overlap syndrome is associated with increased risk of hospitalisation. Int J Tuberc Lung Dis 2015; 19(7): 864-869.
46. Kitaguchi Y, Komatsu Y, Fujimoto K, Hanaoka M, Kubo K. Sputum eosinophilia can predict responsiveness to inhaled corticosteroid treatment in patients with overlap syndrome of COPD and asthma. Int J Chron Obstruct Pulmon Dis 2012; 7: 283-289.
47. de Marco R, Marcon A, Rossi A. Asthma, COPD and overlap syndrome: a longitudinal study in young European adults. Eur Respir J 2015; 46(3): 671-679.