Autor : Dres. Eduardo Borsini, MartĂn Bosio, Silvia Quadrelli, JerĂłnimo Campos, Tamara DĂ©cima, Julio Chertcoff
Servicio de NeumonologĂa - Hospital Británico de Buenos Aires
Correspondencia : Eduardo Borsini Domicilio Postal: Av. Caseros 1671 - 7° G CP 1152 - CABA Tel. 011-43055552 Móvil 011-1550374566 Email: borsinieduardo@yahoo.com.ar
Resumen
La poligrafĂa respiratoria realizada en el domicilio es un mĂ©todo Ăştil para el diagnĂłstico del sĂndrome de apneas del sueño cuando se indica en individuos con alto riesgo y cumple un mĂnimo de requerimientos tĂ©cnicos de calidad. Cuando se interpreta junto a una evaluaciĂłn integral del sueño permite acortar las listas de espera, reservar los estudios de mayor complejidad para casos difĂciles o dudosos y acercar el laboratorio de sueño al domicilio, lo que permite la valoraciĂłn respiratoria del sueño en un ámbito más natural con condiciones similares a las habituales del paciente cuando se dispone a dormir.
Los avances tecnológicos han significado una notable disminución del tamaño, peso y costo de los equipos registradores que pueden ser usados en la cama del paciente y conectarse con equipos de tratamiento (CPAP o dispositivos de ventilación).
Asimismo, han supuesto mayor acceso al diagnóstico en pequeñas unidades menos dotadas de recursos técnicos, lo que ha ampliado el horizonte diagnóstico del médico neumonólogo.
La polisomnografĂa sigue siendo muy importante para definir con certeza los casos dudosos y continĂşa siendo el mĂ©todo patrĂłn que debe ser tomado para valorar los avances de los nuevos y más accesibles mĂ©todos de estudio de las enfermedades respiratorias durante el sueño.
Palabras clave: PoligrafĂa respiratoria; DiagnĂłstico domiciliario; Apneas del sueño
Abstract
Respiratory polygraphy in the diagnosis of sleep respiratory disorders. A necessary tool for the pulmonologist
The respiratory polygraphy (RP) is a useful method for the diagnosis of sleep apnea when it is indicated in high risk patients and meets basic technical requirements for quality. When RP is interpreted in conjunction with a comprehensive evaluation of sleep, it shortens waiting lists approaching the sleep laboratory to the home, and allows the assessment of respiratory performance during sleep in a more natural environment under usual conditions similar to those when the patient is ready to sleep.
Technological developments have brought a considerable reduction in size and weight and in the costs of the recording devices, which can be used bedside and connected to therapeutics devices (CPAP or non invasive ventilator).
Also, they have increased the accessibility to diagnostic process of small units with limited technical resources expanding the diagnostic horizon of the pulmonologist.
The polygraphy or polysomnography is still very important to define with certainty doubtful cases and it is the standard method which should be taken to assess the progress of new accessible methods for the study of these diseases.
Key words: Respiratory polygraphy; Home testing; Sleep apnea
IntroducciĂłn
Si bien todavĂa existen controversias y la informaciĂłn disponible es aĂşn incompleta en algunos aspectos, indudablemente los trastornos respiratorios durante el sueño representan un grupo de entidades que afectan la calidad de vida, acortan la expectativa de vida y aumentan los costos de salud.
Desde hace más de una dĂ©cada se ha documentado que no diagnosticar y por consiguiente no tratar a los pacientes con sĂndrome de apneas e hipopneas obstructivas durante el sueño (SAHOS) significa un incremento en los costos en salud a mediano y largo plazo1, 2. De esta manera, los pacientes con SAHOS moderado y severo sin tratamiento consumen dos a tres veces más recursos de salud en comparaciĂłn a los controles en los 10 años previos al diagnĂłstico3.
Comunicaciones epidemiolĂłgicas han estimado que 9% de la poblaciĂłn tiene anormalidades respiratorias durante el sueño4, 5 definidas por un Ăndice de apneas e hipopneas por hora de sueño (IAH) mayor a 5 por hora y que en aproximadamente el 5% de los adultos varones y 3% de las mujeres se asocia a sĂntomas diurnos de excesiva somnolencia6, trastornos neuro-cognitivos, mnĂ©sicos, cardiovasculares, metabĂłlicos o inflamatorios que definen el SAHOS7 y por ende son pasibles de recibir tratamiento.
Este valor de prevalencia se asemeja al de otras enfermedades frecuentes como por ejemplo, la diabetes, pero a diferencia de esta que puede definirse por exámenes sanguĂneos, el SAHOS requiere estudios de mayor complejidad para certificar el diagnĂłstico y planificar las estrategias terapĂ©uticas.
Existen modelos de cuestionarios para determinar la probabilidad de SAHOS combinando sĂntomas y parámetros antropomĂ©tricos, y si bien son de bajo costo y han mostrado una alta sensibilidad (46%-90%), tienen una baja (13% al 54%) y variable especificidad8.
En este sentido, algunos autores han propuesto la valoraciĂłn mediante la utilizaciĂłn de parámetros clĂnicos9-11 funcionales12 o antropomĂ©tricos13, con el fin de identificar la probabilidad del paciente de padecer SAHOS de relevancia o intentar calcular su IAH. Dentro de este abanico de opciones, las estrategias más estudiadas han sido sin duda los parámetros clĂnicos. Varios estudios han valorado su papel como herramienta diagnĂłstica con la construcciĂłn de ecuaciones de predicciĂłn mediante mĂ©todos multivariados. La combinaciĂłn de variables posibles y la heterogeneidad de las poblaciones en las que se han aplicado dificultan comparaciones y extrapolaciones. Además no han sido evaluados para poblaciones tales como ancianos, niños y algunos grupos Ă©tnicos, por lo que no son recomendados para el diagnĂłstico de certeza y solo deben ser tenidos en cuenta como una aproximaciĂłn.
Es por ello que el diagnĂłstico de certeza del SAHOS requiere la realizaciĂłn de un test que permita evaluar los sucesos respiratorios que ocurren en el paciente durante el sueño. Tradicionalmente la confirmaciĂłn del diagnĂłstico requiere una polisomnografĂa completa (PSG) y esta ha sido durante más de 20 años la estrategia convencional.
Al tratarse de un trastorno tan prevalente y con la mayor difusiĂłn de los conocimientos sobre la patologĂa respiratoria durante el sueño, las listas de espera han ido creciendo de manera progresiva y han alargado la demora entre la decisiĂłn de realizar una prueba de sueño, su concreciĂłn, y el inicio del tratamiento. En este sentido, el auge de la medicina del sueño ha significado un mayor desarrollo de las unidades de diagnĂłstico con la consiguiente centralizaciĂłn que acompañó inicialmente este crecimiento en todo el mundo.
En 1992 en Edimburgo, una experiencia piloto revolucionó el proceso diagnóstico de los trastornos respiratorios del sueño al demostrar que carecer de señales electrofisiológicas no cambiaba la eficacia de expertos en PSG para diagnosticar SAHOS14.
En los Ăşltimos años se han desarrollado mĂşltiples mĂ©todos de diagnĂłstico abreviados o simplificados de menor costo y complejidad que permiten realizar estudios no vigilados y ambulatorios. Es de esta forma, cĂłmo progresivamente, la metodologĂa operativa denominada poligrafĂa respiratoria (PR) ha sido aceptada por las sociedades cientĂficas en la materia alrededor del mundo.
La poligrafĂa respiratoria
Los equipos de PR son dispositivos registradores de señales respiratorias que no disponen de mediciones neurofisiológicas y han sido validados para obtener grabaciones ambulatorias del desempeño respiratorio durante la noche. Han sido aceptados actualmente como equivalentes a la PSG para el diagnóstico de SAHOS y con estos se calcula que pueden manejarse en manos expertas dos tercios de los pacientes15.
Una revisiĂłn conjunta de la American Academy of Sleep Medicine junto a la American Thoracic Society y la American College of Chest Physicians publicada en octubre del 2003, concluyĂł que los dispositivos portátiles que disponen de registro de flujo mediante una cánula, movimientos respiratorios (esfuerzo) y oximetrĂa de pulso denominados equipos de nivel III, pueden ser aceptados cuando se usan de manera controlada en el contexto de una evaluaciĂłn integral de la patologĂa del sueño y cuando la interpretaciĂłn de los datos extraĂdos de los registros son evaluados por personal con experiencia y entrenamiento16.
En 2005 el consenso Español exponĂa: "Por el momento, y teniendo en cuenta la evidencia cientĂfica disponible, la utilizaciĂłn de la PR en domicilio no ha sido suficientemente validada. Por ello, este documento recomienda su empleo en modo vigilado hasta que se disponga de estudios de validaciĂłn que permitan su uso generalizado. Sin embargo, todos los estudios llevados a cabo hasta ahora sugieren que sus resultados serán similares a la PR vigilada y que los estudios domiciliarios formarán parte fundamental del diagnĂłstico del SAHOS. Hasta entonces su empleo deberá ser individualizado por cada unidad de sueño"7. Es de hacer notar que en los Ăşltimos 10 años, se ha incrementado la experiencia debido a la amplia utilizaciĂłn de estos dispositivos e inclusive se han creado redes de complejidad creciente con un hospital coordinador central de referencia con unidad de sueño y capacidad para realizar PSG completa y varios centros perifĂ©ricos satĂ©lites que solo disponen de PR capaces de llevar la exploraciĂłn respiratoria del sueño al domicilio del paciente.
Una innegable ventaja de esta metodologĂa ha sido posibilitar el acceso de centros de menor complejidad, alejados de los grandes hospitales y ha puesto en la escena a especialistas de ciudades alejadas o pequeños centros urbanos donde no se dispone o no se justifica el montaje de la planta fĂsica necesaria para realizar la PSG, quienes han encontrado en la PR acceso rápido a la metodologĂa diagnĂłstica y protagonismo en el tratamiento y monitoreo de los trastornos respiratorios durante el sueño.
La American Academy of Sleep Medicine en el año 2007 confeccionĂł una nueva guĂa para el uso de la PR y sugiriĂł su utilidad para aquellos pacientes con movilidad reducida para acceder a la PSG. Asimismo planteĂł su uso como alternativa al mĂ©todo convencional, siempre y cuando su aplicaciĂłn se implementara por personal experto en el ámbito de una evaluaciĂłn comprensiva de la patologĂa del sueño. Además estableciĂł pautas acerca de las limitaciones de los estudios abreviados en pacientes cuyas condiciones comĂłrbidas pudieran dificultar la interpretaciĂłn de los resultados17.
En 2008, el Center for Medicare and Medicaid Services (CMS), basado en dos reportes solicitados a la Agency for Healthcare Research and Quality (AHRQ) que evaluaron la evidencia disponible sobre confiabilidad y eficacia diagnĂłstica de los dispositivos portátiles de nivel III (cánula de flujo, oxĂmetro y sensor de esfuerzo torácico)18 tomĂł la decisiĂłn polĂtica de aceptar los mĂ©todos abreviados como opciĂłn a la PSG para el diagnĂłstico de SAHOS. De manera similar, la entidad regulatoria de Inglaterra, el National Institute for Health Clinical Excellence (NICE) cuyas recomendaciones son decisiones gubernamentales de cumplimiento obligatorio, en marzo del 2008 reconociĂł la utilidad diagnĂłstica de la PR siempre que se utilice en unidades de sueño por personal experimentado.
En Argentina, en el año 2001 el primer consenso de trastornos respiratorios vinculados al sueño (19) de la AsociaciĂłn Argentina de Medicina Respiratoria (AAMR) considerĂł a la PR como opciĂłn diagnĂłstica en casos de inaccesibilidad a la PSG o inaceptable lista de espera. En octubre del 2009, la secciĂłn de sueño oxigenoterapia y otros tratamientos crĂłnicos domiciliarios de la AAMR actualizĂł el documento en el que expone que los dispositivos portátiles de PR (nivel III) "pueden ser usados en el domicilio del paciente". En este momento, una actualizaciĂłn y revisiĂłn de las indicaciones y la utilidad de los estudios abreviados (nivel III) en formato de documento de consenso (AAMR) se encuentra en proceso de publicaciĂłn, esta reconoce que la PR es "comparable" a la PSG para el diagnĂłstico de SAHOS en pacientes con adecuada sospecha clĂnica. Es posible que la tecnologĂa usada para el diagnĂłstico tenga menos importancia que el nivel de experiencia y el entrenamiento de quienes interpretan los resultados. En nuestro medio varios grupos realizan PR domiciliarias como parte integral del trabajo de los servicios de medicina respiratoria o de las unidades de medicina del sueño, aunque no existe por el momento un sistema de acreditaciones o de control de la calidad de los estudios de PR.
Un registro de PR de buena calidad acompañado de una juiciosa valoraciĂłn clĂnica permiten hacer diagnĂłstico de SAHOS en dos tercios de los pacientes sin necesidad de ocupar un turno de la unidad de sueño, que puede asĂ reservar la PSG para los casos problemáticos o dudosos.
La desventaja más importante de la PR es que no permite evaluar el sueño. En consecuencia no se conoce su calidad ni cantidad, de manera que el número de eventos respiratorios no puede dividirse por el número de horas de sueño, sino por el tiempo de registro, lo que infra-estima la severidad del trastorno7.
Adelantos en los registradores mediante la incorporaciĂłn de canales accesorios permiten inferir perĂodos de sueño y actividad mediante acelerĂłmetros y sensores de movimiento (actimetrĂa y actigrafĂa). Además, el desarrollo en los software de lectura permite eliminar perĂodos de actividad y de este modo modifica el tiempo total de registro válido para el análisis, minimizando la subestimaciĂłn en el IAH.
Otro aspecto que debe ser tenido en cuenta es la modalidad de instalaciĂłn de los dispositivos, ya que los equipos portátiles pueden ser instalados en el hospital por personal tĂ©cnico y asĂ el paciente se lo lleva puesto a su domicilio para regresarlo al dĂa siguiente, o bien puede ser el paciente quien se lleva el equipo y lo instala por sĂ mismo antes de dormir siguiendo un procedimiento pautado previamente. Finalmente, otra forma de uso consiste en que un tĂ©cnico se desplace al domicilio del paciente e instale el equipo. La estrategia elegida dependerá del entorno donde la PR se implemente (grandes ciudades, pequeños centros urbanos, unidades de sueño, servicios de medicina respiratoria, centro hospitalario o domicilio del paciente). Adicionalmente, la portabilidad de los sistemas de PR hace posible la toma de registros durante la internaciĂłn en aquellos pacientes en los que el traslado se torna riesgoso o complejo, como es el caso de los internados en la terapia intensiva o en la unidad coronaria.
En resumen, la PR ha permitido descentralizar el diagnóstico de las unidades de referencia y ha facilitado el acceso diagnóstico a centros más pequeños que utilizan los dispositivos portátiles y que trabajan coordinadamente con aquellas.
El futuro del diagnóstico de los trastornos respiratorios durante el sueño evoluciona hacia la búsqueda de sistemas extraordinariamente sencillos en su aplicación, que puedan emplearse en el domicilio por personal no experto, aunque los equipos en su estructura interna sean de gran complejidad.
PolisomnografĂa convencional y poligrafĂa respiratoria
Diferencias y parecidos
Tradicionalmente el diagnĂłstico de certeza del sĂndrome de apneas de sueño (SAHOS) requiere la realizaciĂłn de un estudio polisomnográfico completo y supervisado, realizado en horario nocturno (o en el habitual de sueño del paciente) en un centro dotado de personal e infraestructura necesarios. Incluye una serie de variables respiratorias y neurofisiolĂłgicas: electroencefalograma (nĂşmero variable de canales segĂşn el montaje), electrooculograma, electromiograma submentoniano, electrocardiograma, flujo aĂ©reo nasobucal por termistancia y presiĂłn nasal, esfuerzo respiratorio por bandas torácica y abdominal, saturaciĂłn de oxĂgeno y posiciĂłn corporal. Es recomendable además el uso de micrĂłfono para la determinaciĂłn de los ronquidos y el registro de electromiografĂa del mĂşsculo tibial anterior. Con este montaje es posible la monitorizaciĂłn de la cantidad y calidad del sueño asĂ como su relaciĂłn con los diferentes eventos respiratorios y los fenĂłmenos asociados. En la actualidad, la PSG es considerada como el patrĂłn de referencia para el diagnĂłstico del SAHOS. Sin embargo no ha estado exenta de crĂticas ni libre de dificultades ya que no es capaz de dar respuesta a todas las preguntas en el universo de pacientes con trastornos del sueño20. De hecho, no es lo mismo estudiar un paciente con alta sospecha clĂnica de SAHOS, sin otros hallazgos, que un paciente con sĂntomas de solapamiento con otros trastornos del sueño, co-morbilidad asociada, etc. Por ello, la aproximaciĂłn más juiciosa al diagnĂłstico del SAHOS depende de quĂ© queremos medir y en quĂ© tipo de paciente deseamos hacerlo. Por otra parte, la disponibilidad (escasa en muchas regiones de nuestro paĂs), las listas de espera, los costos, la necesidad de trasladar a los pacientes al centro de diagnĂłstico (cuando la lĂłgica indica que deberĂa ser al revĂ©s) y otros factores como la complejidad tĂ©cnica de la PSG asĂ como su ocasionalmente difĂcil interpretaciĂłn hacen de esta tĂ©cnica un gold standard complejo.
El informe de la PSG incluye la confecciĂłn de una representaciĂłn en el tiempo de los diferentes estadĂos de sueño llamado hipnograma (exclusivo de la PSG) y la descripciĂłn de las diferentes variables fisiolĂłgicas de la respiraciĂłn y oxigenaciĂłn, asĂ como la cuantificaciĂłn de los eventos respiratorios durante el sueño que se expresan con diferentes Ăndices. Algunos de los más importantes son el Ăndice de apneas e hipopneas (IAH) que resulta de dividir todos los eventos de apnea o las disminuciones de flujo asociadas a alguna evidencia de daño (microdespertar o desaturaciĂłn) denominadas hipopneas sobre el total de las horas de sueño. El Ăndice de disturbios respiratorios (IDR) resulta de la suma de las anteriores anormalidades (apneas + hipopneas) y de los microdespertares que fueron provocados por incremento del esfuerzo respiratorio (incremento de la resistencia de la vĂa aĂ©rea). El nĂşmero de horas de sueño es extraĂdo de la señal electroencefalográfica, es decir, los perĂodos de vigilia durante la noche del estudio no se contabilizan y no modifican los Ăndices finales.
Dada la prevalencia del SAHOS no está justificada su realizaciĂłn en toda la poblaciĂłn en riesgo, por eso se acepta que el diagnĂłstico pueda ser realizado bajo ciertas condiciones mediante poligrafĂa respiratoria (PR).
Estos sistemas denominados "abreviados" o "simplificados" (aunque en rigor de verdad las decisiones basadas en estudios con menos canales no son necesariamente simples) prescinden de los datos neurofisiolĂłgicos y pueden ser Ăştiles para descartar casos de baja probabilidad de SAHOS o para confirmar casos de alta sospecha. Es decir, son Ăştiles para confirmar el diagnĂłstico en pacientes de alto riesgo o descartarlo en individuos sin sĂntomas7, 17.
En ocasiones los hallazgos discordantes entre la PR, la clĂnica o la probabilidad previa al test deberán confirmarse con polisomnografĂa convencional y se ha reportado que esta discordancia sucede hasta en el 20% del los casos7, 17, 21.
La PR comprende el registro de al menos tres variables; flujo aĂ©reo o presiĂłn nasobucal, esfuerzo/ movimientos respiratorios y saturaciĂłn de oxĂgeno. A menor el nĂşmero de sensores el montaje es más sencillo (Figura 1 y 2).

Existen en el mercado un gran nĂşmero de dispositivos de PR validados (en general han sido comparados contra PSG) cuyo nĂşmero de señales varĂan desde las tres básicas a más de 12 opcionales como ser: posiciĂłn, marcador de eventos para ser accionado por el paciente, termistor acoplado a la cánula de presiĂłn nasobucal, banda abdominal, accesorios para comunicaciĂłn con los equipos de terapia (CPAP u otro dispositivo de ventilaciĂłn).
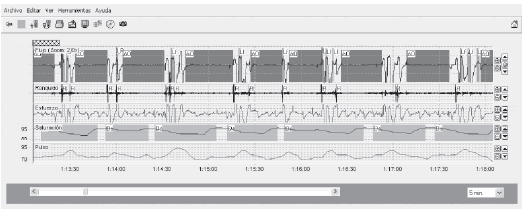
La mayorĂa de los sistemas de registro actualmente disponibles cuentan con un software que puede identificar automáticamente eventos de flujo y descensos de la saturaciĂłn. Este análisis responde a diferentes algoritmos internos del equipo aunque puede ser modificado segĂşn preferencias del usuario a fin de utilizar diferentes criterios de mayor o menor sensibilidad o especificidad. Si bien la lectura automática puede resultar de ayuda se recomienda que la interpretaciĂłn siempre sea manual con ediciĂłn de cada evento por un observador experimentado y entrenado en la metodologĂa de lectura. El conteo (scoring) manual de eventos respiratorios se hace en páginas diferentes a la de la PSG, habitualmente en escala de tiempo entre 2 a 5 minutos (Figura 3), por lo que un operador entrenado puede leer e informar una PR con relativa rapidez.
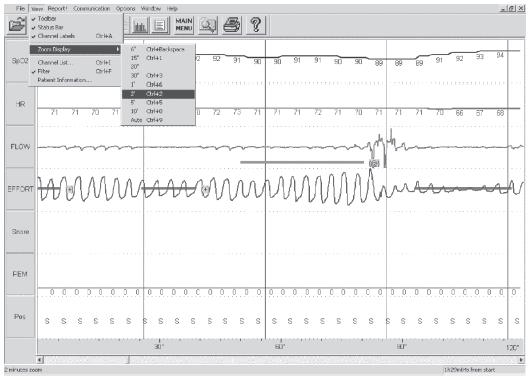
Si bien el SAHOS es la entidad que representa el 80% de las alteraciones respiratorias durante el sueño, no es la Ăşnica. El sĂndrome de obesidad e hipoventilaciĂłn, el sĂndrome de apneas de sueño centrales y la respiraciĂłn de Cheyne Stokes son patologĂas frecuentes de observar en la práctica clĂnica. La PR no ha sido validada aĂşn para el diagnĂłstico de estos trastornos, aunque su hallazgo debe ser consignado (Figuras 4 y 5).
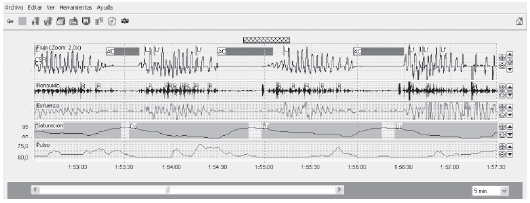
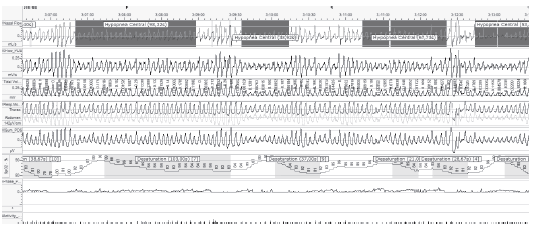
Es de hacer notar que progresivamente las restricciones sobre el uso de la PR en pacientes con condiciones comĂłrbidas han ido disminuyendo al incrementarse la experiencia con la tĂ©cnica que ha determinado un significativo aumento en la evidencia cientĂfica disponible22.
El desarrollo de tĂ©cnicas de exploraciĂłn no invasivas de la respiraciĂłn en los polĂgrafos respiratorios permite monitorear variables especĂficas en el domicilio del paciente durante una o varias noches, (volumen corriente, coordinaciĂłn de los movimientos durante los eventos de apnea o hipopneas) y otorgar informaciĂłn Ăştil para el estudio de las enfermedades neuromusculares o trastornos respiratorios del sueño de mecanismo no obstructivo (Figura 5).
La facilidad de poder conectar el dispositivo a los equipos de ventilaciĂłn (ventilaciĂłn mecánica no invasiva) ha significado un nuevo campo de aplicaciĂłn de estas tecnologĂas al pie de la cama del paciente en una o mĂşltiples noches (Figura 6 y 7) y está cambiando nuestro entendimiento de los fenĂłmenos que ocurren en los pacientes con asistencia ventilatoria aguda y crĂłnica23, 24.
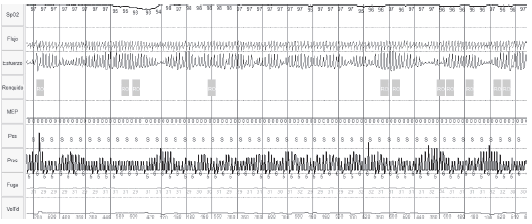
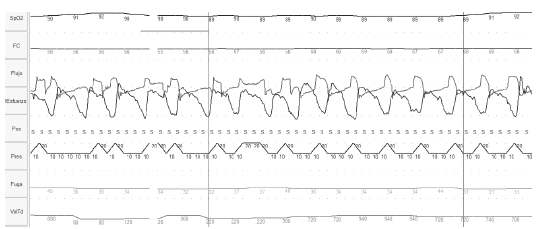
La PR es mĂ©todo de registro de variables "no vigilada" y existe por ello riesgo de desconexiones o perĂodos de registro con señales de mala calidad que dificulten su análisis (Figura 8). Es deseable un tiempo de registro de buena calidad válido para el análisis de al menos cuatro horas. Se ha reportado que aproximadamente el 10% de los estudios de PR no cuentan con criterios de calidad suficiente para ser utilizados por lo que deberán ser repetidos en una segunda noche o bien se deberá optar por realizar una PSG.
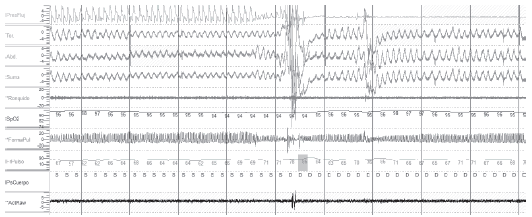
Otra limitaciĂłn de la PR es inherente a la ausencia de señales neurofisiolĂłgicas. Los Ăndices utilizados (IAH e Ăndice de desaturaciones) difieren con los de la PSG. El IAH resulta del cociente entre los eventos de flujo y el tiempo total de registro. En otras palabras, si el paciente no durmiĂł todas las horas del estudio la PR infra estimará la gravedad del trastorno. Es por ello que en individuos con factores que pueden motivar a confusiĂłn (insomnio) es mejor elegir la PSG y reservar los mĂ©todos abreviados para aquellos con alta sospecha de SAHOS, quienes frecuentemente presentan excesiva somnolencia diurna y facilidad para dormir.
Resumen
La PR es un mĂ©todo Ăştil para el diagnĂłstico de SAHOS cuando se indica en individuos de alto riesgo y cumple con un mĂnimo de requerimientos tĂ©cnicos de calidad. Cuando se interpreta junto a una evaluaciĂłn integral del sueño permite acortar las listas de espera, reservar los estudios de mayor complejidad para casos difĂciles o dudosos y acercar el laboratorio de sueño al domicilio, lo que posibilita la valoraciĂłn respiratoria del sueño en un ámbito más natural con condiciones similares a las habituales del paciente cuando se dispone a dormir.
El entrenamiento del personal que realiza estudios de PR y sobre todo el conocimiento de las limitaciones del mĂ©todo y un adecuado juicio clĂnico son condiciones que no pueden ser reemplazadas por las mejoras tecnolĂłgicas en los equipos. La polisomnografĂa sigue siendo muy importante para definir con certeza los casos dudosos y continĂşa siendo el patrĂłn de referencia que debe ser tomado para valorar los avances de los nuevos pero más accesibles mĂ©todos de estudio de los trastornos respiratorios del sueño, que han devenido en herramientas indispensables en el arsenal de los especialistas en medicina respiratoria.
1. Phillipson EA. Sleep apnea. A mayor public health problem. New Eng J Med 1993; 328: 1271-1273.
2. Kryger MH, Ross L, Delaive K, Walld R, Horrocks J. Utilization of health care services in patients with severe obstructive sleep apnea. Sleep 1996; 19: S111-S116.
3. Ronald J, Delaive K, Roos L, Manfreda J, Bahammam A, Kryger MH. Health care utilization in the 10 years prior to diagnosis in obstructive sleep apnea patients. Sleep 1999; 2: 225-229.
4. Young T, Palta M, Dempsey J, y cols. The occurrence of Sleep disorders breathing among middle aged adults. N Engl J Med 1993; 328: 1230-1236.
5. Durán J, Esnaola S, Ramón R, Iztueta A. Obstructive sleep apnea-hypopnea and related clinical features in a population-based sample of subjects aged 30 to 70 years. Am J Respir Crit Care Med 2001; 163: 685-689.
6. Young T, Peppard P, Gottlieb D. Epidemiology of obstructive sleep apnea. Am J Respir Crit Care Med 2002; 165: 1217-1239.
7. Grupo Español de Sueño. Documento consenso español sobre el sĂndrome de apneas-hipopneas del sueño. Arch Bronc.2005; Vol 41, Supl 4: 7.
8. Flemmons WW. Obstructive Sleep apnea. N Engl J Med 2002; 347: 498-501.
9. Hofftein V, Szalai JP. Predictive value of clinical features in diagnosing obstructive sleep apnea. Sleep 1993; 16:118-22.
10. Deegan PC, McNicholas WT. Predictive value of clinical features for the obstructive sleep apnoea syndrome. Eur Respir J 1998; 9: 117-24.
11. Rowley JA, Aboussouan LS, Badr MS. The use of clinical prediction formulas in the evaluation of obstructive sleep apnea. Sleep 2000; 23: 929-37.
12. Zerah-Lancner F, Lofaso F, D'Ortho MP, Delclaux C, Goldenberg F, Coste A, et al. Predictive value of pulmonary function parameters for sleep apnea syndrome. Am J Respir Crit Care Med 2000; 162: 2208-12.
13. Kushida CA, Efron B, Guilleminault C. A predictive morphometric model for the obstructive sleep apnea syndrome. Ann Intern Med 1997; 127: 581-7.
14- Douglas NJ, Thomas S, Jan MA. Clinical value of polysomnography. Lancet 1992; 339 (8789): 347-50.
15- Calleja JM, Esnaola S, Rubio R, Durán J. Comparison of a cardiorespiratory device vs. Polysomnography for diagnosis of sleep apnea. Eur Respir J 2002; 20: 1-6.
16- Executive Summary on the Systematic Review and Practice Parameters for Portable Monitoring in the Investigation of Suspected Sleep Apnea in Adults. Am J Respir Crit Care Med 2004; 169: 1160-1163.
17. Clinical Guidelines for the Use of Unattended Portable Monitors in the Diagnosis of Obstructive Sleep Apnea in Adult Patients. Portable Monitoring Task Force of the American Academy of Sleep Medicine. Journal of Clinical Sleep Medicine 2007; 3: 7.
18. Trikalinos T, Ip S., Raman G, Cepeda M, Balk E, D´Ambrosio C, Lau J Technology Assessment. Home Diagnosis of Obstructive Sleep Apnea- Hypopnea Syndrome. Department of Health and Human Services. Agency for Healthcare Research and Quality. August 8, 2007
19. Trastornos respiratorios durante el sueño. Consenso Argentino de Trastornos Respiratorios Vinculados. Medicina 2001; Vol 61; 3: 351-363.
20. Guilleminault C. Suspiction of sleep-disordered breathing: which test to perform? Sleep Medicine 2000; 1: 73-75.
21. Masa JF, Corral J, Pereira R, Duran-Cantolla J, Cabello M, Hernández-Blasco L, Monasterio C, Alonso A, Chiner E, Rubio M, Garcia-Ledesma E, Cacelo L, Carpizo R, Sacristan L, Salord N, Carrera M, Sancho-Chust JN, Embid C, Vázquez-Polo FJ, NegrĂn MA, Montserrat JM. Effectiveness of home respiratory polygraphy for the diagnosis of sleep apnoea and hypopnoea syndrome. Thorax. 2011: 66(7): 567-73.
22. Soriano JB, Yáñez A, Renom F, de la Peña M, Gómez A, Duro R, Uréndez A, Román M. Program of Epidemiology and Clinical Research, CIMERA, Fundación Caubet-Cimera Illes Balears, Bunyola, Mallorca, Spain. Prim Care Respir J. 2010; 19 (2): 140-7.
23.Rabec C, Rodenstein D, Leger P, Rouault S, Perrin C, Gonzalez-Bermejo J; SomnoNIV group. Ventilator modes and settings during non-invasive ventilation: effects on respiratory events and implications for their identification. Thorax. 2011; 66(2): 170-8
24. Gonzalez-Bermejo J, Perrin C, Janssens JP, Pepin JL, Mroue G, LĂ©ger P, Langevin B, Rouault S, Rabec C, Rodenstein D; SomnoNIV Group. Proposal for a systematic analysis of polygraphy or polysomnography for identifying and scoring abnormal events occurring during non-invasive ventilation. Thorax. 2012; 67(6): 546-52